Clear Sky Science · nl
DNA-kruisingsmotieven-gebaseerde, programmeerbare supramoleculaire hydrogels voor de mechanoregulerende effecten op cellulair gedrag en reorganisatie van het cytoskelet
Beter, celvriendelijker gel bouwen
Ons lichaam bestaat uit meer dan alleen cellen; ze worden bijeengehouden door zachte, met water verzadigde steigers die elke cel omringen. Deze natuurlijke steigers ondersteunen niet alleen weefsels, maar zenden ook mechanische signalen die cellen vertellen hoe ze moeten groeien, bewegen en gezond blijven. Deze studie laat zien hoe wetenschappers DNA – dezelfde molecule die genetische informatie opslaat – kunnen gebruiken om sterk afstelbare, gelei-achtige materialen te bouwen die deze steigers nabootsen en zacht sturen hoe cellen zich gedragen.
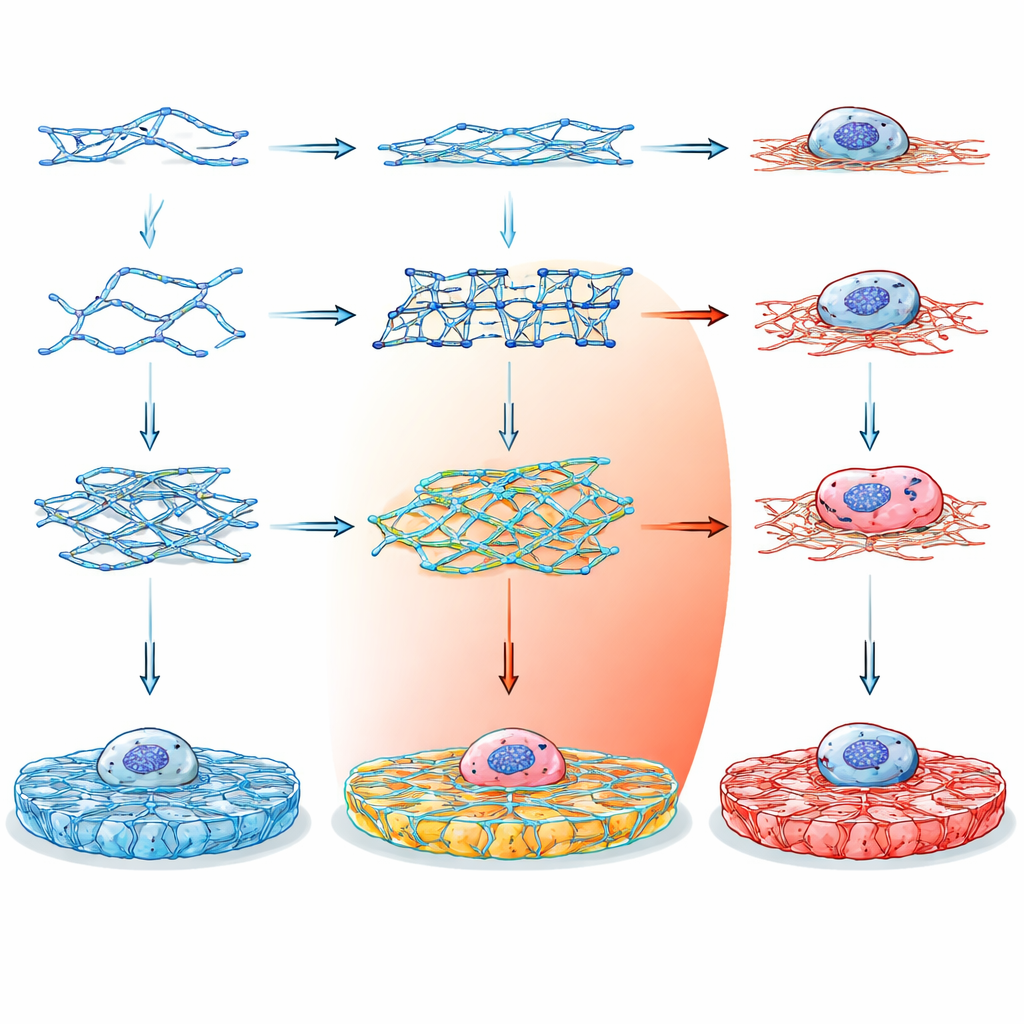
Van genetische code naar slimme gelei
In plaats van te vertrouwen op traditionele materialen zoals collageen of alginaat, die moeilijk fijn af te stemmen zijn zonder extra chemicaliën, richtten de onderzoekers zich op DNA als constructiemateriaal. DNA is aantrekkelijk omdat de bouwregels eenvoudig en voorspelbaar zijn: specifieke basen paren op bekende manieren, wat nauwkeurige controle over vorm en verbinding op nanometerschaal mogelijk maakt. Door korte DNA-strengen te ontwerpen die zich tot verschillende meerarmige kruisingen assembleren, kon het team programmeren hoe de strengen zich verbinden tot een driedimensionale hydrogel – een zacht, met water gevuld vaste stof die eruitziet en aanvoelt als biologisch weefsel.
Een bibliotheek van op maat gemaakte gels ontwerpen
Het team creëerde veertien verschillende DNA-bouwstenen, gegroepeerd in drie hoofdgroepen. Double crossover (DX)-motieven zijn relatief eenvoudige, ladderachtige eenheden; paranemische crossover (PX)-motieven hebben frequentere kruisingen, waardoor ze intrinsiek stijver zijn; en tensegrity-motieven vormen sterachtige eenheden met drie tot zes armen die onder gebalanceerde spanning worden gehouden. Sommige versies hadden stompe uiteinden en konden geen netwerken vormen, en dienden als controles. Andere droegen plakkerige uiteinden die hen in staat stelden in elkaar te haken tot uitgebreide gels, hetzij met flexibele palindromische verbindingen of met meer directionele, niet-palindromische koppelingen. Door strengsequenties zorgvuldig te kiezen en hun stabiliteit met computationele hulpmiddelen te controleren, zorgden de onderzoekers dat elk motief vouwde zoals gepland en biologisch veilig bleef.
De DNA-netwerken zien en voelen
Om te bevestigen dat deze kleine bouwstenen echt grotere structuren vormden, gebruikte het team verschillende visualisatie- en mechanische proeven. Fluorescente kleurstoffen die aan DNA binden, onthulden hoe verschillende motieven zich onder de microscoop tot netwerken organiseerden: sommige vormden losse, klonterige webben, terwijl andere meer regelmatige, gelijkmatig verdeelde mazen creëerden. Atomic force microscopy gaf een gedroogde toestand-weergave op nanometerschaal, en toonde dat tensegrity-gebaseerde gels dikke, gebundelde vezels produceerden die in sommige gevallen leken op natuurlijk collageen. Door de gehydrateerde gels zachtjes te porren met een microscopische cantilever en door bulk-rheometriemetingen uit te voeren, ontdekten ze dat de gels een breed scala aan stijfheden overspanden, van ongeveer 50 tot 185 kilopascal, en dat ze solide-achtig bleven zelfs onder vervormingen die veel groter zijn dan de spanningen die weefsels normaal in het lichaam ervaren.
Cellen reageren op het DNA-landschap
De echte test was of levende cellen deze ontworpen mechanische omgevingen zouden opmerken – en er baat bij zouden hebben. Menselijke retinale pigmentepitheelcellen werden gekweekt op dekglaasjes bedekt met de verschillende DNA-gels en vergeleken met standaardcoatings zoals poly-L-lysine, collageen en commerciële basaalmembraanextracten. Over meerdere DNA-architecturen en concentraties nam de cellulaire levensvatbaarheid toe, in sommige gevallen tot vier keer zo hoog ten opzichte van de zachte poly-L-lysine-controle. Cellen op passend afgestemde DNA-gels spreidden zich meer uit, met grotere oppervlaktes en beter ontwikkelde interne steigers opgebouwd uit actinefilamenten. Hun kernen vergrootten ook, een kenmerk van cellen die stevig met hun omgeving in wisselwerking staan.
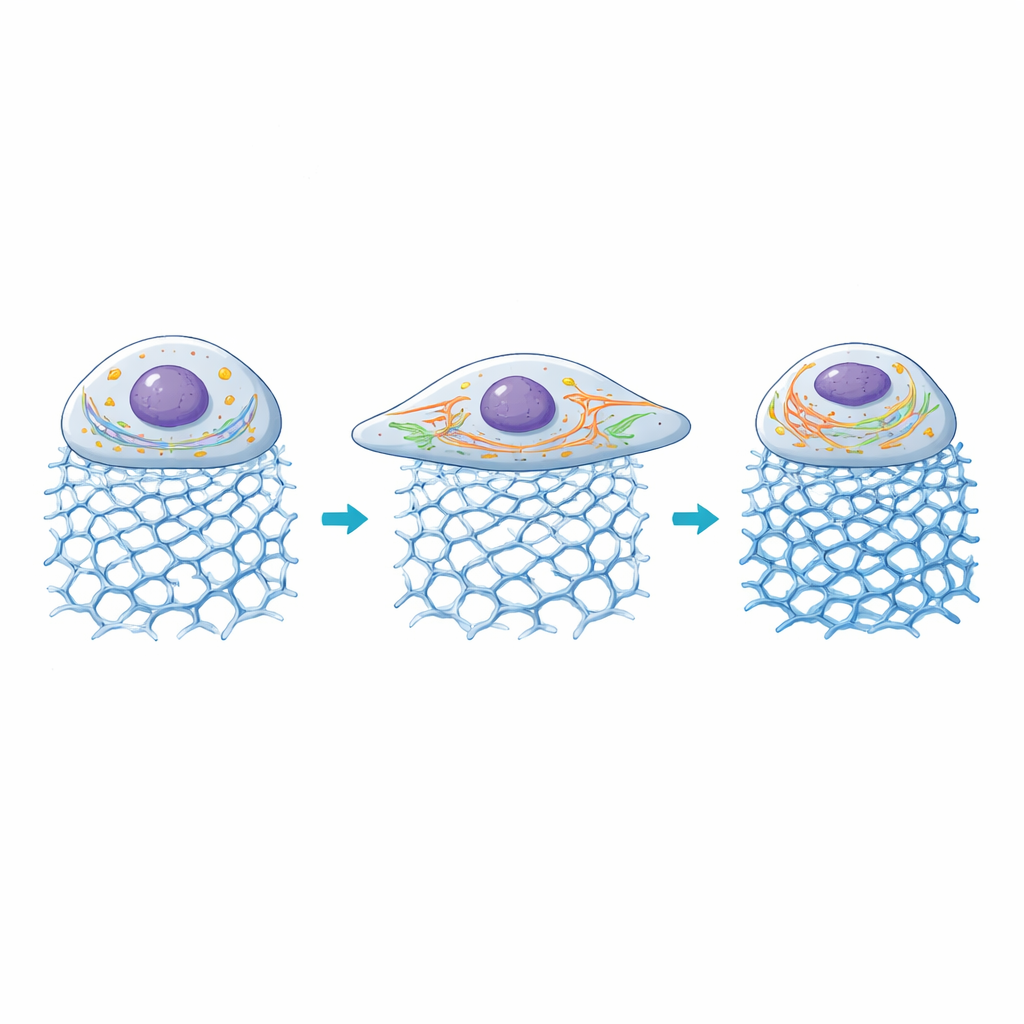
Binnenin de cel: energiecentrales en snelwegen passen zich aan
De onderzoekers bekeken vervolgens hoe twee belangrijke interne structuren reageerden: mitochondriën, die energie leveren, en het endoplasmatisch reticulum (ER), een netwerk dat helpt bij de verwerking van eiwitten en calciumsignalen. Op gels met matige stijfheid raakten mitochondriën meer gefragmenteerd, een toestand die geassocieerd is met een hogere energiedoorvoer tijdens actieve groei, terwijl ER-tubuli verlengden en zich door het vergrote cellichaam verspreidden. Naarmate de stijfheid boven ongeveer 100 kilopascal steeg, begon het celoppervlak weer te krimpen, werden mitochondriale netwerken meer gefuseerd en daalden ER-signalen, wat suggereert dat zeer stijve omgevingen deze cellen uit hun comfortzone duwen. Over het geheel lieten de gels de onderzoekers toe specifieke DNA-architecturen en stijfheidsniveaus te koppelen aan onderscheiden patronen van orgaandelokalisatie en mechanische signalering.
Op weg naar gepersonaliseerde weefselsteigers
Dit werk toont aan dat DNA niet alleen kan dienen als drager van genetische informatie, maar ook als een programmeerbaar bouwmateriaal voor het creëren van celgrootte-landschappen met fijn afgestemde mechanische eigenschappen. Door verschillende DNA-motieven en -sequenties te mixen en te matchen, zou het mogelijk moeten zijn de stijfheid en structuur in te stellen die nodig zijn voor specifieke celtypes of weefsels, en zelfs reactieve elementen toe te voegen die reageren op veranderingen in de omgeving. Dergelijke DNA-gebaseerde hydrogels wijzen op toekomstige gepersonaliseerde steigers die cellen niet alleen in drie dimensies ondersteunen, maar ook actief hun groei, gezondheid en herstel sturen.
Bronvermelding: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
Trefwoorden: DNA-hydrogels, mechanobiologie, weefselengineering, cellulaire mechanotransductie, extracellulaire matrix