Clear Sky Science · ru
Супрамолекулярные гидрогели на основе перекрестных мотивов ДНК, программируемые для механорегуляции клеточного поведения и реорганизации цитоскелета
Создание более благоприятных для клеток гелей
Наши тела состоят не только из клеток; они удерживаются вместе мягкими, насыщенными водой каркасами, окружающими каждую клетку. Эти природные матриксы не только поддерживают ткани, но и передают механические сигналы, которые подсказывают клеткам, как расти, перемещаться и сохранять здоровье. В этом исследовании показано, как учёные могут использовать ДНК — ту же молекулу, что хранит генетическую информацию — для создания легко настраиваемых студнеподобных материалов, имитирующих такие матриксы и мягко направляющих поведение клеток.
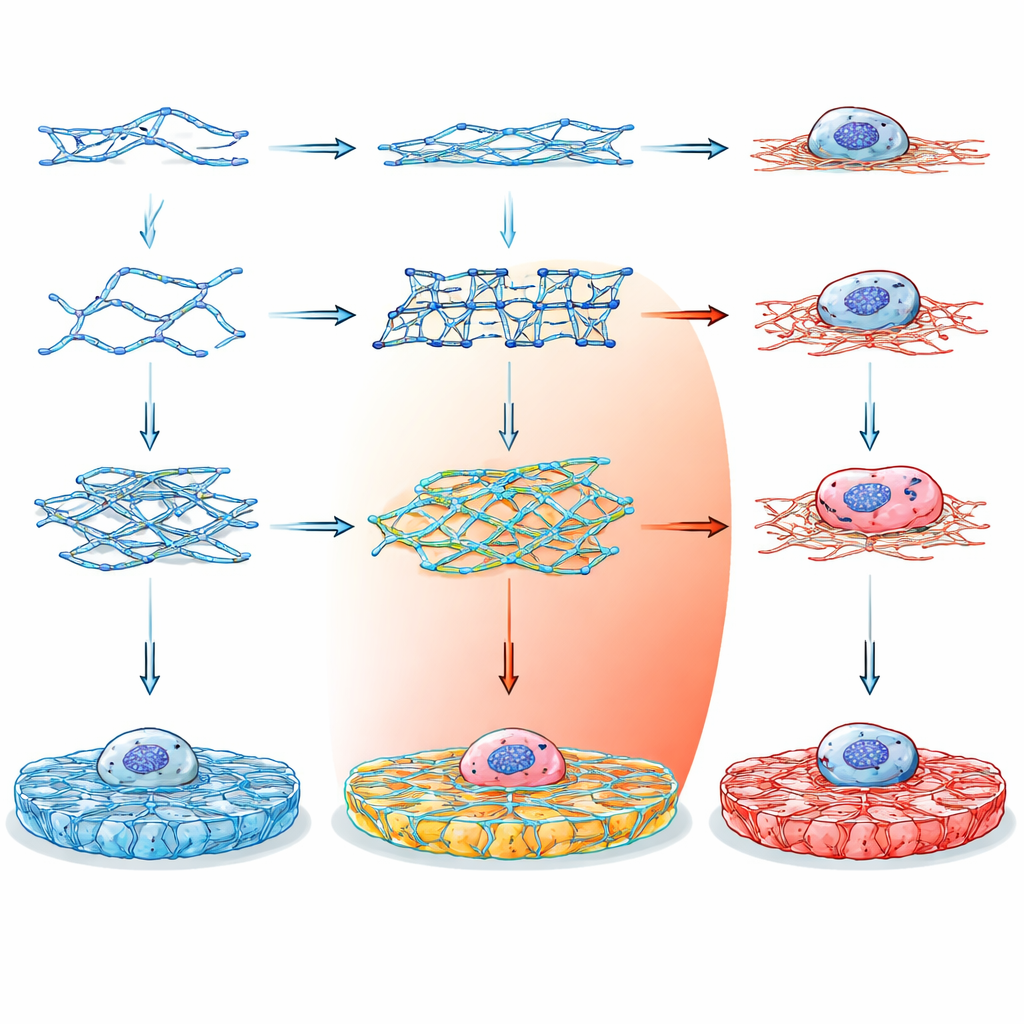
От генетического кода к умному желе
Вместо того чтобы полагаться на традиционные материалы, такие как коллаген или альгинат, которые сложно тонко регулировать без добавления дополнительных химикатов, исследователи обратились к ДНК как к строительному материалу. ДНК привлекательна тем, что правила её сборки просты и предсказуемы: специфические основания спариваются известными способами, что даёт точный контроль формы и связности на нанометровом уровне. Проектируя короткие цепочки ДНК, которые собираются в различные многошарнирные узлы, команда могла запрограммировать то, как звенья соединяются в трёхмерный гидрогель — мягкое, наполненное водой твердое тело, похожее по виду и ощущениям на биологическую ткань.
Создание библиотеки кастомных гелей
Команда разработала четырнадцать различных строительных блоков из ДНК, сгруппированных в три основные семьи. Мотивы с двойным перекрёстком (DX) — относительно простые, лестничные элементы; паранемические перекрёстки (PX) имеют более частые перекрёстные связи, что делает их по своей природе жёстче; а мотивы тенсегрити формируют звездообразные узлы с три- до шестирукими ветвями, удерживаемыми в сбалансированном натяжении. Некоторые варианты имели тупые концы и не могли образовывать сети, служа контролями. Другие несли липкие концы, позволявшие им сцепляться в протяжённые гели — либо с гибкими палиндромными соединениями, либо с более направленными, непалиндромными связями. Тщательно подбирая последовательности цепочек и проверяя их стабильность с помощью вычислительных инструментов, исследователи обеспечили, что каждый мотив складывается согласно замыслу и остаётся биологически безопасным.
Наблюдение и ощупывание ДНК-сетей
Чтобы подтвердить, что эти крошечные строительные блоки действительно формируют более крупные структуры, команда использовала несколько методов визуализации и механических зондов. Флуоресцентные красители, связывающиеся с ДНК, показали, как разные мотивы организуются в сети под микроскопом: некоторые образовывали рыхлые, скомканные паутины, тогда как другие создавали более регулярные, равномерно распределённые ячейки. Сканирующая атомная сила показала вид в высушенном состоянии на нанометровом уровне, продемонстрировав, что гели на основе тенсегрити образуют толстые, связанные пучки волокон, которые в некоторых случаях напоминали натуральный коллаген. Аккуратно протыкая гидратированные гели микроскопическим кантилевером и проводя реологические измерения объемных свойств, они обнаружили, что жёсткость гелей варьировалась в широких пределах — примерно от 50 до 185 килопаскалей — и оставалась подобной твердым материалам даже при деформациях, намного превосходящих те, что обычно испытывают ткани в организме.
Клетки реагируют на ДНК-ландшафт
Истинной проверкой было то, заметят ли живые клетки — и получат ли от этого выгоду — эти созданные механические условия. Человеческие пигментные эпителиальные клетки сетчатки выращивали на покровных стеклах, покрытых различными ДНК-гелями, и сравнивали со стандартными покрытиями, такими как поли-L-лизин, коллаген и коммерческие экстракты базальной мембраны. Во множестве архитектур и концентраций ДНК жизнеспособность клеток увеличивалась, в некоторых случаях в четыре раза по сравнению с мягким контролем на поли-L-лизине. Клетки на адекватно настроенных ДНК-гелях сильнее растягивались, занимая большую площадь и имея лучше развитый внутренний каркас из актиновых филаментов. Также их ядра увеличивались в размерах — признак активного взаимодействия клетки с окружением.
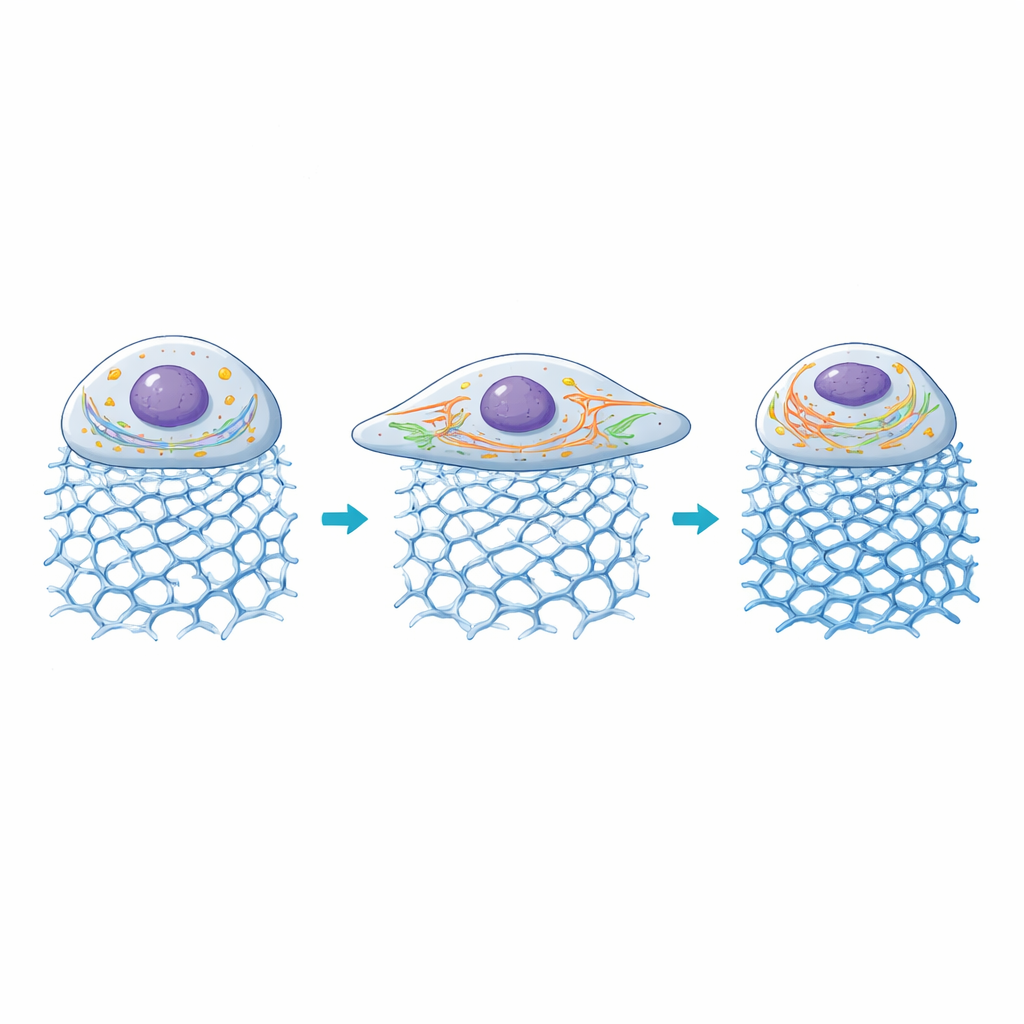
Внутри клетки: митохондрии и магистрали адаптируются
Затем исследователи изучили, как реагируют две ключевые внутриклеточные структуры: митохондрии, обеспечивающие энергией, и эндоплазматический ретикулум (ЭР), сеть, помогающая обрабатывать белки и сигналы кальция. На гелях умеренной жёсткости митохондрии становились более фрагментированными — состояние, связанное с повышенным энергетическим оборотом при активном росте, — в то время как трубочки ЭР удлинялись и распространялись по увеличенному объёму клетки. По мере увеличения жёсткости выше примерно 100 килопаскалей площадь клетки снова начинала сокращаться, митохондриальные сети становились более слившимися, а сигналы ЭР снижались, что указывает на то, что слишком жёсткая среда выводит эти клетки из зоны комфорта. В целом гели позволили учёным связать конкретные ДНК-архитектуры и уровни жёсткости с отличительными паттернами организации органелл и механического сигнального ответа.
К персонализированным каркасам для тканей
Эта работа демонстрирует, что ДНК может служить не только носителем генетической информации, но и программируемым строительным материалом для создания клеткоразмерных ландшафтов с точно настроенными механическими свойствами. Смешивая и сочетая разные ДНК-мотивы и последовательности, можно будет задавать жёсткость и структуру, необходимые для конкретных типов клеток или тканей, и даже добавлять отзывчивые элементы, реагирующие на изменения в окружающей среде. Такие ДНК-основные гидрогели открывают путь к будущим персонализированным каркасам, которые не только поддерживают клетки в трёх измерениях, но и активно направляют их рост, здоровье и восстановление.
Цитирование: Singh, A., Yadav, A., Singh, N. et al. DNA cross-over motifs-based, programmable supramolecular hydrogels for the mechanoregulatory effects of cellular behaviour and cytoskeleton reorganization. npj Biomed. Innov. 3, 30 (2026). https://doi.org/10.1038/s44385-026-00083-9
Ключевые слова: ДНК-гидрогели, механобиология, тканевая инженерия, клеточная механотрансдукция, внеклеточный матрикс