Clear Sky Science · zh
网蛋白-1通过PPARγ和Wnt/β-连环蛋白信号通路扰乱高脂饮食诱导的脂肪生成
这对日常健康意味着什么
肥胖和2型糖尿病常被归咎于“脂肪过多”,但事实更微妙:我们身体储存多余热量的方式与部位,可能会保护我们,也可能将我们推向疾病。本研究揭示了这一过程中一个出人意料的参与者——一种名为网蛋白-1的引导神经蛋白,脂肪组织也会产生该蛋白。研究者表明,在高脂饮食条件下,网蛋白-1会削弱机体以健康方式重塑脂肪的能力,导致血糖控制变差。了解这种对“良好”脂肪扩张的隐性制动,有望为治疗肥胖相关糖尿病打开新途径。
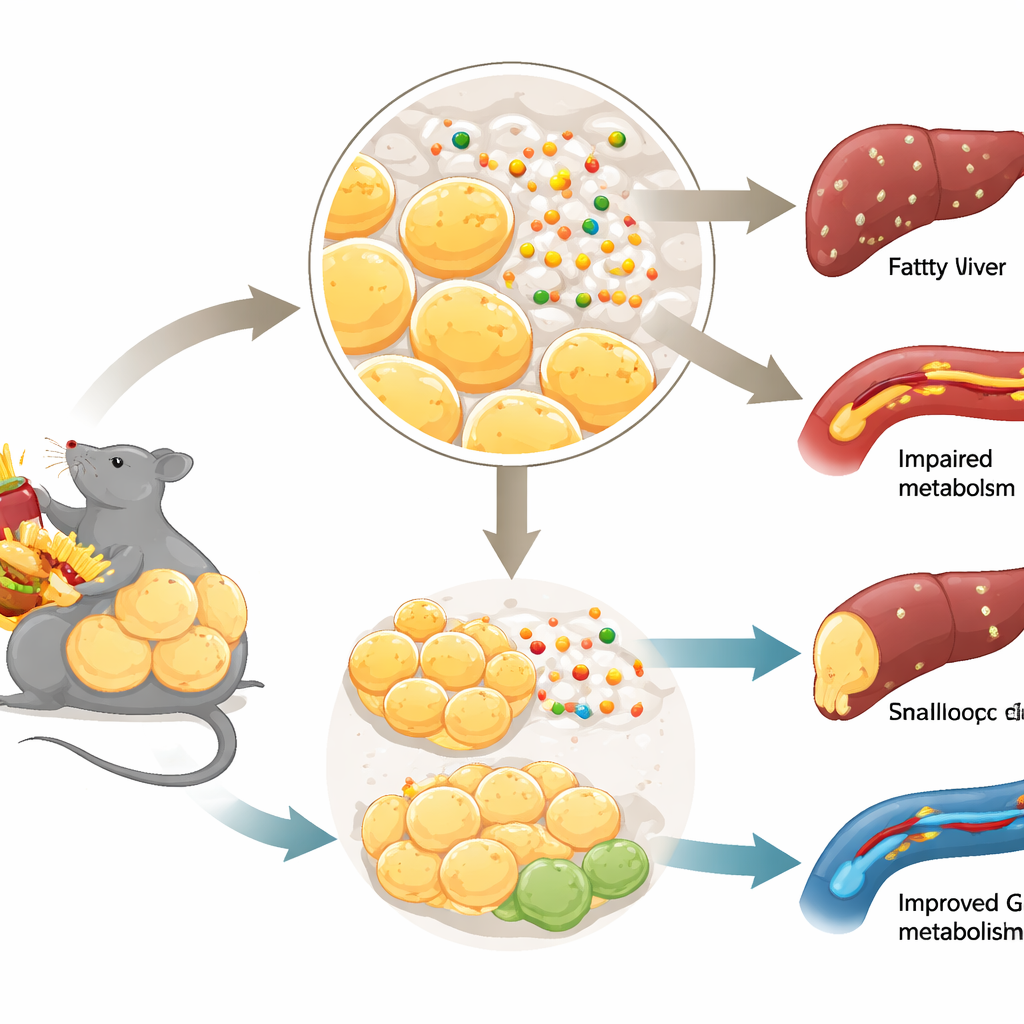
良性脂肪、恶性脂肪与血糖控制
并非所有体脂表现相同。当多余热量通过生成许多小型脂肪细胞被安全储存——尤其是在皮下时——代谢可以保持出乎意料的健康。相比之下,当脂肪储存受阻,脂肪细胞功能失常,脂肪会溢出到肝脏和肌肉等器官。这种“有害”重塑与胰岛素抵抗和2型糖尿病相关。团队关注前体细胞如何分化形成新脂肪细胞的过程(称为脂肪生成),并探究长期以指导生长的神经纤维而闻名的网蛋白-1,是否会影响脂肪组织中的该过程。
关闭网蛋白-1使高脂饮食的危害减轻
为测试网蛋白-1的作用,研究者构建了在脂肪组织中特异性缺失网蛋白-1的小鼠。当这些动物在八周内喂以高脂饮食时,体重实际上比正常小鼠增多——但血糖控制更好。它们表现出更佳的胰岛素反应、较低的空腹血糖及下降的循环脂质水平。影像学和组织测量显示,这部分额外体重主要来自腹股沟附近的皮下白色脂肪增生,这是一个通常与代谢保护相关的脂肪库。增大的脂肪量并非由细胞过度膨胀引起,而是细胞数量增加和疤痕(纤维化)减少,两者都表明脂肪重塑更健康。肝脏脂肪堆积也减少,提示扩张的脂肪库在安全地储存本可能损害其他器官的多余脂质。
过多的网蛋白-1促向糖尿病发展
研究者随后反向操作,通过基因递送病毒促使脂肪组织产生额外的网蛋白-1。在正常和高脂喂养的小鼠中,这种网蛋白-1水平的升高并未显著改变体重,但确实使葡萄糖耐受性恶化并提高血脂。脂肪库相对于体重倾向缩小,而肝脏显示更多脂肪积累。结合细胞培养实验,这些结果表明网蛋白-1在脂肪组织内抑制新功能性脂肪细胞的形成。当网蛋白-1升高时,前体细胞分裂减少,且不易成熟为能有效储存脂质并对胰岛素有反应的脂肪细胞。
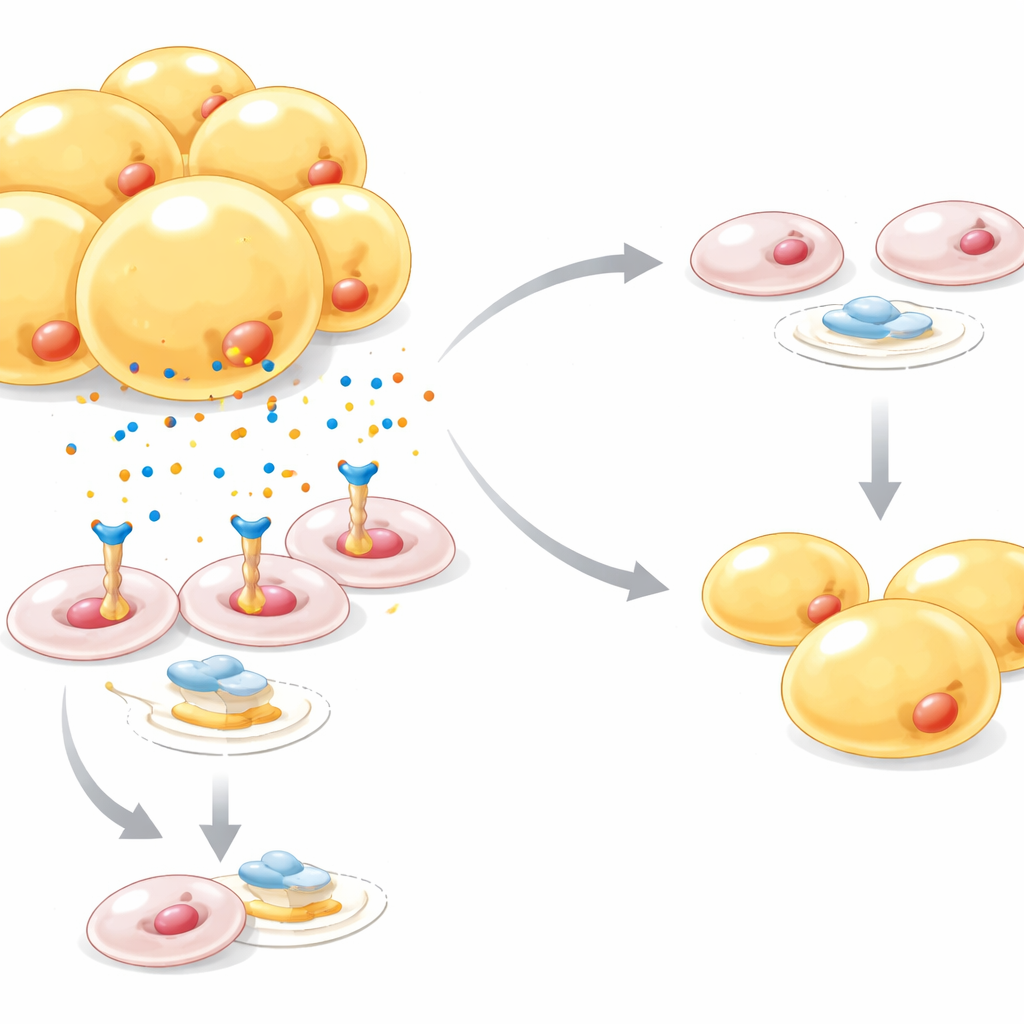
构建新脂肪细胞的分子制动器
进一步研究显示,网蛋白-1抑制了脂肪细胞发育的主开关PPARγ,同时激活了另一条已知可抵消脂肪生成的信号通路Wnt/β-连环蛋白。在鼠类和人类数据集中,网蛋白-1在肥胖和2型糖尿病中水平更高,并在前体细胞中相较于成熟脂肪细胞更为富集。当在人前体细胞中人工提高网蛋白-1时,它们积累的脂滴更少;用一种糖尿病药物激活PPARγ可以在很大程度上逆转这一效应,阻断β-连环蛋白也能缓解网蛋白-1对脂肪细胞成熟的抑制。另一个调控层来自于过度增长脂肪库内的低氧应激:缺氧传感器HIF‑1α直接增强了网蛋白-1基因活性,将高脂饮食引发的氧气短缺与这一反脂肪生成信号连接起来。
这对未来治疗意味着什么
通俗地说,这项工作表明,当我们过度进食时,脂肪组织会尝试生长新细胞以安全地停放多余热量。但在高脂饮食下,局部氧气压力启动网蛋白-1,进而告诉邻近的前体细胞停止成为新的脂肪细胞。结果,脂肪储存被推向不那么健康的模式,血糖升高,胰岛素作用减弱。通过把网蛋白-1鉴定为将受压脂肪组织与不良代谢健康联系起来的关键信使,研究指出了一个潜在的新治疗策略:降低网蛋白-1或其下游通路的活性,可能有助于机体扩展“良好”的脂肪库,更好地缓冲2型糖尿病,即便在热量摄入较高的情况下。
引用: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
关键词: 脂肪组织, 网蛋白-1, 2型糖尿病, 高脂饮食, PPARγ 信号