Clear Sky Science · es
Netrin-1 interfiere en la adipogénesis inducida por dieta alta en grasas a través de las vías de señalización PPARγ y Wnt/β‑catenina
Por qué importa para la salud cotidiana
La obesidad y la diabetes tipo 2 suelen atribuirse a “demasiada grasa”, pero la realidad es más matizada: cómo y dónde almacena el cuerpo las calorías extra puede protegernos o predisponernos a la enfermedad. Este estudio revela un actor inesperado en esa historia: una proteína guía de nervios llamada Netrin-1 que también es producida por el tejido adiposo. Los investigadores muestran que, bajo una dieta alta en grasas, Netrin-1 puede sabotear la capacidad del organismo para remodelar la grasa de forma saludable, empeorando el control de la glucemia. Comprender este freno oculto a la expansión “buena” de la grasa podría abrir nuevas vías para tratar la diabetes asociada a la obesidad.
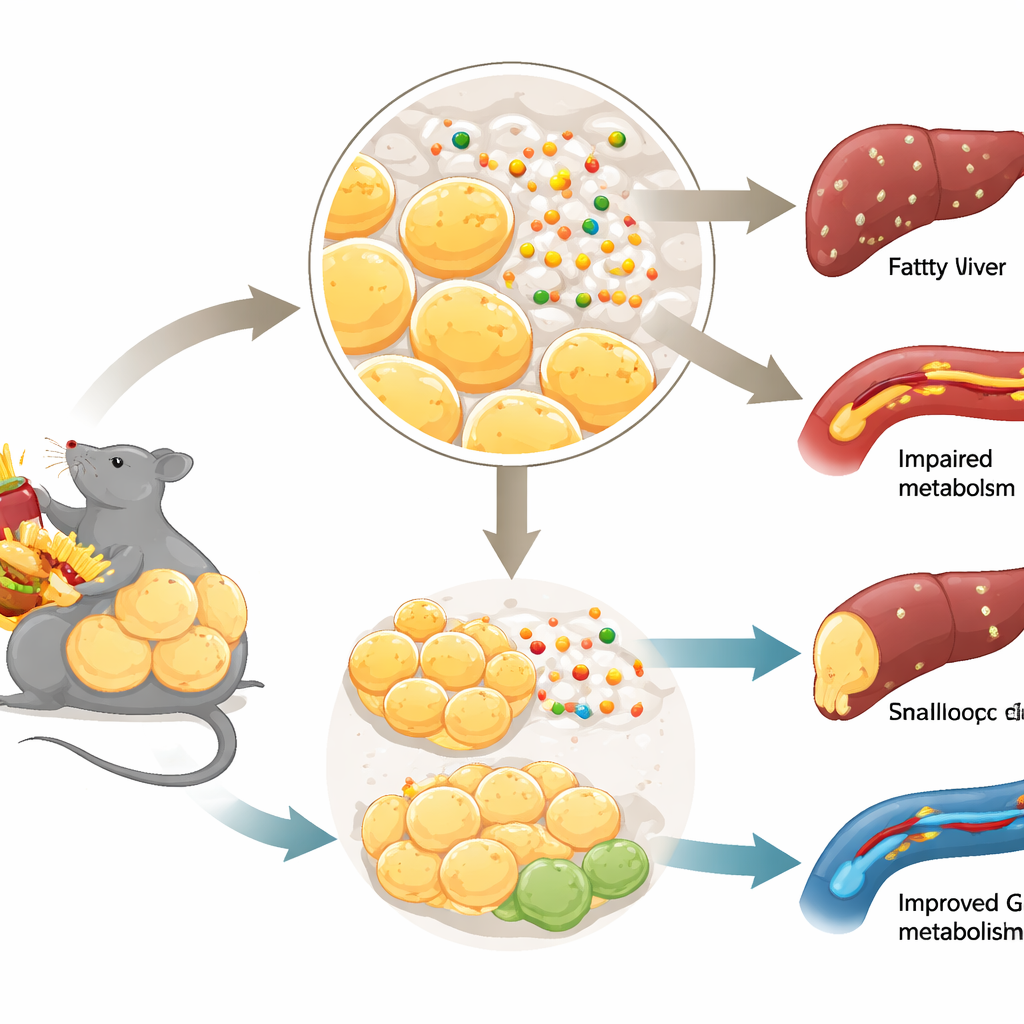
Grasa buena, grasa mala y control del azúcar
No toda la grasa corporal se comporta igual. Cuando las calorías excedentes se almacenan de forma segura creando muchas células grasas pequeñas—especialmente justo bajo la piel—el metabolismo puede permanecer sorprendentemente saludable. En cambio, cuando el almacenamiento de grasa se bloquea, las células grasas se vuelven disfuncionales y la grasa se derrama a órganos como el hígado y los músculos. Esta remodelación “mala” está ligada a la resistencia a la insulina y a la diabetes tipo 2. El equipo se centró en cómo se forman nuevas células grasas a partir de precursores, un proceso llamado adipogénesis, y se preguntó si Netrin-1, conocido desde hace tiempo por guiar fibras nerviosas en crecimiento, podría influir en este proceso en el tejido adiposo.
Apagar Netrin-1 hace que las dietas altas en grasas sean menos dañinas
Para probar el papel de Netrin-1, los investigadores diseñaron ratones que carecen de Netrin-1 específicamente en el tejido adiposo. Cuando estos animales fueron alimentados con una dieta alta en grasas durante ocho semanas, en realidad ganaron más peso que los ratones normales—pero su control glucémico fue mejor. Mostraron respuestas a la insulina mejoradas, glucosa en ayunas más baja y niveles reducidos de lípidos circulantes. Las imágenes y las mediciones de tejido revelaron que este peso adicional se debió principalmente a la expansión de la grasa blanca subcutánea cerca de la región inguinal, un depósito a menudo asociado con protección metabólica. La mayor masa grasa no se debió a células sobrecargadas, sino a un aumento en el número de células y a una menor fibrosis, ambos signos de una remodelación grasa más saludable. La acumulación de grasa en el hígado también se redujo, lo que sugiere que el depósito ampliado almacenaba de forma segura los lípidos excedentes que de otro modo dañarían otros órganos.
Exceso de Netrin-1 empuja hacia la diabetes
Los científicos invirtieron luego el experimento y forzaron al tejido adiposo a producir Netrin-1 adicional mediante un virus de entrega génica. En ratones normales y en aquellos alimentados con dieta alta en grasas, este aumento de Netrin-1 no cambió mucho el peso corporal, pero sí empeoró la tolerancia a la glucosa y elevó los lípidos sanguíneos. Los depósitos de grasa tendieron a reducirse en proporción al tamaño corporal, mientras que el hígado mostró mayor acumulación de grasa. Junto con experimentos en cultivo celular, estos hallazgos indican que Netrin-1 actúa dentro del tejido adiposo para frenar la formación de nuevas células grasas funcionales. Cuando Netrin-1 está elevado, las células precursoras se dividen menos y tienen menor capacidad para madurar en adipocitos que almacenen lípidos eficientemente y respondan a la insulina.
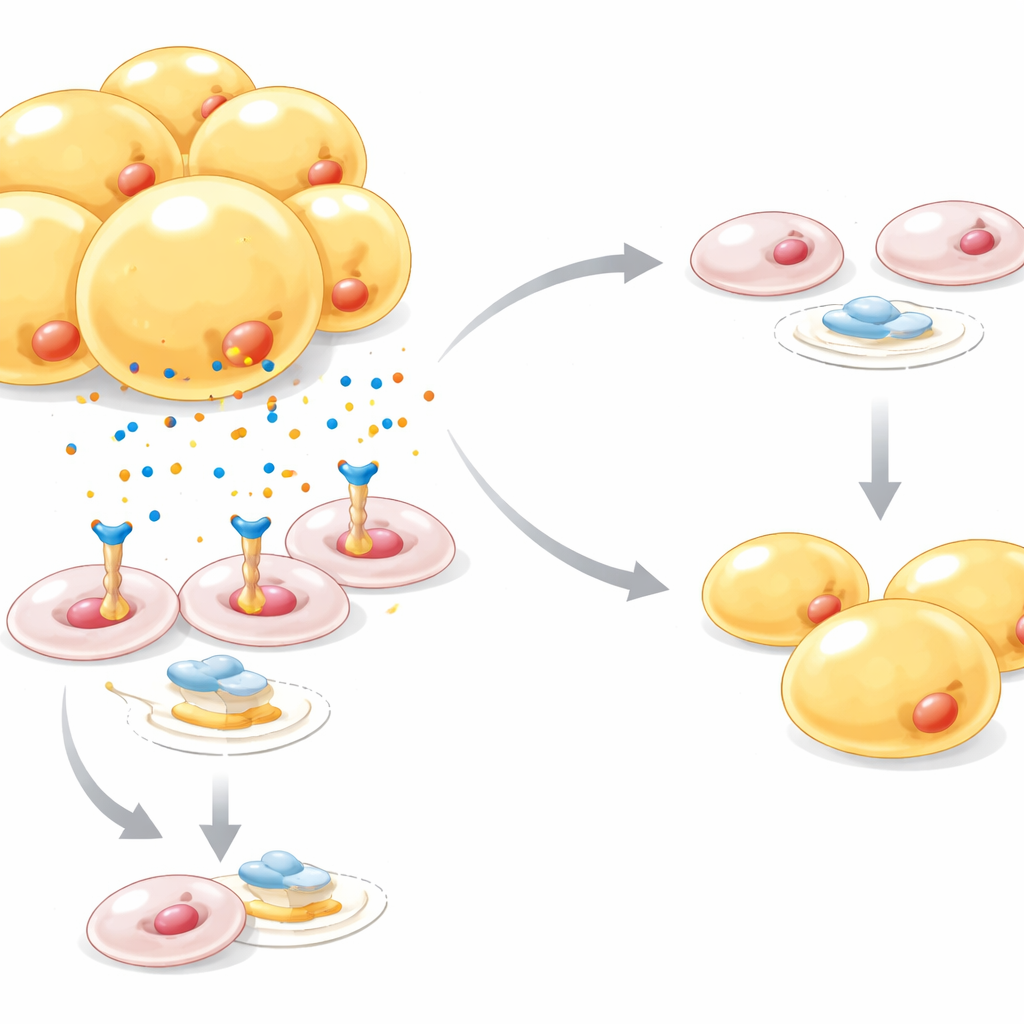
Un freno molecular a la formación de nuevas células grasas
Indagando más, el equipo mostró que Netrin-1 atenúa un interruptor maestro para el desarrollo de adipocitos llamado PPARγ, a la vez que activa una vía de señalización diferente conocida como Wnt/β‑catenina, que se sabe que se opone a la formación de adipocitos. En conjuntos de datos de ratón y humano, los niveles de Netrin-1 fueron más altos en la obesidad y la diabetes tipo 2, y se concentraron en las células precursoras en comparación con las células adiposas maduras. Cuando Netrin-1 se aumentó artificialmente en las células precursoras, acumularon menos gotas lipídicas; la activación de PPARγ con un fármaco antidiabético pudo rescatar en gran medida este efecto, y el bloqueo de β‑catenina también alivió el freno de Netrin-1 sobre la maduración de los adipocitos. Otra capa de control provino del estrés por baja oxigenación dentro de depósitos de grasa sobredimensionados: el sensor de hipoxia HIF‑1α impulsó directamente la actividad génica de Netrin-1, vinculando la escasez de oxígeno inducida por dieta alta en grasas con esta señal antiadipogénica.
Qué significa esto para tratamientos futuros
En términos accesibles, este trabajo sugiere que cuando comemos en exceso, nuestro tejido adiposo intenta generar nuevas células para aparcar las calorías extra de forma segura. Pero bajo una dieta alta en grasas, el estrés local por falta de oxígeno activa Netrin-1, que entonces indica a las células precursoras cercanas que dejen de convertirse en adipocitos nuevos. Como resultado, el almacenamiento de grasa se desplaza hacia patrones menos saludables, la glucosa en sangre aumenta y la insulina funciona peor. Al identificar a Netrin-1 como un mensajero clave que enlaza el tejido adiposo estresado con la mala salud metabólica, el estudio apunta a una posible estrategia terapéutica nueva: reducir Netrin-1, o sus vías descendentes, podría ayudar al cuerpo a expandir depósitos de grasa “buenos” y amortiguar mejor contra la diabetes tipo 2, incluso cuando la ingesta calórica es alta.
Cita: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
Palabras clave: tejido adiposo, Netrin-1, diabetes tipo 2, dieta alta en grasas, señalización PPARγ