Clear Sky Science · ru
Netrin-1 нарушает индуцируемую жирной диетой адипогенез через пути сигнализации PPARγ и Wnt/β-катенин
Почему это важно для повседневного здоровья
Ожирение и сахарный диабет 2 типа часто сводят к «слишком большому количеству жира», но картина гораздо тоньше: то, как и где наш организм хранит избыточные калории, может либо защищать нас, либо толкать к болезни. В этом исследовании выявлен неожиданный участник этой истории — направляющий нервы белок Netrin-1, который также вырабатывается жировой тканью. Ученые показывают, что при жирной диете Netrin-1 способен подрывать способность организма здорово перестраивать жировую ткань, ухудшая контроль уровня сахара в крови. Понимание этого скрытого тормоза «хорошего» расширения жировых депо может открыть новые пути лечения, связанных с ожирением форм диабета.
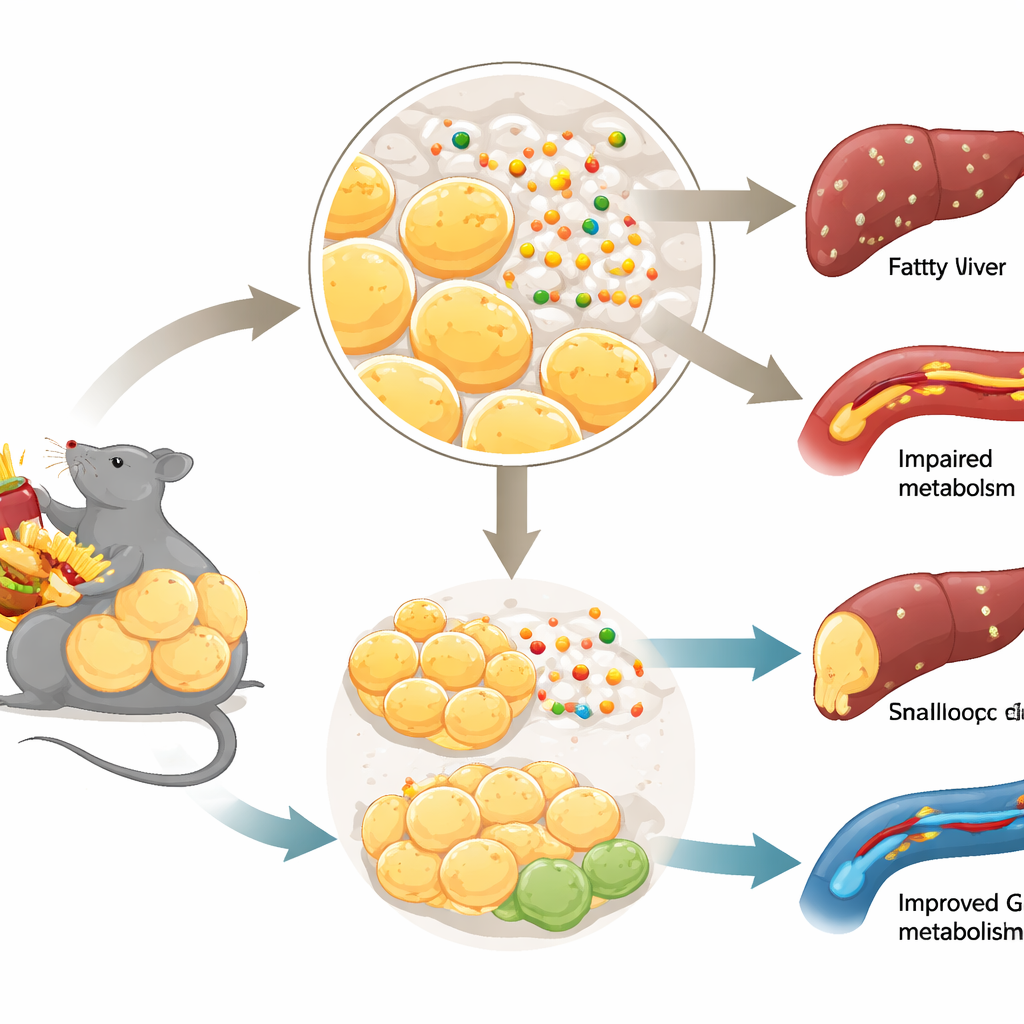
Хороший жир, плохой жир и контроль сахара
Не весь жир в организме ведет себя одинаково. Когда избыточные калории безопасно запасаются за счет образования множества мелких жировых клеток — особенно непосредственно под кожей — обмен веществ может оставаться удивительно здоровым. Напротив, когда хранение жира блокируется, жировые клетки становятся дисфункциональными, и жир распространяется по органам, таким как печень и мышцы. Такая «плохая» перестройка связана с инсулинорезистентностью и диабетом 2 типа. Команда сосредоточилась на том, как новые жировые клетки формируются из предшественников, процессе, называемом адипогенезом, и задала вопрос, может ли Netrin-1, давно известный как направитель растущих нервных волокон, влиять на этот процесс в жировой ткани.
Отключение Netrin-1 делает вред жирной диеты менее заметным
Чтобы проверить роль Netrin-1, исследователи создали мышей, у которых Netrin-1 отсутствовал специфически в жировой ткани. Когда этих животных кормили жирной диетой в течение восьми недель, они фактически набрали больше веса, чем обычные мыши, но у них наблюдался лучший контроль сахара в крови. У них улучшилась реакция на инсулин, снизился уровень глюкозы натощак и уменьшились циркулирующие концентрации жиров. Визуализация и измерения тканей показали, что этот дополнительный набор веса в основном был обусловлен расширением подкожного белого жира в области паха — депо, часто ассоциируемого с метаболической защитой. Увеличение массы жира было вызвано не переполнением отдельных клеток, а увеличением их числа и уменьшением рубцевания, что свидетельствует о более здоровой перестройке. Отложение жира в печени также уменьшилось, что указывает на то, что расширенное жировое депо безопасно запасало избыточные липиды, которые в противном случае повредили бы другие органы.
Избыток Netrin-1 толкает к диабету
Затем ученые провели обратный эксперимент и заставили жировую ткань производить избыток Netrin-1 с помощью вируса для доставки гена. У мышей как на обычной, так и на жирной диете повышение уровня Netrin-1 существенно не изменяло массу тела, но ухудшало толерантность к глюкозе и повышало уровень циркулирующих жиров. Жировые депо, как правило, уменьшались относительно массы тела, в то время как в печени накапливалось больше жира. Вкупе с опытом на клеточных культурах эти данные указывают, что Netrin-1 действует в самой жировой ткани, притормаживая формирование новых функциональных жировых клеток. При высоком Netrin-1 предшественники делятся меньше и хуже созревают в клетки, способные эффективно запасать липиды и реагировать на инсулин.
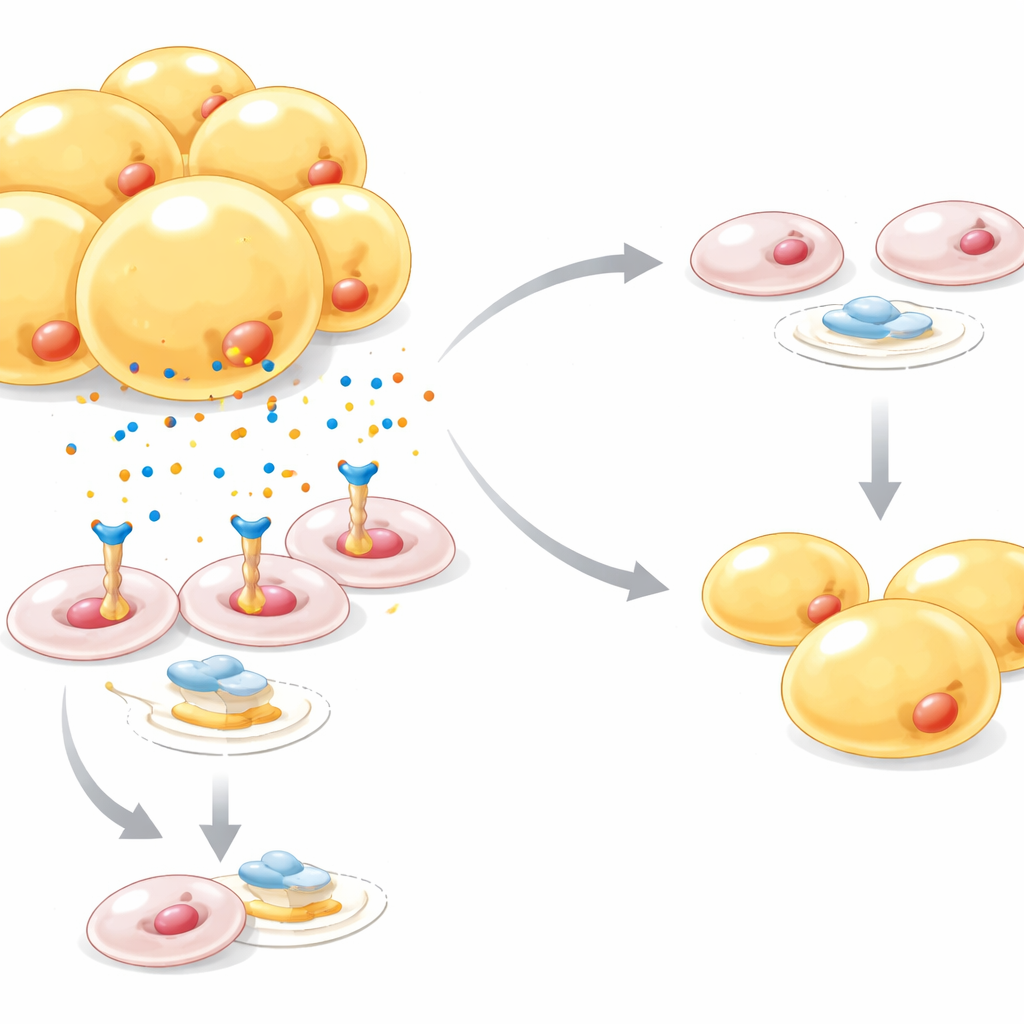
Молекулярный тормоз на формирование новых жировых клеток
Углубившись в механизм, команда показала, что Netrin-1 подавляет главный переключатель развития жировых клеток — PPARγ, одновременно активируя отдельный сигнальный маршрут Wnt/β-катенин, известный как противодействующий адипогенезу. В наборах данных мышей и людей уровни Netrin-1 были выше при ожирении и диабете 2 типа и концентрировались в предшественниках по сравнению со зрелыми жировыми клетками. При искусственном повышении Netrin-1 в предшественниках они накапливали меньше жировых капель; активация PPARγ с помощью противодиабетического препарата в значительной степени восстанавливала этот эффект, а блокада β-катенина также ослабляла тормозящее действие Netrin-1 на созревание жировых клеток. Еще один уровень регуляции возникал из-за дефицита кислорода внутри разросшихся жировых депо: сенсор гипоксии HIF‑1α прямо усиливал активность гена Netrin-1, связывая индуцированный жирной диетой дефицит кислорода с этим антиадипогенным сигналом.
Что это значит для будущих способов лечения
Проще говоря, эта работа предлагает, что при переедании наша жировая ткань пытается создать новые клетки, чтобы безопасно перераспределить лишние калории. Но при жирной диете локальный стресс из‑за нехватки кислорода включает Netrin-1, который затем «приказывает» близлежащим предшественникам перестать становиться новыми жировыми клетками. В результате хранение жира переходит в менее здоровые схемы, уровень сахара в крови повышается, а действие инсулина ослабляется. Выявив Netrin-1 как ключевой посредник, связывающий стрессовую жировую ткань с ухудшением метаболического здоровья, исследование указывает на потенциальную новую терапевтическую стратегию: снижение активности Netrin-1 или его сигнальных путей может помочь организму расширять «полезные» жировые депо и лучше защищать от диабета 2 типа, даже при высоком потреблении калорий.
Цитирование: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
Ключевые слова: жировая ткань, Netrin-1, сахарный диабет 2 типа, жирная диета, сигнализация PPARγ