Clear Sky Science · sv
Netrin-1 stör fetmaframkallad adipogenes via PPARγ- och Wnt/β-catenin‑signalvägarna
Varför detta betyder något för vardagshälsan
Fetma och typ 2‑diabetes skylls ofta på ”för mycket fett”, men verkligheten är mer nyanserad: hur och var kroppen lagrar överskottskalorier kan antingen skydda oss eller driva oss mot sjukdom. Denna studie avslöjar en oväntad aktör i den berättelsen, ett nervstyrande protein kallat Netrin‑1 som också produceras av fettvävnad. Forskarna visar att Netrin‑1 vid en fettrik kost kan sabotera kroppens förmåga att omforma fett på ett hälsosamt sätt och därigenom förvärra blodsockerkontrollen. Att förstå denna dolda broms på ”bra” fettrans expansion kan öppna nya vägar för behandling av fetmarelaterad diabetes.
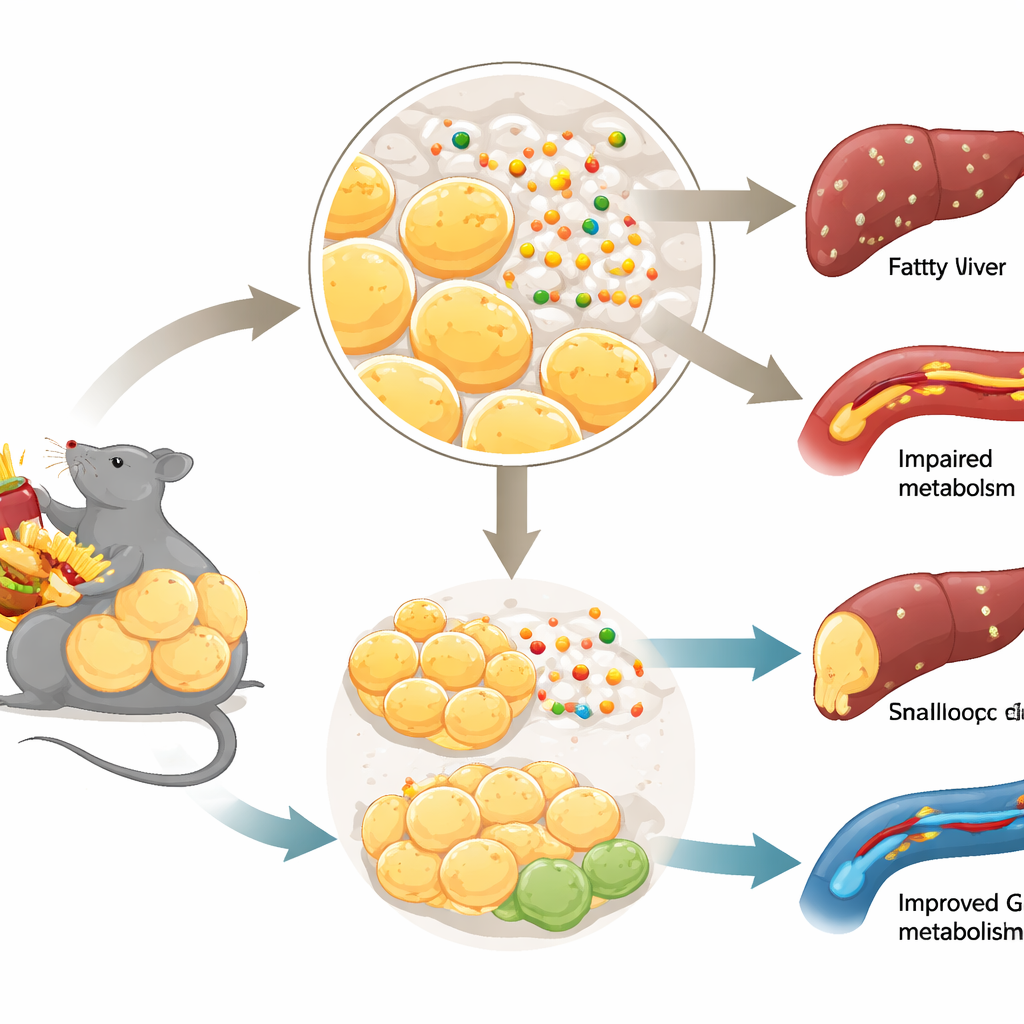
Bra fett, dåligt fett och sockerkontroll
Inte allt kroppsfett beter sig likadant. När överskottskalorier lagras säkert genom att bilda många små fettceller—särskilt strax under huden—kan ämnesomsättningen förbli förvånansvärt hälsosam. Däremot, när fettlagring blockeras, blir fettceller dysfunktionella och fett läcker över till organ som levern och musklerna. Denna ”dåliga” ombyggnad kopplas till insulinresistens och typ 2‑diabetes. Teamet koncentrerade sig på hur nya fettceller bildas från prekursorceller, en process som kallas adipogenes, och frågade om Netrin‑1, länge känt för att styra växande nervtrådar, kan påverka denna process i fettvävnad.
Att stänga av Netrin‑1 gör fettrik kost mindre skadlig
För att testa Netrin‑1:s roll konstruerade forskarna möss som saknar Netrin‑1 specifikt i fettvävnad. När dessa djur matades med en fettrik kost i åtta veckor gick de faktiskt upp mer i vikt än normala möss—men deras blodsockerkontroll var bättre. De visade förbättrade insulinsvar, lägre fasteglukos och minskade nivåer av cirkulerande fetter. Avbildning och vävnadsmätningar visade att denna extra vikt mestadels berodde på expansion av subkutant vitt fett i ljumskeområdet, en depå som ofta förknippas med metabolt skydd. Den förstorade fettmängden orsakades inte av överfyllda celler, utan av en ökning i cellantal och minskad ärrbildning, båda tecken på hälsosammare fettreformering. Fettansamling i levern var också minskad, vilket tyder på att den utvidgade fettdepån säkert lagrade överskottslipider som annars kunde ha skadat andra organ.
För mycket Netrin‑1 skjuter mot diabetes
Forskarna vände sedan experimentet och tvingade fettvävnad att producera extra Netrin‑1 med hjälp av ett genleveransvirus. Hos både normala och fettrik-matade möss förändrade den höjda Netrin‑1‑nivån inte kroppsvikten kraftigt, men försämrade glukostolerans och ökade blodfetter. Fettdepåer tenderade att krympa i förhållande till kroppsstorlek, medan levern uppvisade mer fettansamling. Tillsammans med cellkultureexperiment tyder dessa fynd på att Netrin‑1 verkar i fettvävnaden för att dämpa bildandet av nya, funktionella fettceller. När Netrin‑1 är hög delar sig prekursorceller mindre och har sämre förmåga att mogna till fettceller som effektivt lagrar lipider och svarar på insulin.
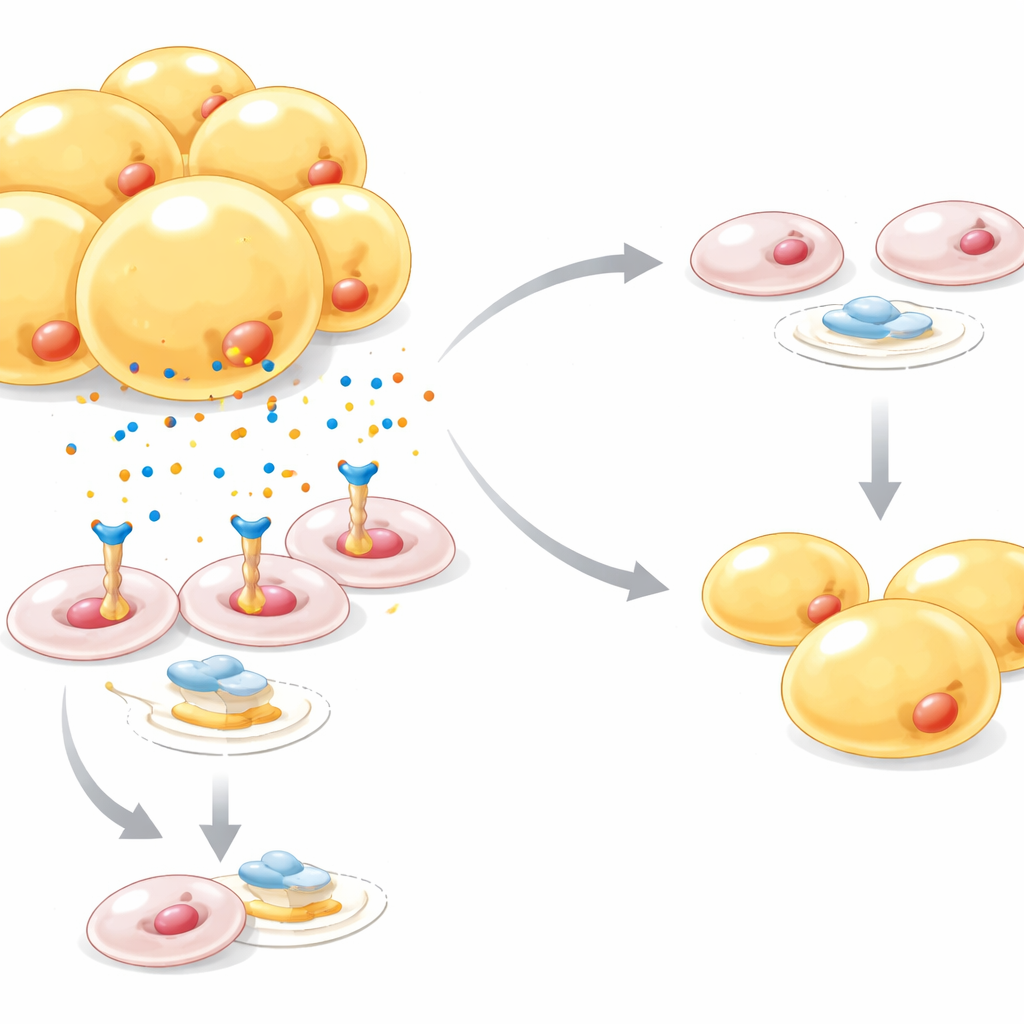
En molekylär broms för att bygga nya fettceller
Närmare granskning visade att Netrin‑1 dämpar en huvudbrytare för fettcellsutveckling kallad PPARγ, samtidigt som den aktiverar en separat signalväg känd som Wnt/β‑catenin, vilken är känd för att motverka fettcellsbildning. I mus‑ och människadatamängder var Netrin‑1‑nivåerna högre vid fetma och typ 2‑diabetes, och koncentrerade i prekursorceller jämfört med mogna fettceller. När Netrin‑1 artificiellt ökades i prekursorceller ackumulerade de färre fettkorn; aktivering av PPARγ med en diabetesläkemedel kunde till stor del rädda denna effekt, och blockering av β‑catenin lättade också Netrin‑1:s broms på fettcellsmognad. En annan kontrollnivå kom från syrebrist i överväxta fettdepåer: hypoxisensorn HIF‑1α ökade direkt Netrin‑1‑genaktivitet och kopplade därmed fettrik-kost‑inducerad syrebrist till denna anti‑adipogena signal.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt antyder detta arbete att när vi överäter försöker vår fettvävnad bilda nya celler för att parkera överskottskalorier säkert. Men vid en fettrik kost slår lokal syrebrist på Netrin‑1, som sedan säger åt närliggande prekursorceller att sluta bli nya fettceller. Resultatet blir att fettlagringen skjuts över i mindre hälsosamma mönster, blodsockret stiger och insulinets effekt försämras. Genom att identifiera Netrin‑1 som en nyckelbudbärare som länkar stressad fettvävnad till dålig metabol hälsa pekar studien på en potentiell ny terapeutisk strategi: att dämpa Netrin‑1, eller dess nedströmsvägar, skulle kunna hjälpa kroppen att expandera ”bra” fettdepåer och bättre buffra mot typ 2‑diabetes, även när kaloriintaget är högt.
Citering: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
Nyckelord: fettvävnad, Netrin-1, typ 2‑diabetes, fettrik kost, PPARγ‑signalering