Clear Sky Science · de
Netrin-1 stört die durch fettreiche Ernährung induzierte Adipogenese über die PPARγ- und Wnt/β-Catenin-Signalwege
Warum das für die alltägliche Gesundheit wichtig ist
Fettleibigkeit und Typ-2-Diabetes werden oft mit „zu viel Fett“ erklärt, doch die Situation ist komplexer: Wie und wo unser Körper überschüssige Kalorien speichert, kann uns schützen oder in Richtung Krankheit treiben. Diese Studie deckt einen überraschenden Akteur in diesem Prozess auf — ein für Nervenleitungsprozesse bekanntes Protein namens Netrin-1, das auch vom Fettgewebe produziert wird. Die Forschenden zeigen, dass Netrin-1 unter fettreicher Ernährung die Fähigkeit des Körpers, Fett auf gesunde Weise umzubauen, sabotieren und dadurch die Blutzuckerregulation verschlechtern kann. Das Verständnis dieser verborgenen Bremse für die „gute“ Fettvermehrung könnte neue Wege zur Behandlung von adipositasbedingtem Diabetes eröffnen.
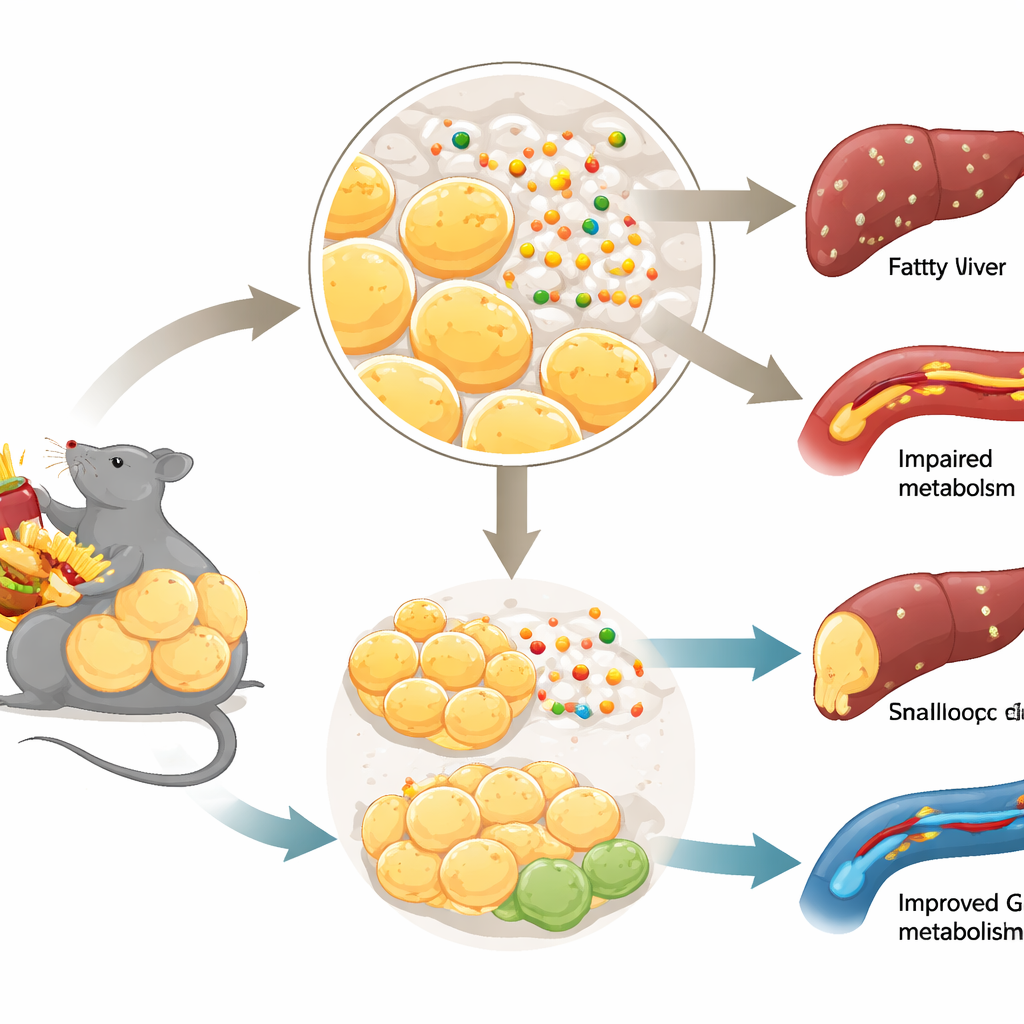
Gutes Fett, schlechtes Fett und Blutzuckerregulation
Nicht jedes Körperfett verhält sich gleich. Wenn überschüssige Kalorien sicher gespeichert werden, indem viele kleine Fettzellen gebildet werden — besonders direkt unter der Haut — kann der Stoffwechsel überraschend gesund bleiben. Im Gegensatz dazu, wenn die Fettspeicherung blockiert ist, werden Fettzellen dysfunktional und Fett verteilt sich in Organe wie Leber und Muskeln. Diese „schlechte“ Umgestaltung steht im Zusammenhang mit Insulinresistenz und Typ-2-Diabetes. Das Team konzentrierte sich darauf, wie neue Fettzellen aus Vorläuferzellen entstehen, ein Prozess, der Adipogenese genannt wird, und fragte, ob Netrin-1, lange bekannt für das Lenken wachsender Nervenfasern, diesen Prozess im Fettgewebe beeinflussen könnte.
Das Abschalten von Netrin-1 macht fettreiche Ernährung weniger schädlich
Um die Rolle von Netrin-1 zu testen, erzeugten die Forschenden Mäuse, denen Netrin-1 spezifisch im Fettgewebe fehlt. Als diese Tiere acht Wochen lang eine fettreiche Ernährung erhielten, nahmen sie tatsächlich mehr Gewicht zu als normale Mäuse — doch ihre Blutzuckerregulation war besser. Sie zeigten verbesserte Insulinantworten, niedrigere Nüchternglukosewerte und reduzierte zirkulierende Fettwerte. Bildgebung und Gewebemessungen ergaben, dass dieses Mehrgewicht hauptsächlich durch eine Vergrößerung des subkutanen weißen Fettes in der Leistengegend verursacht wurde, einem Depot, das oft mit metabolischem Schutz assoziiert ist. Die vergrößerte Fettmasse beruhte nicht auf überfüllten Zellen, sondern auf einer Zunahme der Zellzahl und geringerer Vernarbung, beides Anzeichen für eine gesündere Fettumgestaltung. Auch die Fettansammlung in der Leber war vermindert, was darauf hindeutet, dass das vergrößerte Fettdepot überschüssige Lipide sicher speicherte, die sonst andere Organe geschädigt hätten.
Zu viel Netrin-1 treibt in Richtung Diabetes
Die Wissenschaftler drehten das Experiment um und zwangen das Fettgewebe, mithilfe eines Genlieferungsvirus zusätzliches Netrin-1 zu produzieren. Bei sowohl normal- als auch fettreich ernährten Mäusen veränderte dieses erhöhte Netrin-1 den Körpergewichtsverlauf kaum, verschlechterte jedoch die Glukosetoleranz und erhöhte Blutfettwerte. Fettdepots neigten dazu, im Verhältnis zur Körpergröße zu schrumpfen, während die Leber mehr Fett ansammelte. Zusammen mit Zellkulturversuchen deuten diese Befunde darauf hin, dass Netrin-1 im Fettgewebe wirkt, um die Bildung neuer, funktionaler Fettzellen zu dämpfen. Wenn Netrin-1 erhöht ist, teilen sich Vorläuferzellen weniger und reifen schlechter zu Fettzellen heran, die Lipide effizient speichern und auf Insulin reagieren.
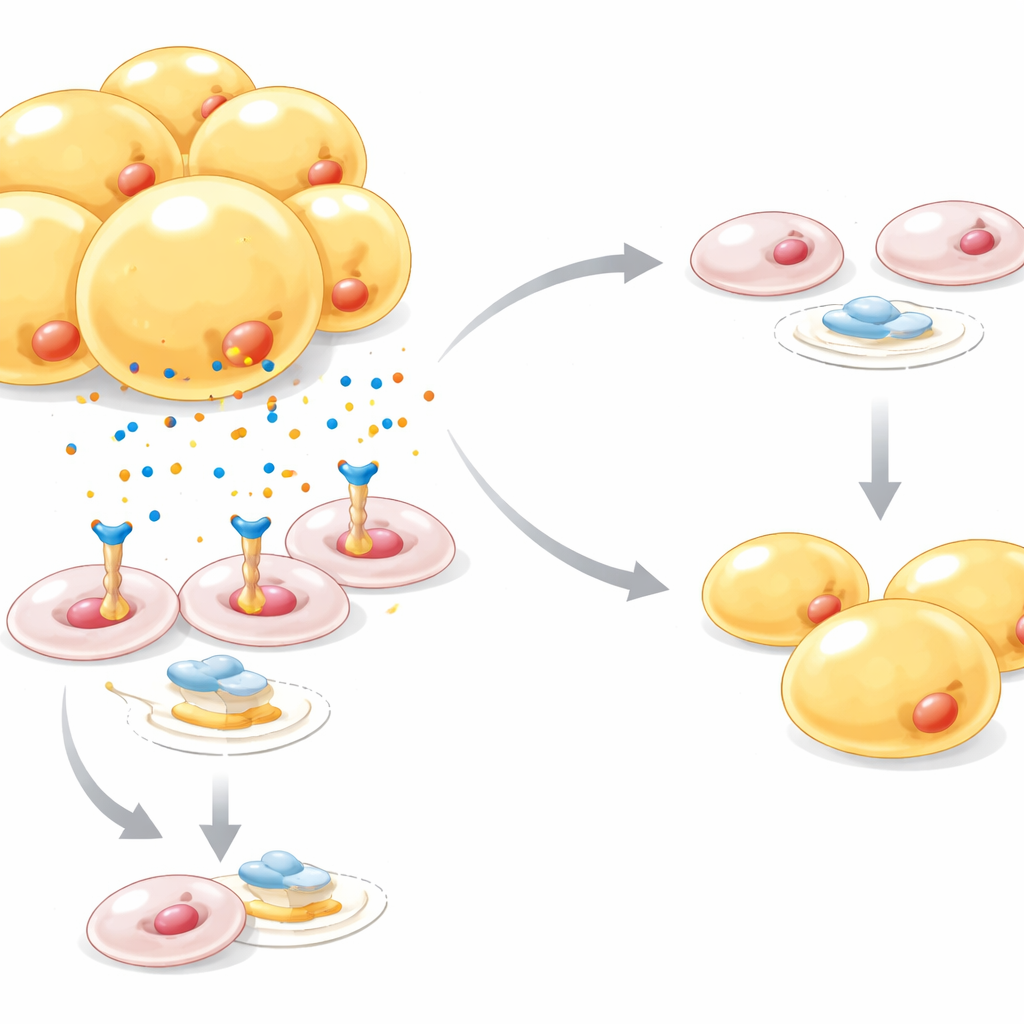
Eine molekulare Bremse beim Aufbau neuer Fettzellen
Bei näherer Untersuchung zeigten die Forschenden, dass Netrin-1 einen Schlüsselschalter der Fettzellentwicklung namens PPARγ dämpft, während es gleichzeitig einen separaten Signalweg aktiviert, bekannt als Wnt/β-Catenin, der die Fettzellbildung zu hemmen pflegt. In Maus- und Menschendatensätzen waren Netrin-1-Spiegel bei Adipositas und Typ-2-Diabetes erhöht und in Vorläuferzellen stärker konzentriert als in ausgereiften Fettzellen. Wenn Netrin-1 künstlich in Vorläuferzellen erhöht wurde, akkumulierten diese weniger Fetttröpfchen; die Aktivierung von PPARγ mit einem Diabetesmedikament konnte diesen Effekt weitgehend rückgängig machen, und das Blockieren von β-Catenin milderte ebenfalls Netrin-1s Bremse auf die Reifung von Fettzellen. Eine weitere Steuerungsebene ergab sich aus Sauerstoffmangelstress innerhalb überwucherter Fettdepots: Der Hypoxie-Sensor HIF‑1α erhöhte direkt die Netrin-1-Genaktivität und verband so die durch fettreiche Ernährung verursachte Sauerstoffknappheit mit diesem anti-adipogenen Signal.
Was das für zukünftige Behandlungen bedeutet
Vereinfacht ausgedrückt legt diese Arbeit nahe, dass unser Fettgewebe beim Überessen versucht, neue Zellen zu bilden, um überschüssige Kalorien sicher zu parken. Unter fettreicher Ernährung schaltet lokaler Sauerstoffstress Netrin-1 an, das dann benachrichtigte Vorläuferzellen daran hindert, zu neuen Fettzellen zu werden. Infolgedessen verschiebt sich die Fettspeicherung in weniger gesunde Muster, der Blutzucker steigt und Insulin wirkt weniger effektiv. Indem die Studie Netrin-1 als wichtigen Boten identifiziert, der gestresstes Fettgewebe mit schlechter metabolischer Gesundheit verbindet, weist sie auf eine mögliche neue therapeutische Strategie hin: Das Herunterregeln von Netrin-1 oder seiner nachgeschalteten Wege könnte dem Körper helfen, „gute“ Fettdepots zu vergrößern und besser gegen Typ-2-Diabetes abzupuffern, selbst bei hoher Kalorienzufuhr.
Zitation: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
Schlüsselwörter: Fettgewebe, Netrin-1, Typ-2-Diabetes, fettreiche Ernährung, PPARγ-Signalgebung