Clear Sky Science · fr
La Nétrine-1 perturbe l’adipogenèse induite par un régime riche en graisses via les voies de signalisation PPARγ et Wnt/β-caténine
Pourquoi cela compte pour la santé au quotidien
L’obésité et le diabète de type 2 sont souvent attribués à « trop de graisse », mais la réalité est plus subtile : la manière et l’endroit où notre corps stocke des calories supplémentaires peuvent soit nous protéger, soit nous pousser vers la maladie. Cette étude met en lumière un acteur surprenant de cette dynamique, une protéine guide des nerfs appelée Nétrine-1 qui est également produite par le tissu adipeux. Les chercheurs montrent que, sous un régime riche en graisses, la Nétrine-1 peut saboter la capacité du corps à remodeler la graisse de façon saine, aggravant ainsi le contrôle de la glycémie. Comprendre ce frein caché à l’expansion de la « bonne » graisse pourrait ouvrir de nouvelles voies pour traiter le diabète lié à l’obésité.
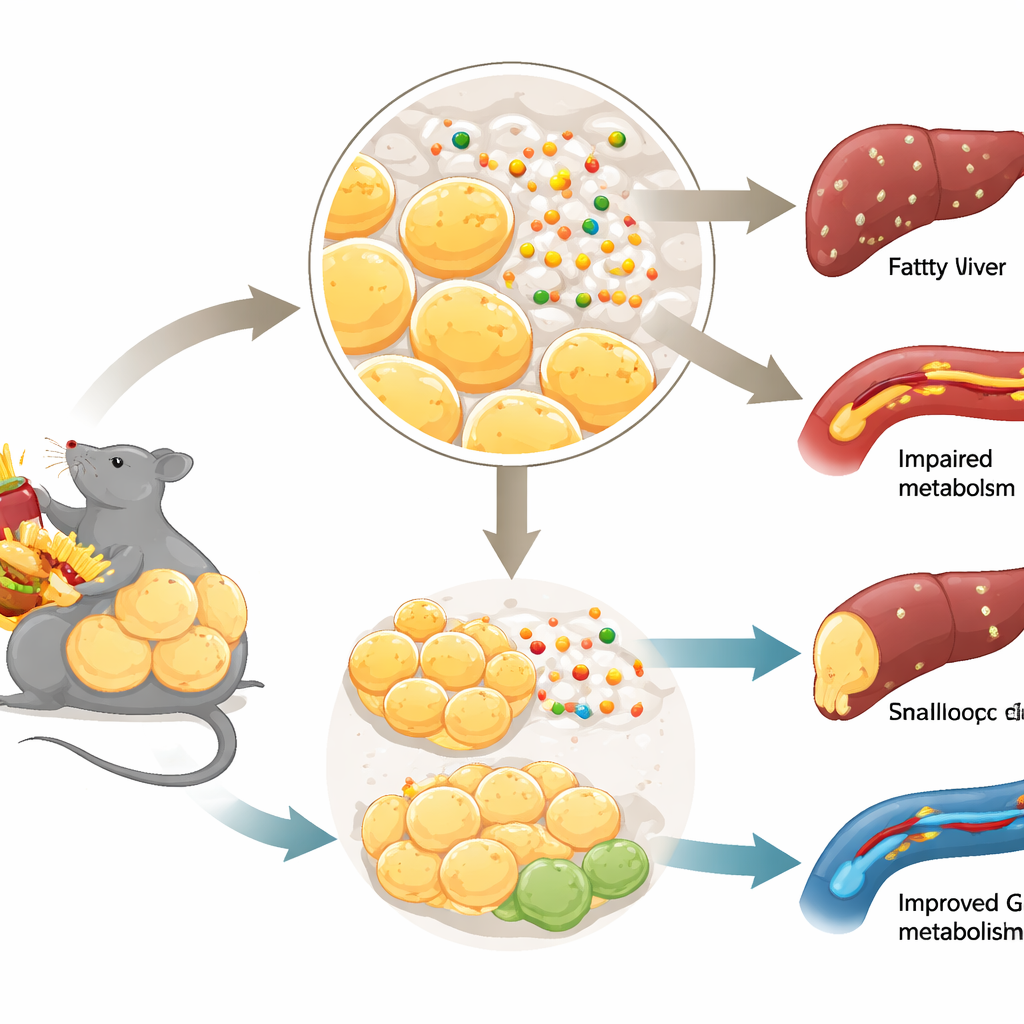
Bonne graisse, mauvaise graisse et contrôle du sucre
Toute la graisse corporelle ne se comporte pas de la même manière. Lorsque les calories excédentaires sont stockées en sécurité en créant de nombreuses petites cellules adipeuses — en particulier sous la peau — le métabolisme peut rester étonnamment sain. En revanche, lorsque le stockage des graisses est entravé, les adipocytes deviennent dysfonctionnels et les lipides se déversent dans des organes comme le foie et les muscles. Ce remodelage « mauvais » est lié à la résistance à l’insuline et au diabète de type 2. L’équipe s’est concentrée sur la formation de nouvelles cellules graisseuses à partir de précurseurs, un processus appelé adipogenèse, et s’est demandé si la Nétrine-1, connue depuis longtemps pour orienter les fibres nerveuses en croissance, pouvait influencer ce processus dans le tissu adipeux.
Éteindre la Nétrine-1 rend les régimes riches en graisses moins nocifs
Pour tester le rôle de la Nétrine-1, les chercheurs ont conçu des souris dépourvues de Nétrine-1 spécifiquement dans le tissu adipeux. Lorsque ces animaux ont été nourris avec un régime riche en graisses pendant huit semaines, ils ont en fait pris plus de poids que les souris normales — mais leur contrôle glycémique était meilleur. Ils présentaient une meilleure réponse à l’insuline, une glycémie à jeun plus basse et des taux de lipides circulants diminués. L’imagerie et les mesures tissulaires ont révélé que ce surpoids provenait principalement de l’expansion de la graisse blanche sous-cutanée près de la région inguinale, un dépôt souvent associé à une protection métabolique. L’augmentation de la masse grasse n’était pas due à des cellules surchargées, mais plutôt à une augmentation du nombre de cellules et à une réduction des cicatrices, deux signes d’un remodelage adipeux plus sain. L’accumulation de graisse dans le foie était également diminuée, ce qui suggère que ce dépôt adipeux élargi stockait en sécurité les lipides excédentaires qui auraient autrement endommagé d’autres organes.
Trop de Nétrine-1 pousse vers le diabète
Les scientifiques ont ensuite inversé l’expérience et forcé le tissu adipeux à produire un excès de Nétrine-1 en utilisant un virus de délivrance génique. Chez les souris normales comme chez celles nourries au régime riche en graisses, cette augmentation de Nétrine-1 n’a pas modifié fortement le poids corporel, mais a aggravé la tolérance au glucose et augmenté les lipides sanguins. Les dépôts adipeux avaient tendance à diminuer par rapport à la taille corporelle, tandis que le foie présentait davantage d’accumulation lipidique. En association avec des expériences en culture cellulaire, ces résultats indiquent que la Nétrine-1 agit au sein du tissu adipeux pour freiner la formation de nouvelles cellules graisseuses fonctionnelles. Lorsque la Nétrine-1 est élevée, les cellules précurseurs se divisent moins et sont moins capables de mûrir en adipocytes capables de stocker efficacement les lipides et de répondre à l’insuline.
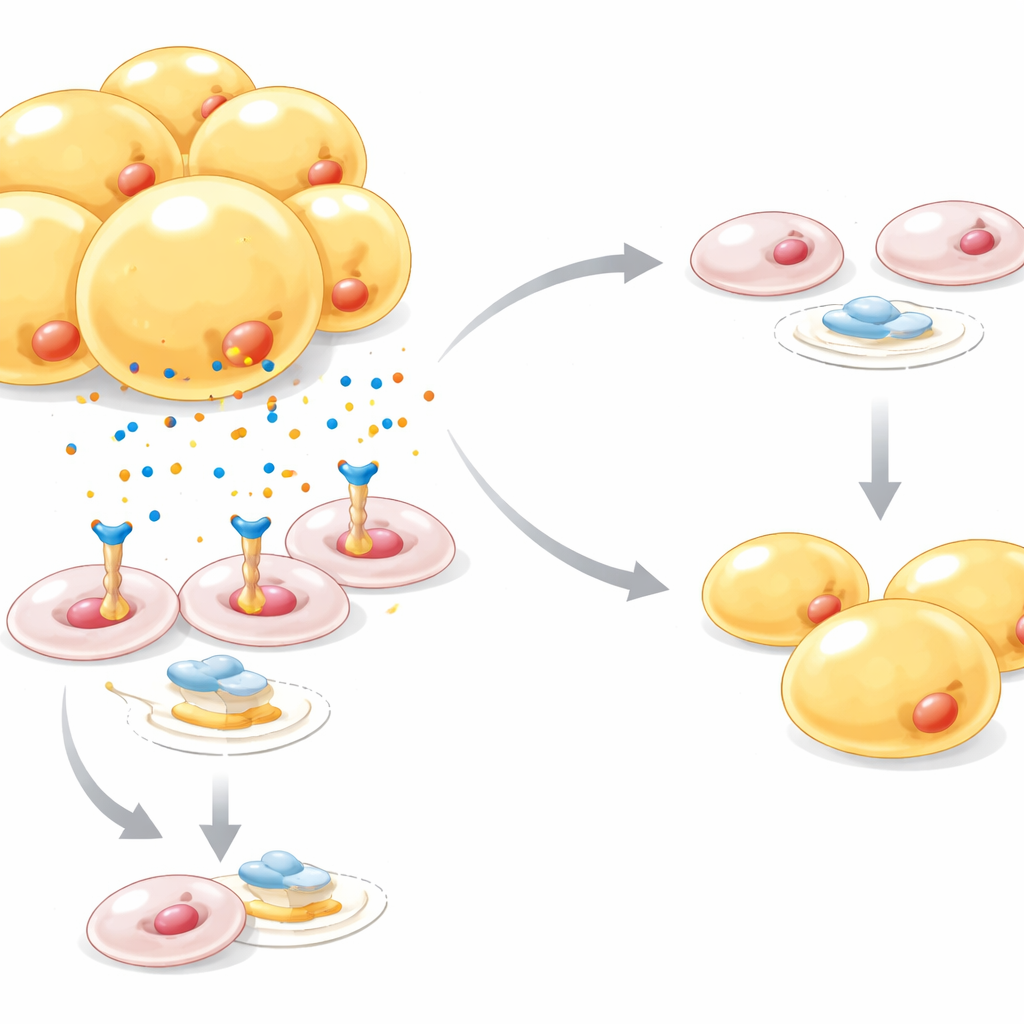
Un frein moléculaire à la création de nouveaux adipocytes
En approfondissant, l’équipe a montré que la Nétrine-1 atténue un commutateur maître du développement des adipocytes appelé PPARγ, tout en activant une voie de signalisation distincte connue sous le nom de Wnt/β-caténine, qui s’oppose à la formation d’adipocytes. Dans des jeux de données de souris et d’humains, les niveaux de Nétrine-1 étaient plus élevés dans l’obésité et le diabète de type 2, et concentrés dans les cellules précurseurs par rapport aux adipocytes matures. Lorsque la Nétrine-1 était artificiellement augmentée dans les cellules précurseurs, elles accumulaient moins de gouttelettes lipidiques ; l’activation de PPARγ avec un médicament antidiabétique pouvait en grande partie sauver cet effet, et le blocage de la β-caténine a également atténué le frein exercé par la Nétrine-1 sur la maturation des adipocytes. Un autre niveau de contrôle provenait du stress hypoxique à l’intérieur des dépôts adipeux hypertrophiés : le senseur d’hypoxie HIF‑1α stimulait directement l’activité du gène Nétrine-1, reliant la pénurie d’oxygène induite par un régime riche en graisses à ce signal anti-adipogénique.
Ce que cela signifie pour les traitements futurs
En termes accessibles, ce travail suggère que lorsque nous mangeons en excès, notre tissu adipeux tente de créer de nouvelles cellules pour stocker les calories supplémentaires en sécurité. Mais sous un régime riche en graisses, le stress local en oxygène active la Nétrine-1, qui dit alors aux cellules précurseurs voisines d’arrêter de devenir de nouvelles cellules graisseuses. En conséquence, le stockage des graisses se fait selon des schémas moins sains, la glycémie augmente et l’insuline agit moins efficacement. En identifiant la Nétrine-1 comme un messager clé reliant le tissu adipeux stressé à une mauvaise santé métabolique, l’étude pointe vers une stratégie thérapeutique potentielle : réduire la Nétrine-1, ou ses voies en aval, pourrait aider le corps à développer des dépôts de « bonne » graisse et mieux protéger contre le diabète de type 2, même lorsque l’apport calorique est élevé.
Citation: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
Mots-clés: tissu adipeux, Nétrine-1, diabète de type 2, régime riche en graisses, signalisation PPARγ