Clear Sky Science · pl
Netrin-1 zakłóca adipogenezę wywołaną dietą wysokotłuszczową poprzez szlaki sygnałowe PPARγ i Wnt/β-katenina
Dlaczego ma to znaczenie dla codziennego zdrowia
Otyłość i cukrzycę typu 2 często sprowadza się do „zbyt dużej ilości tłuszczu”, ale prawda jest bardziej złożona: to, jak i gdzie nasze ciało przechowuje nadmiar kalorii, może nas albo chronić, albo skłaniać w stronę choroby. W tym badaniu odkryto zaskakujący element tej układanki — białko kierujące nerwy, zwane Netrin-1, które jest również wytwarzane przez tkankę tłuszczową. Badacze pokazują, że w warunkach diety wysokotłuszczowej Netrin-1 może sabotować zdolność organizmu do zdrowej przebudowy tłuszczu, pogarszając kontrolę poziomu cukru we krwi. Zrozumienie tego ukrytego hamulca ekspansji „dobrego” tłuszczu może otworzyć nowe drogi leczenia cukrzycy związanej z otyłością.
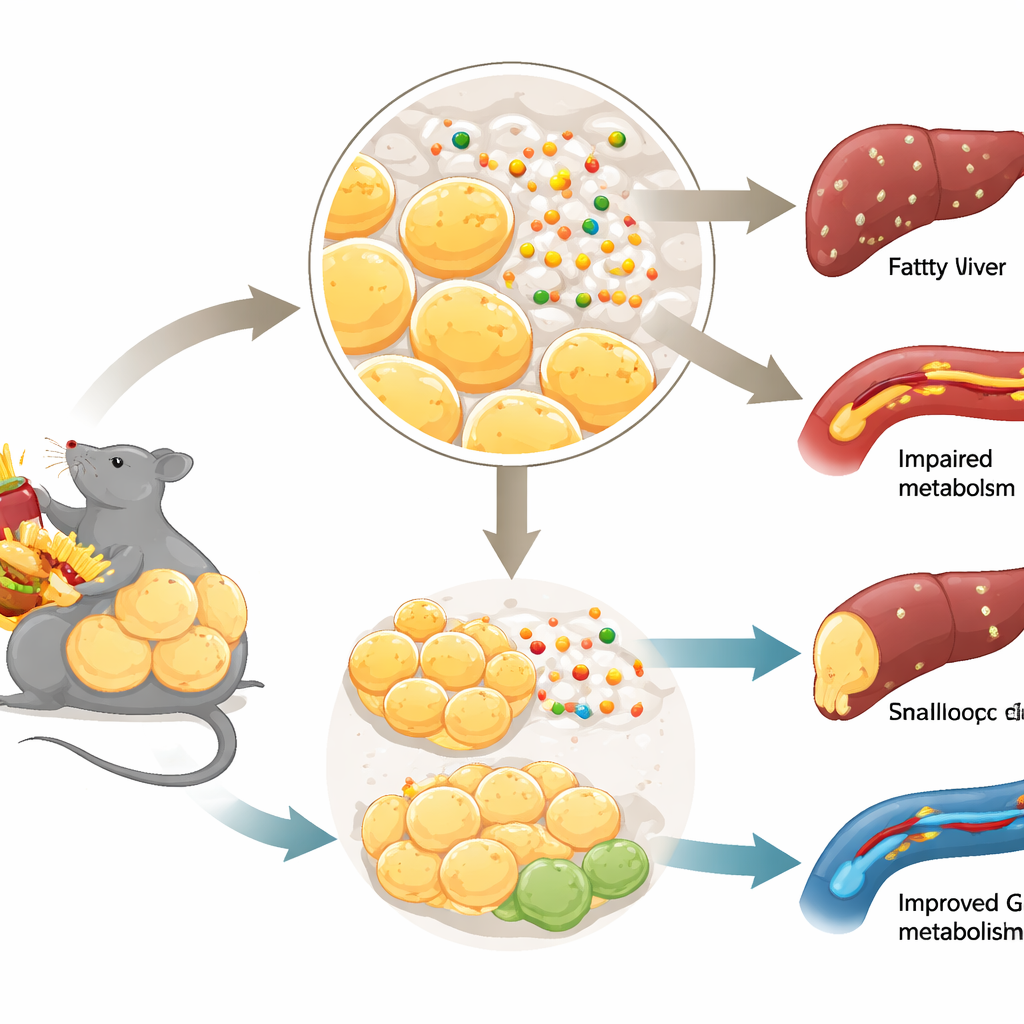
Dobry tłuszcz, zły tłuszcz i kontrola cukru
Nie każdy tłuszcz w organizmie zachowuje się tak samo. Gdy nadmiar kalorii jest bezpiecznie magazynowany przez tworzenie wielu małych komórek tłuszczowych — szczególnie tuż pod skórą — metabolizm może pozostać zaskakująco zdrowy. W przeciwieństwie do tego, gdy magazynowanie tłuszczu jest zablokowane, komórki tłuszczowe ulegają dysfunkcji, a tłuszcz przedostaje się do narządów, takich jak wątroba i mięśnie. Ta „zła” przebudowa wiąże się z insulinoopornością i cukrzycą typu 2. Zespół skupił się na tym, jak powstają nowe komórki tłuszczowe z komórek prekursorowych — proces zwany adipogenezą — i zapytał, czy Netrin-1, znany od dawna z kierowania rozwijającymi się włóknami nerwowymi, może wpływać na ten proces w tkance tłuszczowej.
Wyłączenie Netrin-1 zmniejsza szkodliwy wpływ diety wysokotłuszczowej
Aby przetestować rolę Netrin-1, badacze zmodyfikowali myszy tak, by brakowało im Netrin-1 specyficznie w tkance tłuszczowej. Gdy zwierzęta te były karmione dietą wysokotłuszczową przez osiem tygodni, w rzeczywistości przybrały na wadze więcej niż myszy kontrolne — ale miały lepszą kontrolę glikemii. Wykazywały lepsze odpowiedzi na insulinę, niższe stężenie glukozy na czczo oraz obniżone poziomy krążących tłuszczów. Obrazowanie i pomiary tkanek ujawniły, że dodatkowa masa ciała wynikała głównie z powiększenia podskórnej białej tkanki tłuszczowej w okolicy pachwiny — depozytu często związanego z ochroną metaboliczną. Powiększona masa tłuszczu nie była spowodowana przeładowanymi komórkami, lecz wzrostem ich liczby i zmniejszeniem bliznowacenia, co są oznaki zdrowszej przebudowy tłuszczu. Nagromadzenie tłuszczu w wątrobie także było zmniejszone, co sugeruje, że powiększony depozyt bezpiecznie magazynował nadmiar lipidów, które w przeciwnym razie mogłyby uszkadzać inne narządy.
Zbyt dużo Netrin-1 kieruje w stronę cukrzycy
Naukowcy odwrócili eksperyment i zmusili tkankę tłuszczową do produkcji dodatkowego Netrin-1 przy użyciu wirusa dostarczającego geny. Zarówno u myszy normalnych, jak i karmionych dietą wysokotłuszczową, podwyższony poziom Netrin-1 nie zmienił silnie masy ciała, ale pogorszył tolerancję glukozy i podniósł poziom tłuszczów we krwi. Depozyty tłuszczu miały tendencję do kurczenia się względem masy ciała, podczas gdy wątroba wykazywała większe nagromadzenie tłuszczu. W połączeniu z eksperymentami na hodowlach komórkowych wyniki te wskazują, że Netrin-1 działa w obrębie tkanki tłuszczowej, tłumiąc powstawanie nowych, funkcjonalnych komórek tłuszczowych. Gdy Netrin-1 jest wysoki, komórki prekursorowe dzielą się mniej i trudniej dojrzewają do postaci zdolnej efektywnie magazynować lipidy i reagować na insulinę.
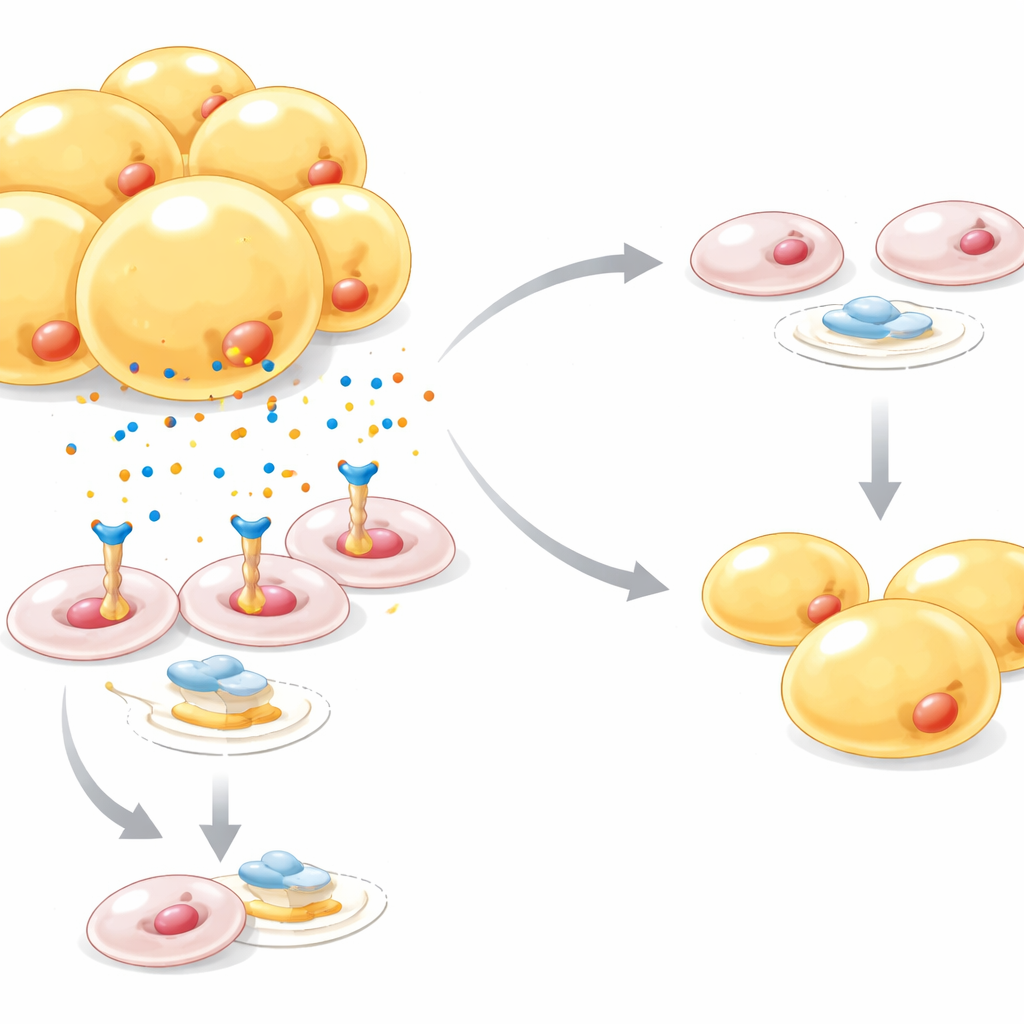
Cząsteczkowy hamulec na budowanie nowych komórek tłuszczowych
Badając mechanizmy, zespół wykazał, że Netrin-1 tłumi główny przełącznik rozwoju komórek tłuszczowych zwany PPARγ, jednocześnie aktywując odrębny szlak sygnałowy znany jako Wnt/β-katenina, który sprzyja hamowaniu adipogenezy. W zbiorach danych mysich i ludzkich poziomy Netrin-1 były wyższe w otyłości i cukrzycy typu 2 oraz skoncentrowane w komórkach prekursorowych w porównaniu z komórkami dojrzałymi. Gdy Netrin-1 sztucznie zwiększano w komórkach prekursorowych, kumulowały one mniej kropelek tłuszczu; aktywacja PPARγ za pomocą leku przeciwcukrzycowego mogła w dużej mierze odwrócić ten efekt, a blokada β-kateniny również złagodziła hamujący wpływ Netrin-1 na dojrzewanie komórek tłuszczowych. Kolejna warstwa kontroli wynikała ze stresu niskotlenowego wewnątrz przerosłych depozytów tłuszczu: sensor hipoksji HIF‑1α bezpośrednio zwiększał aktywność genu Netrin-1, łącząc niedobór tlenu wywołany dietą wysokotłuszczową z tym sygnałem anty-adipogennym.
Co to oznacza dla przyszłych terapii
Mówiąc prostym językiem, praca ta sugeruje, że gdy przejadamy się, nasza tkanka tłuszczowa próbuje wytworzyć nowe komórki, by bezpiecznie przechować nadmiar kalorii. Ale przy diecie wysokotłuszczowej lokalny stres tlenowy włącza Netrin-1, które następnie mówi pobliskim komórkom prekursorowym, by przestały przekształcać się w nowe komórki tłuszczowe. W rezultacie magazynowanie tłuszczu przesuwa się w mniej korzystne wzorce, poziom cukru we krwi rośnie, a działanie insuliny słabnie. Identyfikując Netrin-1 jako kluczowego przekaźnika łączącego zestresowaną tkankę tłuszczową ze złym stanem metabolicznym, badanie wskazuje potencjalną nową strategię terapeutyczną: przyciszenie Netrin-1 lub jego ścieżek efektorowych mogłoby pomóc organizmowi rozbudować „dobre” depozyty tłuszczu i lepiej chronić przed cukrzycą typu 2, nawet przy wysokim spożyciu kalorii.
Cytowanie: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
Słowa kluczowe: tkanka tłuszczowa, Netrin-1, cukrzyca typu 2, dieta wysokotłuszczowa, sygnalizacja PPARγ