Clear Sky Science · nl
Netrin-1 verstoort door vetrijke voeding geïnduceerde adipogenese via de PPARγ- en Wnt/β-catenine-signaleringsroutes
Waarom dit belangrijk is voor alledaagse gezondheid
Obesitas en type 2 diabetes worden vaak toegeschreven aan “te veel vet”, maar het verhaal is genuanceerder: hoe en waar ons lichaam extra calorieën opslaat, kan ons beschermen of juist richting ziekte duwen. Deze studie onthult een onverwachte speler in dat verhaal, een zenuwgeleidingsproteïne genaamd Netrin-1 die ook door vetweefsel wordt gemaakt. De onderzoekers tonen aan dat Netrin-1 bij een vetrijke voeding het vermogen van het lichaam om vet op een gezonde manier te herschikken kan ondermijnen, wat de bloedsuikerregulatie verslechtert. Inzicht in deze verborgen rem op de uitbreiding van “goede” vetmassa kan nieuwe wegen openen voor de behandeling van obesitasgerelateerde diabetes.
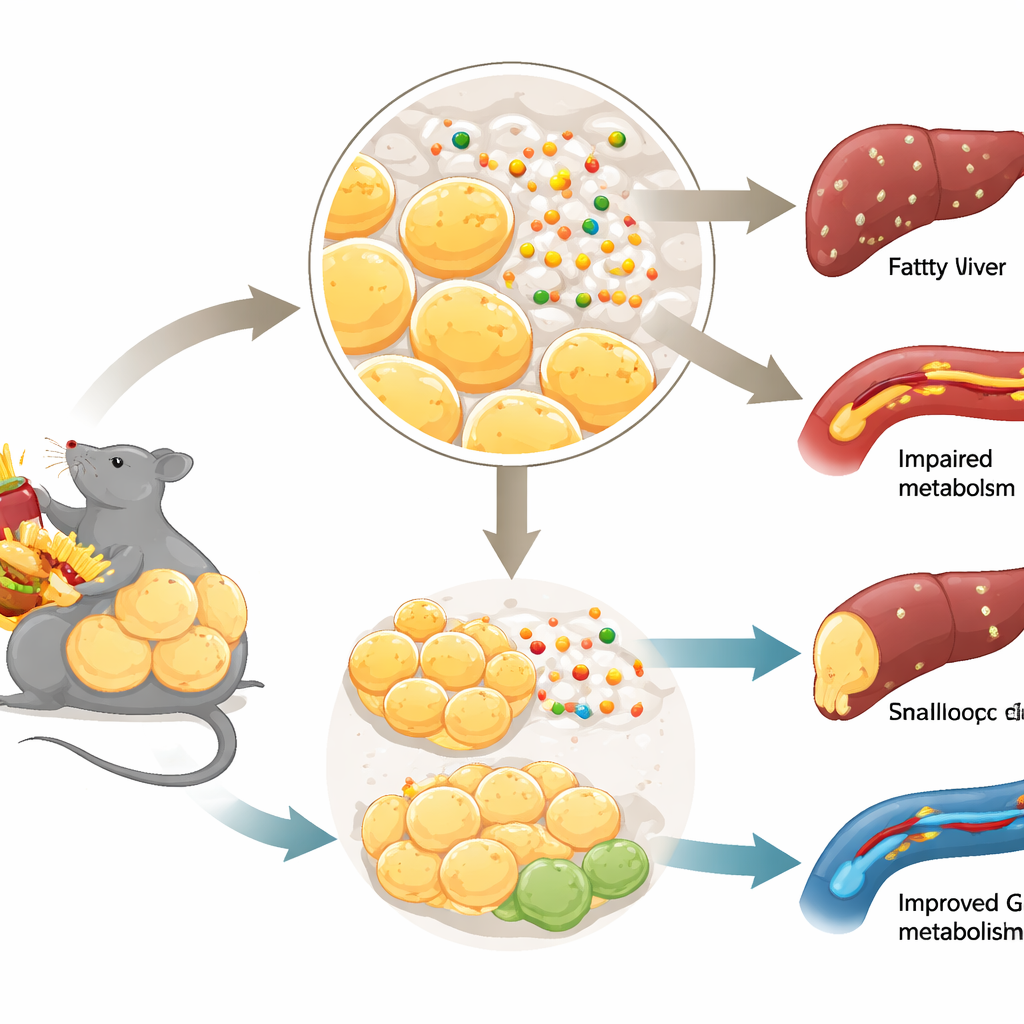
Goed vet, slecht vet en suikermanagement
Niet al het lichaamsvet gedraagt zich hetzelfde. Wanneer overtollige calorieën veilig worden opgeslagen door veel kleine vetcellen te vormen—vooral net onder de huid—kan het metabolisme verrassend gezond blijven. Daarentegen, wanneer vetopslag geblokkeerd raakt, worden vetcellen disfunctioneel en lekt vet naar organen zoals de lever en spieren. Deze “slechte” herschikking hangt samen met insulineresistentie en type 2 diabetes. Het team richtte zich op hoe nieuwe vetcellen ontstaan uit voorlopercellen, een proces dat adipogenese wordt genoemd, en vroeg zich af of Netrin-1, lang bekend om het sturen van groeiende zenuwvezels, dit proces in vetweefsel zou beïnvloeden.
Netrin-1 uitschakelen maakt vetrijke diëten minder schadelijk
Om de rol van Netrin-1 te testen, maakten de onderzoekers muizen die specifiek in vetweefsel geen Netrin-1 meer produceren. Toen deze dieren acht weken een vetrijk dieet kregen, kwamen ze eigenlijk meer aan dan normale muizen—maar hun bloedsuikerregulatie was beter. Ze vertoonden verbeterde insulinegevoeligheid, lagere nuchtere glucosewaarden en verminderde circulerende vetten. Beeldvorming en weefselmetingen lieten zien dat dit extra gewicht voornamelijk het gevolg was van uitbreiding van subcutaan wit vet rond de liesregio, een depot dat vaak met metabole bescherming wordt geassocieerd. De vergrote vetmassa werd niet veroorzaakt door overvolle cellen, maar door een toename in celnummer en verminderde littekenvorming, beide tekenen van gezondere vetherschikking. Vetophoping in de lever nam ook af, wat suggereert dat het vergrote vetdepot overtollige lipiden veilig opsloeg die anders andere organen zouden beschadigen.
Te veel Netrin-1 duwt richting diabetes
De wetenschappers draaiden het experiment om en lieten vetweefsel extra Netrin-1 produceren met behulp van een genleveringsvirus. Bij zowel normaal gevoede als vetrijke-dieetmuizen veranderde dit verhoogde Netrin-1-niveau het lichaamsgewicht niet sterk, maar het verslechterde de glucosetolerantie en verhoogde bloedvetten. Vetdepots leken relatief ten opzichte van het lichaamsgewicht te krimpen, terwijl de lever meer vet ophoopte. Samen met celcultuurexperimenten wijzen deze bevindingen erop dat Netrin-1 binnen vetweefsel de vorming van nieuwe, functionele vetcellen afremt. Wanneer Netrin-1 hoog is, delen voorlopercellen minder en zijn ze minder in staat te rijpen tot vetcellen die efficiënt lipiden opslaan en op insuline reageren.
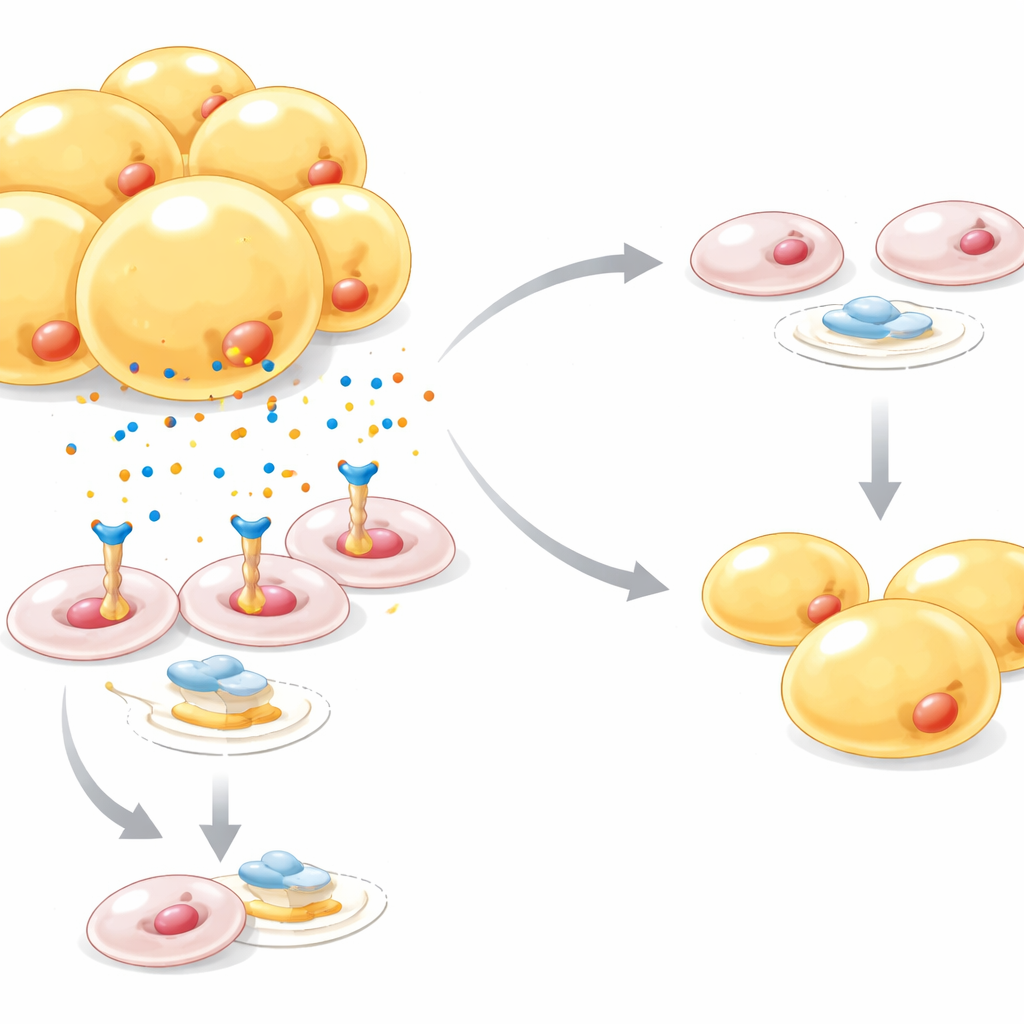
Een moleculaire rem op het bouwen van nieuwe vetcellen
Dieper gravend toonden de onderzoekers aan dat Netrin-1 een hoofdschakelaar voor vetcelontwikkeling, PPARγ, onderdrukt, terwijl het een aparte signaalroute activeert die bekendstaat als Wnt/β-catenine, welke vetcelvorming tegenwerkt. In muis- en humangegevens waren Netrin-1-niveaus hoger bij obesitas en type 2 diabetes, en geconcentreerd in voorlopercellen vergeleken met rijpe vetcellen. Wanneer Netrin-1 kunstmatig verhoogd werd in voorlopercellen, stapelden ze minder vetdruppels op; het activeren van PPARγ met een antidiabeticum kon dit effect grotendeels herstellen, en het blokkeren van β-catenine verlichtte ook Netrin-1’s rem op vetcelrijping. Een andere controlelaag kwam van zuurstofarmoedestress in overgroeide vetdepots: de hypoxiesensor HIF‑1α verhoogde direct de Netrin-1-genactiviteit, waarmee de door vetrijke voeding veroorzaakte zuurstoftekort koppelt aan dit anti-adipogene signaal.
Wat dit betekent voor toekomstige behandelingen
Eenvoudig gesteld suggereert dit werk dat wanneer we te veel eten, ons vetweefsel probeert nieuwe cellen te vormen om extra calorieën veilig te parkeren. Maar bij een vetrijk dieet schakelt lokale zuurstofstress Netrin-1 aan, dat vervolgens nabije voorlopercellen vertelt te stoppen met volwassen worden tot nieuwe vetcellen. Hierdoor verschuift vetopslag naar minder gezonde patronen, stijgt de bloedsuiker en werkt insuline minder effectief. Door Netrin-1 te identificeren als een belangrijke boodschapper die gestrest vetweefsel koppelt aan slechte metabole gezondheid, wijst de studie op een potentiële nieuwe therapeutische strategie: het remmen van Netrin-1, of van zijn downstreamroutes, zou het lichaam kunnen helpen “goede” vetdepots uit te breiden en beter te bufferen tegen type 2 diabetes, zelfs bij hoge calorie-inname.
Bronvermelding: Shi, H., Tang, J., Yan, X. et al. Netrin-1 disrupt high-fat-diet-induced adipogenesis via the PPARγ and Wnt/β-catenin signaling pathways. Commun Biol 9, 471 (2026). https://doi.org/10.1038/s42003-026-09749-x
Trefwoorden: vetweefsel, Netrin-1, type 2 diabetes, vetrijke voeding, PPARγ-signaleringsroute