Clear Sky Science · zh
C16orf87 蛋白是控制胚胎发育和细胞迁移的 MIER 核压制子复合物的一个亚基
为何一个小蛋白对生长与健康至关重要
我们体内的每个细胞都必须处理大量遗传信息,在恰当的时间开启或关闭正确的基因。本文揭示了一种此前神秘的人类蛋白 C16orf87 的功能,研究者建议将其重命名为组蛋白去乙酰化酶相互作用蛋白(HDIP)。他们展示了这种小分子如何帮助控制 DNA 的紧密包装、癌细胞的迁移以及胚胎的发育——将基因基本调控与细胞行为和活体动物的体型联系起来。 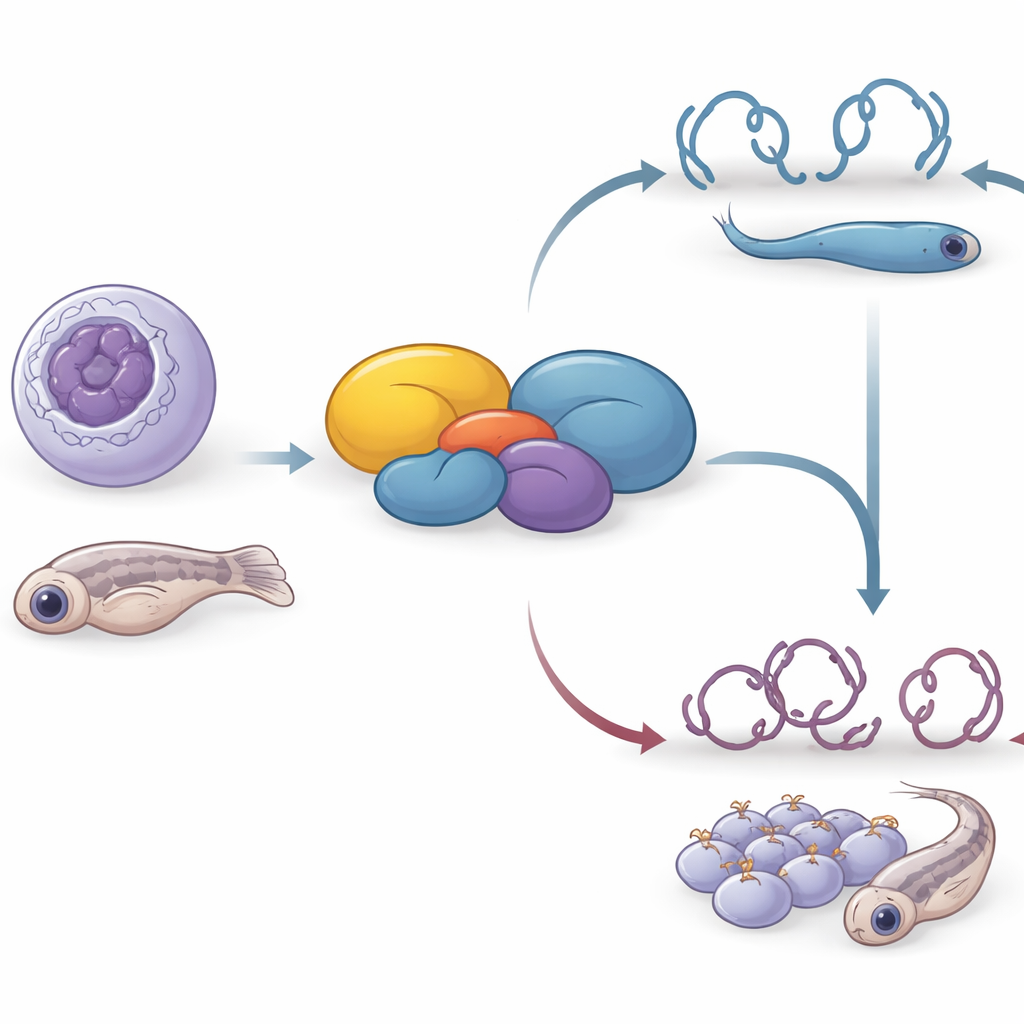
DNA 包装中的隐秘助手
细胞内的 DNA 围绕蛋白质缠绕形成称为染色质的结构,染色质可处于较开放或较致密的状态。这种包装强烈影响基因是处于活跃还是沉默状态。被称为组蛋白去乙酰化酶(HDACs)的酶帮助使染色质变得更紧密从而关闭基因表达。它们很少单独工作,通常位于更大的蛋白“团队”中,称为核压制子复合物。这些复合物的许多成员仍了解甚少。通过结合蛋白化学、结构预测和细胞实验,作者将 C16orf87 识别为其中一个团队——MIER 核压制子复合物——中缺失的一块,该复合物包括关键酶 HDAC1。
HDIP 如何连接基因沉默机器
研究者发现 C16orf87 与 HDAC1、HDAC2 以及作为支架的 MIER1 和 MIER3 蛋白在物理上相互关联,这些支架蛋白帮助将 HDACs 送到特定的 DNA 区域。通过在人类细胞中进行质谱和拉下实验,他们显示 C16orf87 在 MIER 复合物内充当 HDAC1 与 MIER1 之间的连接子。当通过 RNA 干扰降低 C16orf87 水平或用 CRISPR 基因编辑完全去除时,若干组蛋白的水平发生变化,表明该连接子有助于维持 DNA 包装成分的平衡。使用 AlphaFold3 的高级结构预测进一步支持这样一种模型:C16orf87 大部分是柔性的,但利用一段短而结构良好的尾部在 HDAC1 与 MIER1 的中心区域之间对接,稳定它们的结合关系,而不直接改变 HDAC1 的化学活性。 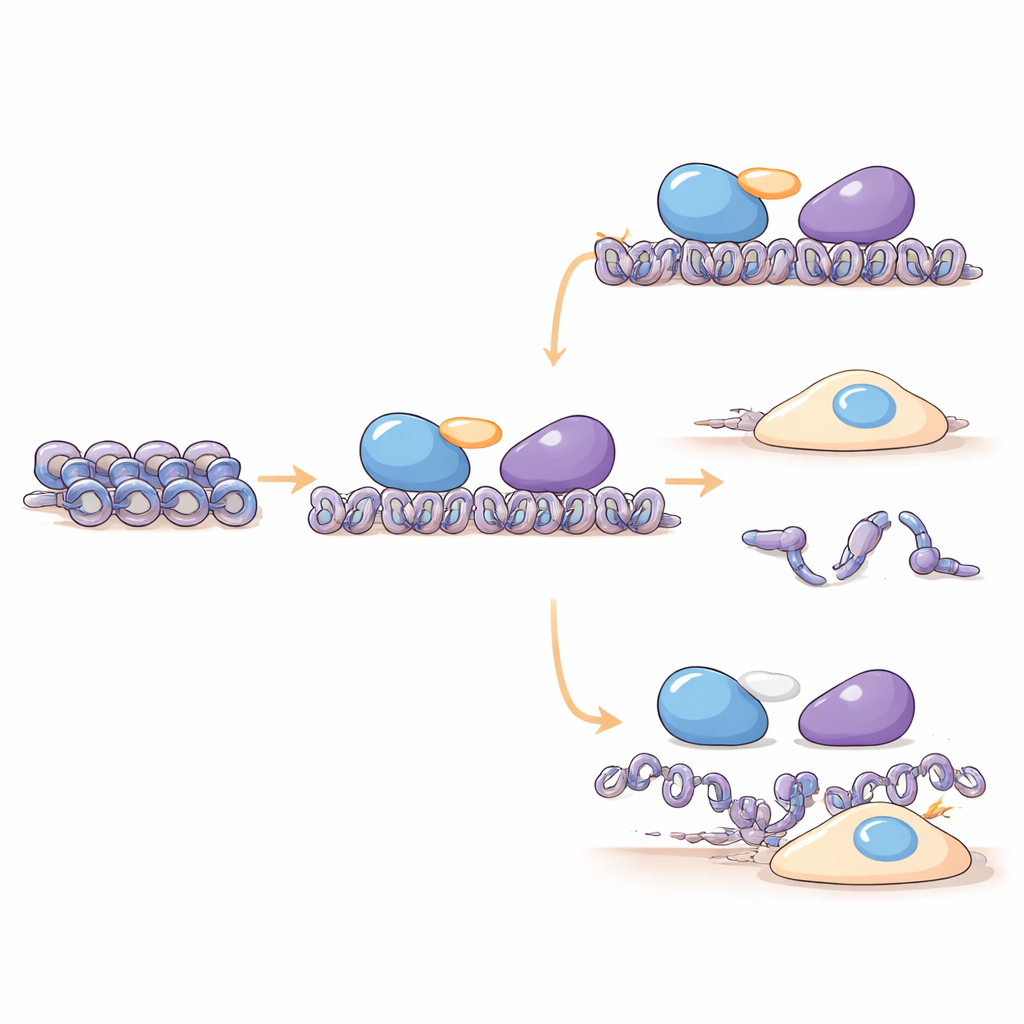
改变连接子就会改变染色质和细胞行为
为了解缺失该连接蛋白会发生什么,团队在一株人胰腺癌细胞系中删除了 C16orf87。被编辑的细胞表现出若干核心组蛋白水平下降,但也许令人惊讶的是,它们仍能存活,甚至 DNA 复制略有加快。然而,当科学家测试这些细胞在平面上迁移的能力——这是伤口愈合和癌症扩散等过程的关键行为时,缺失 C16orf87 的细胞移动明显变慢。基于全基因组的染色质可及性测量(使用 ATAC-seq)显示,缺失 C16orf87 导致许多特定 DNA 区域变得更开放,尤其是在先前已知由 HDAC1/2 和 MIER 蛋白靶向的位置。这些区域中有些位于与细胞信号转导和应激反应相关基因附近,染色质开放性的变化常常伴随基因活性变化。
从培养皿中的细胞到发育中的鱼体
鉴于含 HDAC 的复合物已知可指导早期发育,研究者接着询问同一连接蛋白在整个生物体中是否也重要。他们在胚胎中用 CRISPR 破坏了斑马鱼对应的基因 C7H16orf87。与其同窝兄弟姐妹相比,缺失功能性 C7H16orf87 的幼鱼体长较短、眼睛和体表面积较小,并表现出更弯曲的背部和改变的头身角度。这些缺陷表明该蛋白并非生存所必需,但对发育中个体的正确成形与生长很重要,强化了精细调控染色质在胚胎发生期间不可或缺的观点。
这对未来研究与医学意味着什么
综合来看,这些发现将 C16orf87/HDIP 描绘为一个灵活的适配子,帮助组装特定的基因沉默复合物并将其定向到基因组的特定位点。通过影响哪些 DNA 区域被紧密包装或保持可及,HDIP 塑造了影响人类癌细胞迁移和斑马鱼幼体体形的基因活动模式。因为 HDAC 已是抗癌药物的靶点,理解像 HDIP 这样的辅助伙伴可能为更精确的疗法打开大门,使其仅微调特定基因程式,而不是广泛抑制所有 HDAC 活性。本研究将一个鲜为人知的基因名称转化为功能性故事,把细胞核内的分子连接与有形的生长和运动变化联系了起来。
引用: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
关键词: 染色质调控, 组蛋白去乙酰化酶, 胚胎发育, 细胞迁移, MIER 复合物