Clear Sky Science · ar
بروتين C16orf87 هو وحدة فرعية في مركب الكبت الجيني MIER التي تتحكم في التطور الجنيني وهجرة الخلايا
لماذا يهم بروتين صغير للنمو والصحة
يجب على كل خلية في أجسامنا إدارة كمية هائلة من المعلومات الوراثية، وتفعيل الجينات المناسبة أو إيقافها في الوقت المناسب. تكشف هذه الورقة دور بروتين بشري غامض سابقاً، C16orf87، الذي يقترح الباحثون الآن إعادة تسميته إلى بروتين متفاعل مع HDAC (HDIP). يُظهر الباحثون أن هذه الجزيئة الصغيرة تساعد في التحكم بمدى إحكام تعبئة الحمض النووي لدينا، وبكيفية تحرك خلايا السرطان، وبكيفية تطور الأجنّة — رابطين بين التحكم الجيني الأساسي وسلوك الخلية وشكل الجسم في كائن حي. 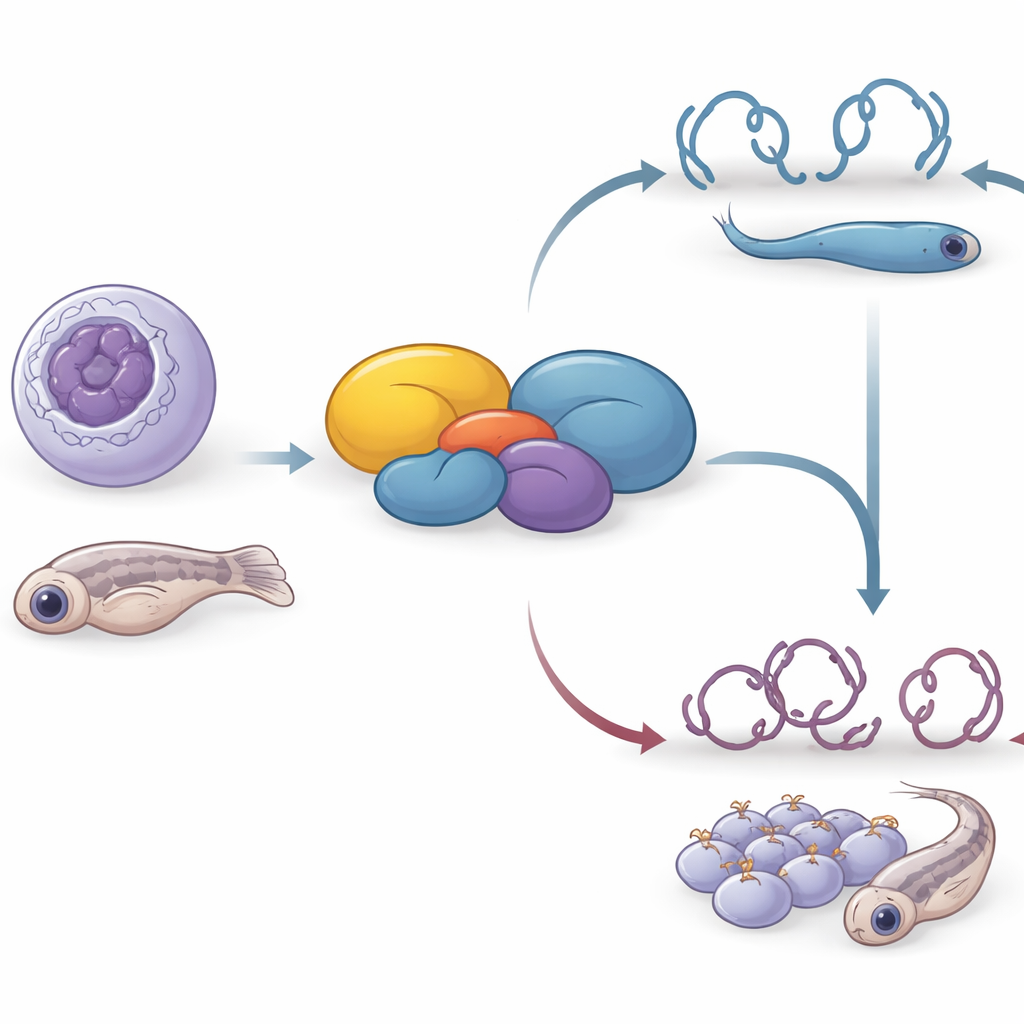
مساعد خفي في تغليف الحمض النووي
الحمض النووي داخل خلايانا ملفوف حول بروتينات ليكوّن بنية تُسمى الكروماتين، التي قد تكون أكثر انفتاحاً أو أكثر انضغاطاً. يؤثر هذا التغليف بقوة على ما إذا كانت الجينات نشطة أم مكتومة. الإنزيمات المعروفة باسم نازعات أسيتلة الهيستون (HDACs) تساعد على تشديد الكروماتين وإيقاف نشاط الجينات. ونادراً ما تعمل هذه الإنزيمات بمفردها؛ بل توجد ضمن فرق بروتينية أكبر تُدعى مركبات الكبت (corepressor complexes). ما زال كثير من أعضاء هذه المركبات غير معروفين جيداً. من خلال الجمع بين كيمياء البروتين، وتنبؤات تركيبية، وتجارب خلوية، يحدد المؤلفون C16orf87 كقطعة مفقودة في أحد هذه الفرق، مركب الكبت MIER، الذي يضم الإنزيم الرئيس HDAC1.
كيف يربط HDIP آلة كبت الجينات
وجد الباحثون أن C16orf87 يرتبط فعلياً بـ HDAC1 وHDAC2، وببروتينات السقالة MIER1 وMIER3 التي تساعد في جلب HDACs إلى مقاطع معينة من الحمض النووي. باستخدام مطيافية الكتلة وتجارب السحب في خلايا بشرية، يوضحون أن C16orf87 يعمل كموصل بين HDAC1 وMIER1 داخل مركب MIER. عندما انخفضت مستويات C16orf87 بواسطة التداخل الحمضي النووي الريبوزي، أو أُزيلت تماماً بتحرير الجينات المعتمد على CRISPR، تغيّرت مستويات عدة بروتينات هيستون، مما يشير إلى أن هذا الموصل يساعد في الحفاظ على التوازن الصحيح لمكونات تغليف الحمض النووي. تدعم تنبؤات التركيب المتقدمة باستخدام AlphaFold3 نموذجاً يكون فيه C16orf87 مرناً في معظم أجزاءه لكنه يستخدم ذيلاً قصيراً ومشكّلاً جيداً ليرسو بين HDAC1 والمنطقة المركزية في MIER1، مثبتاً تعاونهما دون تغيير النشاط الكيميائي لـ HDAC1 بشكل مباشر. 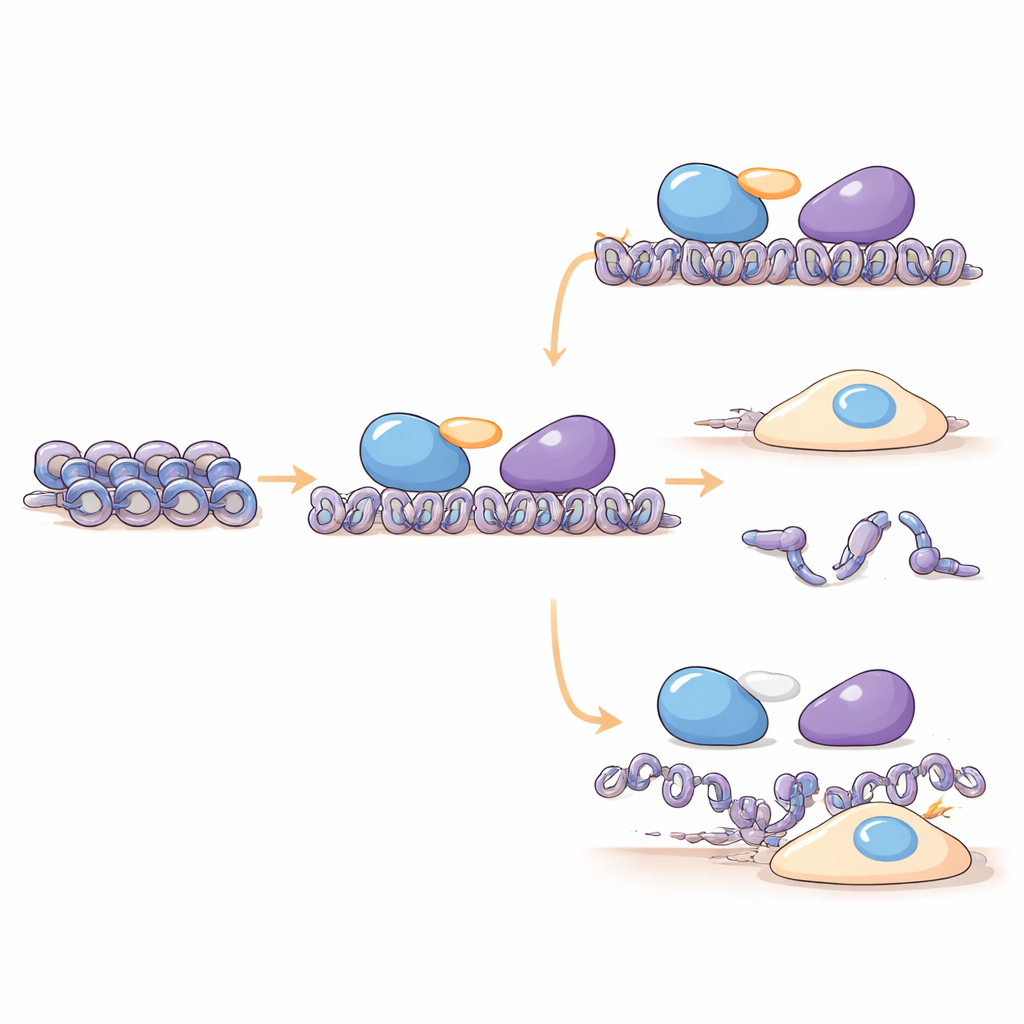
تغيير الموصل يغيّر الكروماتين وسلوك الخلية
لمعرفة ما يحدث عند غياب هذا البروتين الموصل، حذف الفريق C16orf87 في سلالة خلوية بشرية من سرطان البنكرياس. أظهرت الخلايا المعدّلة انخفاض مستويات عدة هيستونات أساسية لكنها، وربما بشكل مفاجئ، بقيت حية وحتى كررت نسخ حمضها النووي بوتيرة أسرع قليلاً. ومع ذلك، عندما اختبر العلماء كيفية هجرة هذه الخلايا عبر سطح — وهو سلوك أساسي لعمليات مثل التئام الجروح وانتشار السرطان — تحركت الخلايا الخالية من C16orf87 ببطء أكبر بشكل ملحوظ. كشفت قياسات إمكانية الوصول إلى الكروماتين عبر الجينوم (باستخدام ATAC-seq) أن فقدان C16orf87 جعل العديد من مناطق الحمض النووي محددة أكثر انفتاحاً، خصوصاً في مواقع كانت معروفة سابقاً بأنها مستهدفة من HDAC1/2 وبروتينات MIER. تقع بعض هذه المناطق بالقرب من جينات تشارك في إشارات الخلية واستجابات الإجهاد، وغالباً ما ترافق التغيرات في انفتاح الكروماتين تغييرات في نشاط الجينات.
من خلايا في طبق إلى أسماك في طور النماء
بما أن المركبات الحاوية على HDAC معروفة بتوجيه التطور المبكر، تساءل الباحثون بعد ذلك ما إذا كان نفس البروتين الموصل مهمّاً في كائن حي كامل. عطلوا النسخة السمكية من الجين، المسماة C7H16orf87، باستخدام CRISPR في الأجنّة. بالمقارنة مع أشقائهم، كان السمك الذي يفتقر إلى C7H16orf87 الوظيفي أقصر قامة، وله عيون ومساحة سطح جسد أصغر، وأظهر ظهراً أكثر تقوساً وزاوية رأس-إلى-جسم معدلة. تكشف هذه العيوب أن البروتين ليس ضرورياً تماماً للبقاء على قيد الحياة لكنه مهم لتشكيل ونمو الجسم بشكل صحيح أثناء التطور، مما يعزز فكرة أن ضبط الكروماتين بدقة ضروري خلال الجنينيّة.
ماذا يعني هذا للبحوث والطب في المستقبل
تجمع النتائج معاً صورة C16orf87/HDIP كمواءم مرن يساعد في تجميع مركب كبت جيني محدد وتوجيهه إلى مواقع مختارة في الجينوم. من خلال التأثير في أي مناطق الحمض النووي تكون محكمة التغليف مقابل أيها متاحة، يشكل HDIP أنماط نشاط الجينات التي تؤثر في هجرة الخلايا في خلايا السرطان البشرية وتكوين الجسم في يرقات السمك. وبما أن HDACs هي حالياً أهداف لأدوية مضادة للسرطان، فقد يفتح فهم شركائها الداعمين مثل HDIP أبواباً لعلاجات أكثر دقة تستهدف برامج جينية معينة بدلاً من حجب كل نشاطات HDAC بشكل واسع. يحول هذا العمل اسماً جينياً غامضاً إلى قصة وظيفية، رابطاً الاتصالات الجزيئية داخل النواة بتغييرات مرئية في كيفية نمو الكائنات وتحركها.
الاستشهاد: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
الكلمات المفتاحية: تنظيم الكروماتين, نزع أسيتلة الهيستون, التطور الجنيني, هجرة الخلايا, مركب MIER