Clear Sky Science · ru
Белок C16orf87 является субъединицей корепрессорного комплекса MIER, контролирующего эмбриональное развитие и миграцию клеток
Почему маленький белок важен для роста и здоровья
Каждая клетка нашего организма должна управлять огромным объёмом генетической информации, включая включение или выключение нужных генов в нужное время. В этой статье раскрыта роль ранее малоизвестного человеческого белка C16orf87, который авторы предлагают переименовать в белок, взаимодействующий с HDAC (HDIP). Исследователи показывают, что эта небольшая молекула помогает контролировать степень упаковывания ДНК, перемещение раковых клеток и развитие эмбриона — связывая базовый регулятор генов с поведением клеток и формированием тела в живом организме. 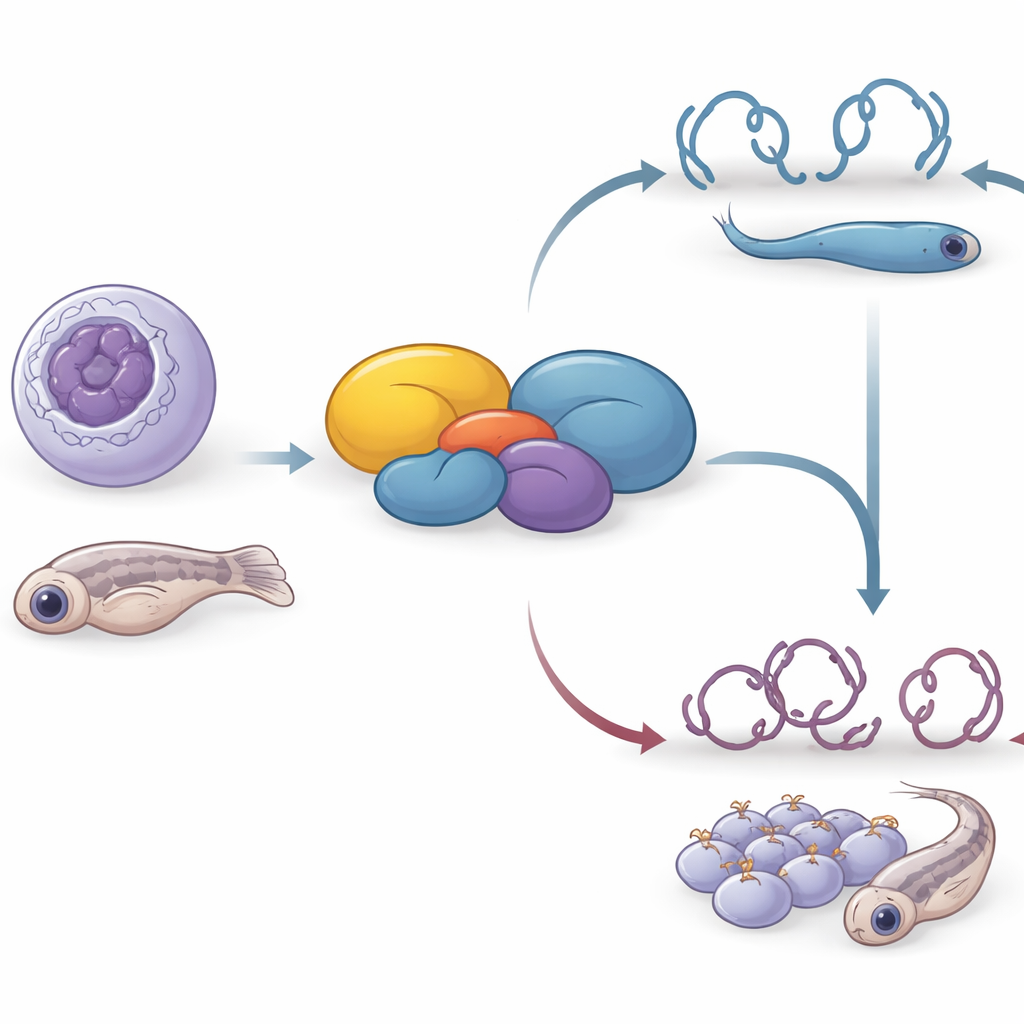
Скрытый помощник в упаковке ДНК
ДНК внутри наших клеток оборачивается вокруг белков, формируя структуру, называемую хроматином, которая может быть более открытой или более компактной. Это упаковывание сильно влияет на то, активен ген или молчит. Ферменты, известные как гистоновые деацетилазы (HDAC), помогают уплотнять хроматин и выключать активность генов. Они редко действуют в одиночку; обычно они входят в состав больших белковых команд — корепрессорных комплексов. Многие члены этих комплексов всё ещё плохо изучены. Объединив методы белковой химии, структурного предсказания и клеточных экспериментов, авторы идентифицируют C16orf87 как недостающий элемент одного из таких комплексов — корепрессора MIER, в состав которого входит ключевой фермент HDAC1.
Как HDIP соединяет машину подавления генов
Исследователи обнаружили, что C16orf87 физически ассоциируется с HDAC1, HDAC2 и каркасными белками MIER1 и MIER3, которые помогают направлять HDAC на определённые участки ДНК. С помощью масс-спектрометрии и экспериментов pull-down в человеческих клетках они показали, что C16orf87 действует как связующее звено между HDAC1 и MIER1 внутри комплекса MIER. При снижении уровней C16orf87 с помощью РНК-интерференции или полном удалении гена методом CRISPR уровни нескольких гистонов изменялись, что указывает на то, что этот коннектор помогает поддерживать правильный баланс компонентов упаковки ДНК. Продвинутые предсказания структуры с AlphaFold3 дополнительно поддерживают модель, в которой C16orf87 в основном гибкий, но использует короткий, хорошо оформленный хвост, чтобы встать между HDAC1 и центральной областью MIER1, стабилизируя их партнёрство без прямого изменения химической активности HDAC1. 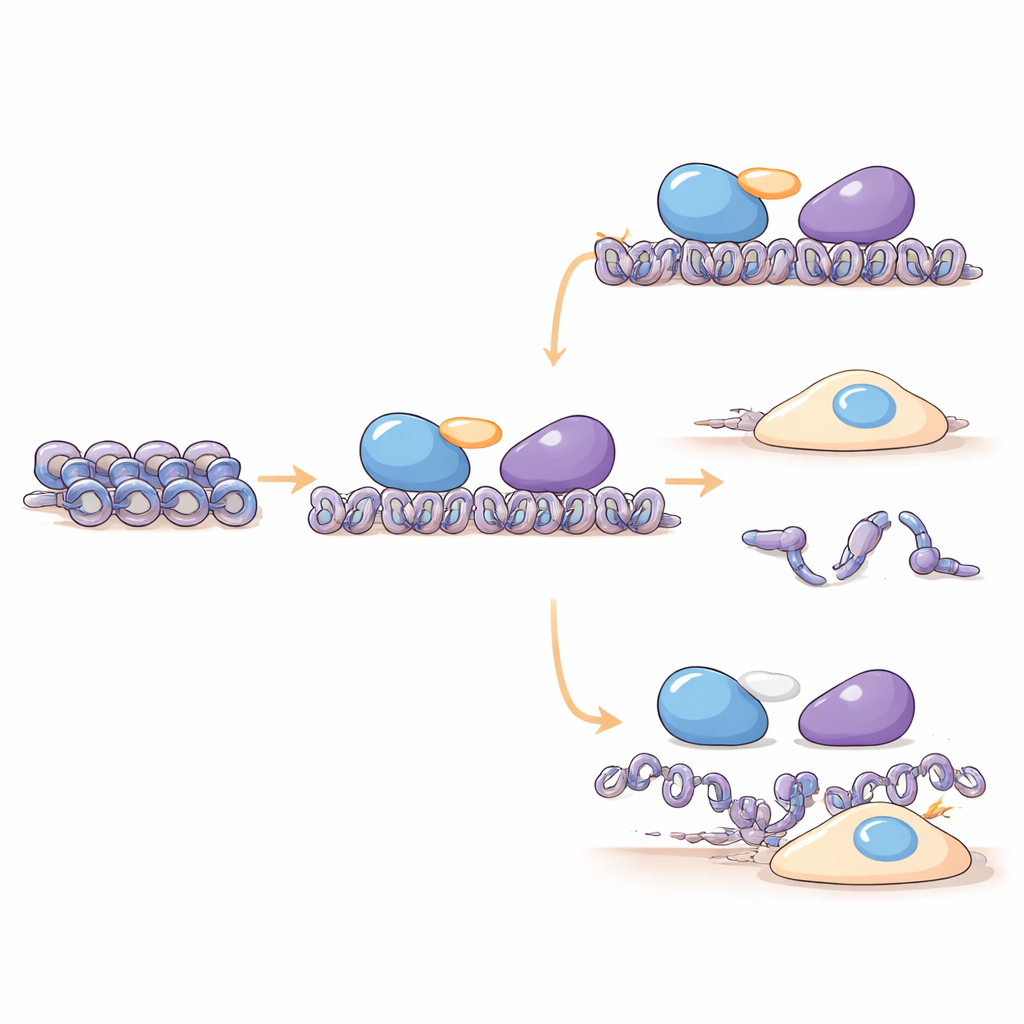
Изменение коннектора меняет хроматин и поведение клеток
Чтобы понять, что происходит при отсутствии этого связующего белка, команда удалила C16orf87 в линии человеческого рака поджелудочной железы. У редактированных клеток наблюдалось снижение уровней нескольких основных гистонов, но, возможно удивительно, они оставались жизнеспособными и даже немного быстрее реплицировали ДНК. Однако при тестировании миграции этих клеток по поверхности — ключевого поведения для таких процессов, как заживление ран и распространение рака — клетки без C16orf87 двигались существенно медленнее. Геномные измерения доступности хроматина (ATAC-seq) показали, что потеря C16orf87 делала многие специфические участки ДНК более открытыми, особенно в сайтах, ранее известных как мишени HDAC1/2 и белков MIER. Некоторые из этих областей расположены рядом с генами, вовлечёнными в клеточную сигнализацию и ответ на стресс, и изменения в открытости хроматина часто сопровождались изменениями активности генов.
От клеток в чашке Петри до развивающейся рыбы
Поскольку комплексы, содержащие HDAC, известны своей ролью в раннем развитии, исследователи проверили, важен ли тот же связующий белок в целом организме. Они нарушили зебрафишевую версию гена, названную C7H16orf87, с помощью CRISPR в эмбрионах. По сравнению с сиблингами, рыбы, лишённые функционального C7H16orf87, были короче, имели меньшие глаза и меньшую площадь поверхности тела, а также демонстрировали более изогнутую спину и изменённый угол головы относительно тела. Эти дефекты показывают, что белок не абсолютно необходим для выживания, но важен для правильного формирования и роста развивающегося тела, что подчеркивает идею о том, что тонкая регуляция хроматина критична во время эмбриогенеза.
Что это значит для будущих исследований и медицины
В совокупности результаты представляют C16orf87/HDIP как гибкий адаптер, который помогает собирать специфический комплекс подавления генов и направлять его в выбранные участки генома. Влияя на то, какие регионы ДНК туго упакованы, а какие доступны, HDIP формирует шаблоны активности генов, которые влияют на миграцию клеток в человеческих раковых клетках и на формирование тела у личинок зебрафиша. Поскольку HDAC уже являются мишенями противораковых препаратов, понимание их вспомогательных партнёров, таких как HDIP, может открыть путь к более точным терапиям, которые будут корректировать лишь определённые генетические программы, вместо широкого блокирования всей активности HDAC. Эта работа превращает малоизвестное название гена в функциональную историю, связывая молекулярные взаимодействия в ядре с видимыми изменениями в росте и поведении организмов.
Цитирование: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
Ключевые слова: регуляция хроматина, гистоновая деацетилаза, эмбриональное развитие, миграция клеток, комплекс MIER