Clear Sky Science · sv
Proteinet C16orf87 är en subenhet i MIER-korrepresorkomplexet som styr embryonal utveckling och cellmigration
Varför ett litet protein spelar roll för tillväxt och hälsa
Varje cell i vår kropp måste hantera en enorm mängd genetisk information och slå på eller av rätt gener vid rätt tidpunkt. Denna artikel avslöjar rollen för ett tidigare mystiskt mänskligt protein, C16orf87, som nu föreslås få namnet HDAC Interacting Protein (HDIP). Forskarna visar att denna lilla molekyl hjälper till att kontrollera hur tätt vårt DNA är packat, hur cancerceller rör sig och hur embryon utvecklas — och länkar grundläggande genreglering till cellbeteende och kroppsform i ett levande djur. 
En dold hjälpare i DNA-packningen
DNA i våra celler är lindat runt proteiner för att bilda en struktur som kallas kromatin, som kan vara mer öppen eller mer kompakt. Denna paketering påverkar starkt om gener är aktiva eller tysta. Enzymer som kallas histondeacetylaser (HDACs) hjälper till att dra ihop kromatinet och stänga av genaktivitet. De arbetar sällan ensamma; istället ingår de i större proteinkomplex kallade korrepresorkomplex. Många medlemmar i dessa komplex är fortfarande dåligt förstådda. Genom att kombinera proteinvetenskap, strukturförutsägelser och cellexperiment identifierar författarna C16orf87 som en saknad pusselbit i ett sådant komplex, MIER-korrepresorkomplexet, som inkluderar den centrala enzymkomponenten HDAC1.
Hur HDIP kopplar samman en genstängande maskin
Forskarna fann att C16orf87 fysiskt associerar med HDAC1, HDAC2 och stommeproteinerna MIER1 och MIER3, vilka hjälper till att föra HDACs till specifika DNA-regioner. Med hjälp av masspektrometri och pull-down-experiment i humana celler visar de att C16orf87 fungerar som en förbindelselänk mellan HDAC1 och MIER1 i MIER-komplexet. När nivåerna av C16orf87 minskades med RNA-interferens, eller togs bort helt med CRISPR-baserad genredigering, förändrades nivåerna av flera histonproteiner, vilket tyder på att denna länk hjälper till att upprätthålla rätt balans av DNA-packningskomponenter. Avancerade strukturförutsägelser med AlphaFold3 stöder vidare en modell där C16orf87 till största delen är flexibel men använder en kort, välordnad svans för att docka mellan HDAC1 och den centrala MIER1-regionen, vilket stabiliserar deras partnerskap utan att direkt ändra HDAC1:s kemiska aktivitet. 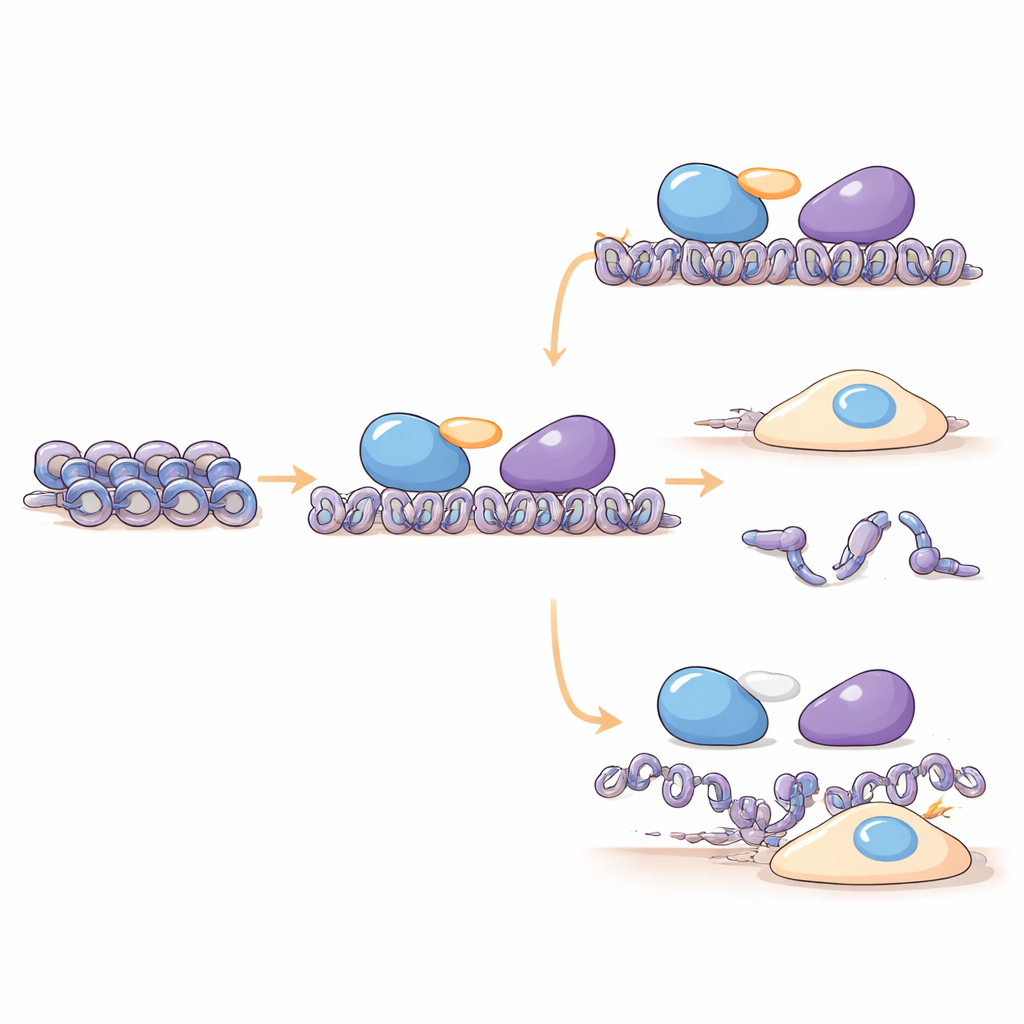
Att förändra förbindelsen förändrar kromatin och cellbeteende
För att se vad som händer när detta kopplingsprotein saknas raderade teamet C16orf87 i en mänsklig pankreascancercellinje. De redigerade cellerna visade minskade nivåer av flera kärnhiston men förblev, kanske förvånande, livsdugliga och replikerade till och med sitt DNA något snabbare. När forskarna testade hur dessa celler migrerade över en yta — ett nyckelbeteende i processer som sårhelande och cancer spridning — rörde sig cellerna utan C16orf87 betydligt långsammare. Genom omfattande mätningar av kromatinåtkomlighet (med ATAC-seq) visade det sig att förlust av C16orf87 gjorde många specifika DNA-regioner mer öppna, särskilt vid platser som tidigare är kända mål för HDAC1/2 och MIER-proteiner. Några av dessa regioner ligger nära gener involverade i cellsignalering och stressresponser, och förändringar i kromatinöppning var ofta förenade med förändringar i genaktivitet.
Från celler i skål till utvecklande fisk
Eftersom komplex som innehåller HDACs är kända för att styra tidig utveckling frågade forskarna nästa om samma kopplingsprotein spelar roll i en hel organism. De störde zebrafiskens version av genen, kallad C7H16orf87, med CRISPR i embryon. Jämfört med sina syskon var fiskar som saknade funktionell C7H16orf87 kortare, hade mindre ögon och kroppsyta samt visade en mer krökt rygg och förändrad huvud-till-kropps-vinkel. Dessa defekter visar att proteinet inte är absolut nödvändigt för överlevnad men är viktigt för korrekt formning och tillväxt under utvecklingen, och förstärker idén att finjusterad kromatinreglering är avgörande under embryogenesen.
Vad detta betyder för framtida forskning och medicin
Sammantaget målar fynden upp C16orf87/HDIP som en flexibel adapter som hjälper till att samla ett specifikt genstängande komplex och styra det till utvalda platser i genomet. Genom att påverka vilka DNA-regioner som är tätt packade kontra åtkomliga formar HDIP mönster av genaktivitet som påverkar cellmigration i mänskliga cancerceller och kroppsutveckling i zebrafisklarver. Eftersom HDACs redan är mål för anticancerläkemedel kan förståelsen av deras stödjande partner som HDIP öppna dörrar för mer precisa terapier som bara finjusterar specifika genprogram istället för att brett blockera all HDAC-aktivitet. Detta arbete förvandlar ett obskyrt gen-namn till en funktionell berättelse som länkar molekylära förbindelser i cellkärnan till synliga förändringar i hur organismer växer och rör sig.
Citering: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
Nyckelord: kromatinreglering, histondeacetylas, embryonal utveckling, cellmigration, MIER-komplexet