Clear Sky Science · fr
La protéine C16orf87 est une sous-unité du complexe corépresseur MIER contrôlant le développement embryonnaire et la migration cellulaire
Pourquoi une petite protéine compte pour la croissance et la santé
Chaque cellule de notre corps doit gérer une quantité énorme d'information génétique, en activant ou désactivant les bons gènes au bon moment. Cet article révèle le rôle d'une protéine humaine jusqu'ici mystérieuse, C16orf87, proposée désormais pour être renommée Protéine Interagissant avec les HDAC (HDIP). Les auteurs montrent que cette petite molécule aide à contrôler le compactage de l'ADN, la migration des cellules cancéreuses et le développement embryonnaire — reliant la régulation génétique de base au comportement cellulaire et à la morphologie corporelle chez un animal vivant. 
Un assistant caché dans l'empaquetage de l'ADN
L'ADN à l'intérieur de nos cellules est enroulé autour de protéines pour former une structure appelée chromatine, qui peut être plus ouverte ou plus compacte. Ce conditionnement influence fortement l'activité ou le silence des gènes. Des enzymes appelées histone désacétylases (HDAC) contribuent à resserrer la chromatine et à éteindre l'expression génique. Elles fonctionnent rarement seules ; elles siègent dans de plus grandes équipes protéiques appelées complexes corépresseurs. De nombreux membres de ces complexes restent mal caractérisés. En combinant chimie des protéines, prédiction structurale et expériences cellulaires, les auteurs identifient C16orf87 comme une pièce manquante d'un de ces ensembles, le complexe corépresseur MIER, qui inclut l'enzyme clé HDAC1.
Comment HDIP relie une machine d'extinction des gènes
Les chercheurs ont constaté que C16orf87 s'associe physiquement à HDAC1, HDAC2 et aux protéines échafaudage MIER1 et MIER3, qui aident à amener les HDAC vers des segments d'ADN spécifiques. Grâce à la spectrométrie de masse et à des expériences d'extraction (pull-down) dans des cellules humaines, ils montrent que C16orf87 agit comme un connecteur entre HDAC1 et MIER1 au sein du complexe MIER. Lorsque les niveaux de C16orf87 ont été réduits par interférence ARN ou supprimés par édition génomique CRISPR, les niveaux de plusieurs histones ont changé, suggérant que ce connecteur aide à maintenir l'équilibre des composants d'empaquetage de l'ADN. Des prédictions structurales avancées avec AlphaFold3 soutiennent en outre un modèle où C16orf87 est majoritairement flexible mais utilise une courte queue bien formée pour s'ancrer entre HDAC1 et la région centrale de MIER1, stabilisant leur association sans modifier directement l'activité chimique de HDAC1. 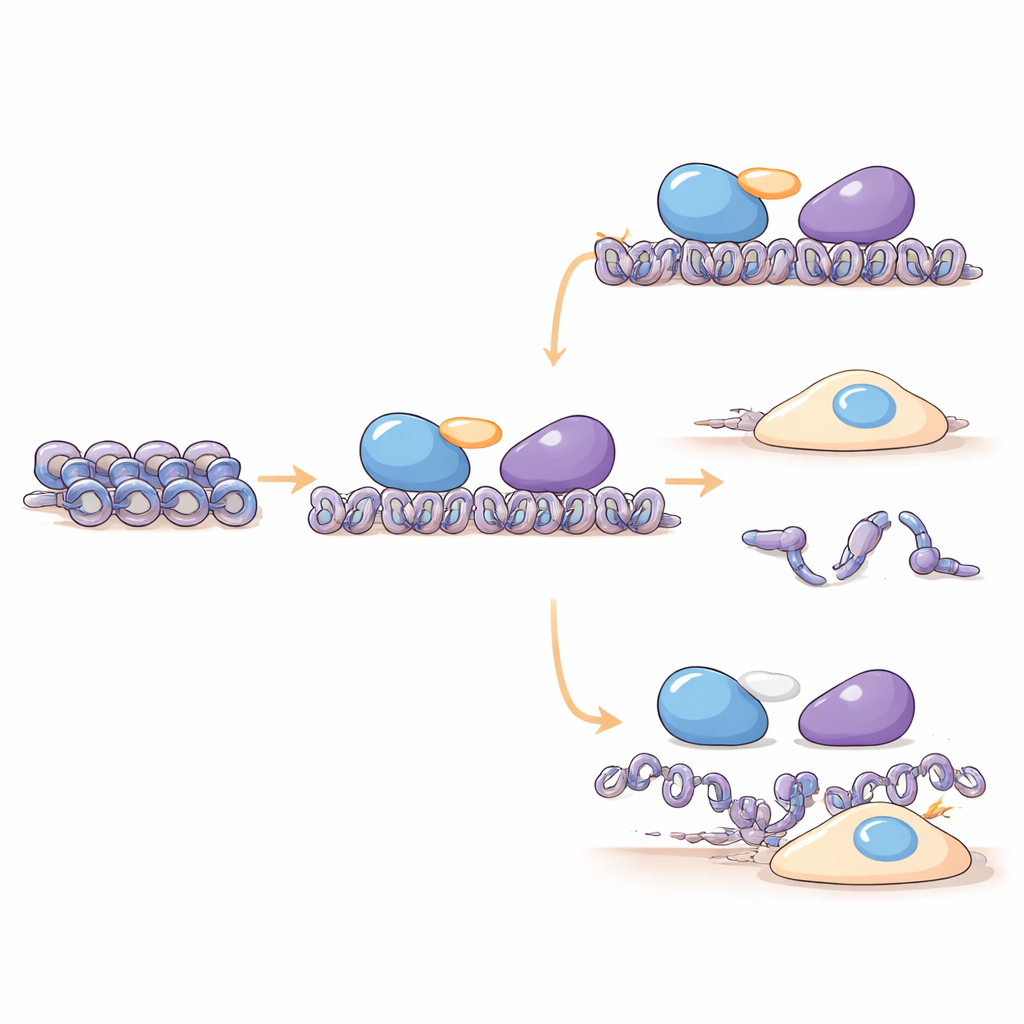
Modifier le connecteur modifie la chromatine et le comportement cellulaire
Pour observer l'effet de l'absence de ce connecteur, l'équipe a supprimé C16orf87 dans une lignée cellulaire humaine de cancer du pancréas. Les cellules éditées présentaient des niveaux réduits de plusieurs histones de base mais, peut-être contre-intuitif, restaient viables et répliquaient même leur ADN un peu plus rapidement. En revanche, lorsqu'ils ont évalué la migration de ces cellules sur une surface — un comportement clé pour des processus comme la cicatrisation et la dissémination tumorale — les cellules dépourvues de C16orf87 se déplaçaient significativement plus lentement. Des mesures génomiques de l'accessibilité de la chromatine (ATAC-seq) ont révélé que la perte de C16orf87 rendait de nombreuses régions d'ADN spécifiques plus accessibles, en particulier à des sites auparavant connus pour être ciblés par HDAC1/2 et les protéines MIER. Certaines de ces régions sont proches de gènes impliqués dans la signalisation cellulaire et la réponse au stress, et les modifications de l'ouverture de la chromatine allaient souvent de pair avec des changements dans l'activité génique.
Des cellules en culture aux poissons en développement
Étant donné que les complexes contenant des HDAC guident le développement précoce, les chercheurs ont ensuite testé si ce même connecteur était important dans un organisme entier. Ils ont perturbé la version zebrafish du gène, nommée C7H16orf87, à l'aide de CRISPR chez des embryons. Par rapport à leurs frères et sœurs, les poissons dépourvus de C7H16orf87 fonctionnel étaient plus courts, avaient des yeux et une surface corporelle plus petits, et présentaient un dos plus courbé ainsi qu'un angle tête-corps modifié. Ces défauts montrent que la protéine n'est pas absolument nécessaire à la survie mais qu'elle est importante pour la morphogenèse et la croissance appropriées du corps en développement, renforçant l'idée qu'un contrôle fin de la chromatine est essentiel lors de l'embryogenèse.
Ce que cela signifie pour la recherche et la médecine
Pris ensemble, ces résultats présentent C16orf87/HDIP comme un adaptateur flexible qui aide à assembler un complexe d'extinction génique spécifique et à le diriger vers des endroits choisis du génome. En influençant quelles régions de l'ADN sont compactées ou accessibles, HDIP façonne des schémas d'expression génique qui affectent la migration cellulaire dans des cellules cancéreuses humaines et la formation corporelle chez les larves de poisson-zèbre. Étant donné que les HDAC sont déjà des cibles de médicaments anticancéreux, comprendre leurs partenaires d'appui comme HDIP pourrait ouvrir la voie à des thérapies plus précises qui moduleraient uniquement des programmes géniques particuliers, plutôt que d'inhiber largement toute l'activité des HDAC. Ce travail transforme un nom de gène obscur en une histoire fonctionnelle, reliant des connexions moléculaires au sein du noyau à des changements visibles dans la croissance et le déplacement des organismes.
Citation: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
Mots-clés: régulation de la chromatine, histone désacétylase, développement embryonnaire, migration cellulaire, complexe MIER