Clear Sky Science · pl
Białko C16orf87 jest podjednostką kompleksu korepresorowego MIER kontrolującego rozwój embrionalny i migrację komórek
Dlaczego małe białko ma znaczenie dla wzrostu i zdrowia
Każda komórka w naszym ciele musi zarządzać ogromną ilością informacji genetycznej, włączając i wyłączając właściwe geny w odpowiednim czasie. Artykuł ten ujawnia rolę dotąd tajemniczego białka ludzkiego, C16orf87, które autorzy proponują nazwać białkiem interagującym z HDAC (HDIP). Badacze pokazują, że ta niewielka cząsteczka pomaga kontrolować stopień upakowania DNA, wpływać na ruchliwość komórek nowotworowych oraz na rozwój embrionów — łącząc podstawową regulację genów z zachowaniem komórek i kształtem ciała u żywego organizmu. 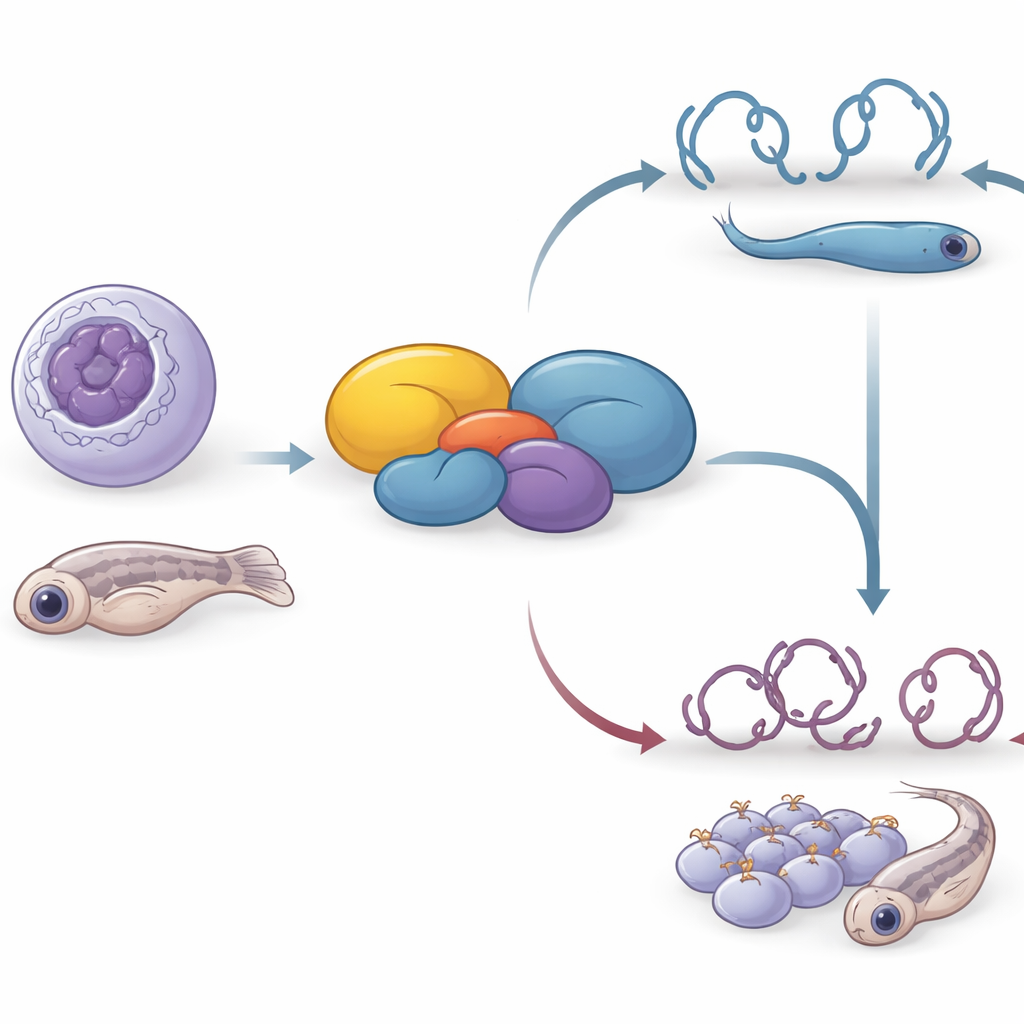
Ukryty pomocnik w pakowaniu DNA
DNA w naszych komórkach jest nawinięty wokół białek, tworząc strukturę zwaną chromatyną, która może być bardziej otwarta lub bardziej zwarta. To upakowanie silnie wpływa na to, czy geny są aktywne czy uśpione. Enzymy znane jako deacetylazy histonowe (HDAC) pomagają zagęszczać chromatynę i wyciszać aktywność genów. Rzadko działają samodzielnie; zwykle wchodzą w skład większych zespołów białkowych zwanych kompleksami korepresorowymi. Wiele składników tych kompleksów jest wciąż słabo poznanych. Łącząc chemię białek, przewidywanie struktur i eksperymenty komórkowe, autorzy identyfikują C16orf87 jako brakujące ogniwo jednego z takich zespołów — kompleksu korepresorowego MIER, w skład którego wchodzi kluczowa deacetylaza HDAC1.
Jak HDIP łączy maszynę wyciszającą geny
Badacze wykazali, że C16orf87 fizycznie kojarzy się z HDAC1, HDAC2 oraz z białkami rusztowania MIER1 i MIER3, które pomagają rekrutować HDACy do określonych odcinków DNA. Przy użyciu spektrometrii mas i eksperymentów pull-down w komórkach ludzkich pokazują, że C16orf87 działa jako łącznik między HDAC1 a MIER1 w kompleksie MIER. Gdy poziomy C16orf87 były obniżone przez interferencję RNA lub całkowicie usunięte przy użyciu edycji genów metodą CRISPR, zmieniały się poziomy kilku białek histonowych, co sugeruje, że ten łącznik pomaga utrzymać właściwą równowagę składników upakowujących DNA. Zaawansowane przewidywania strukturalne z AlphaFold3 dodatkowo wspierają model, w którym C16orf87 jest w większości elastyczny, ale wykorzystuje krótką, dobrze ukształtowaną końcówkę do wpięcia się między HDAC1 a centralny region MIER1, stabilizując ich współpracę bez bezpośredniej zmiany chemicznej aktywności HDAC1. 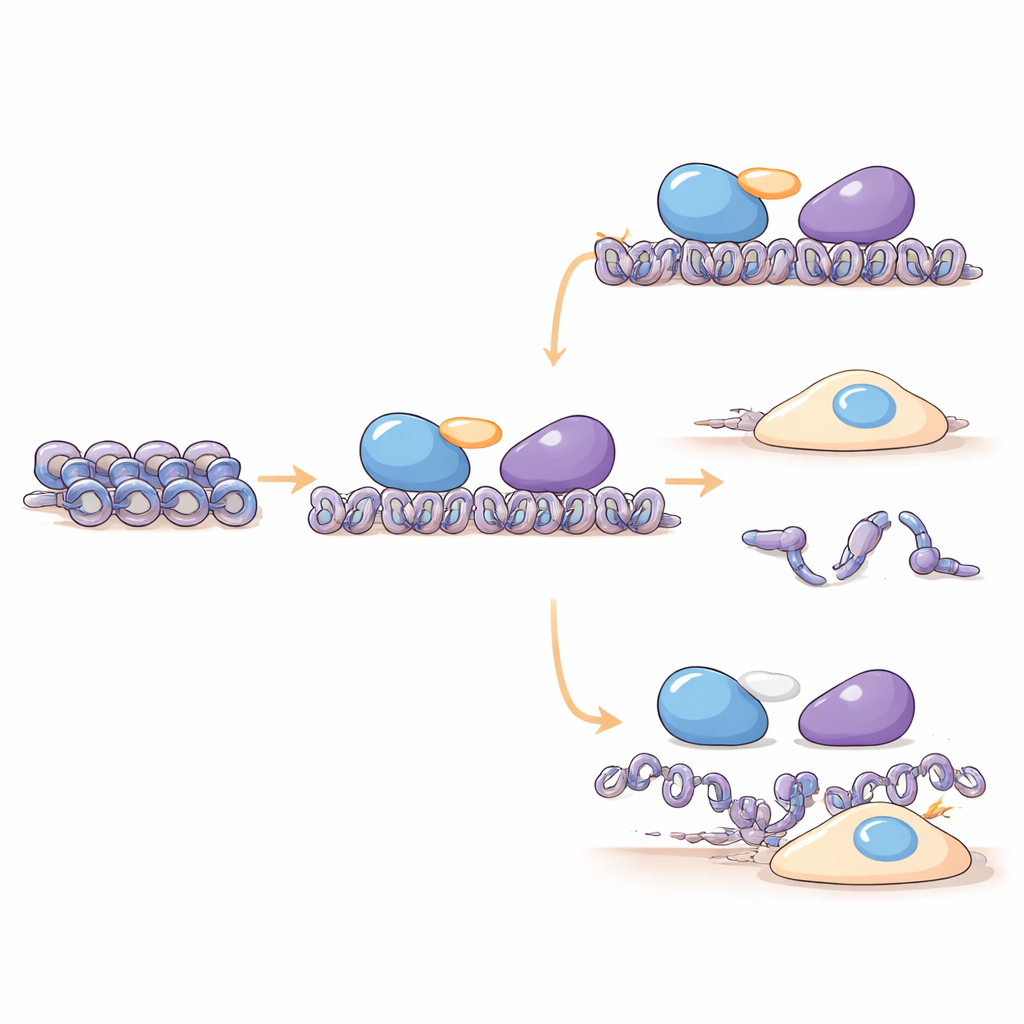
Zmiana łącznika zmienia chromatynę i zachowanie komórek
Aby sprawdzić, co się dzieje, gdy ten łącznik białkowy zniknie, zespół usunął C16orf87 w ludzkiej linii komórkowej raka trzustki. Edytowane komórki wykazywały obniżone poziomy kilku podstawowych histonów, ale, co może zaskakiwać, pozostawały żywotne i nawet nieco szybciej replikujeły DNA. Jednak gdy naukowcy sprawdzili, jak te komórki poruszają się po powierzchni — kluczowe zachowanie w procesach takich jak gojenie ran i rozprzestrzenianie się nowotworów — komórki pozbawione C16orf87 poruszały się istotnie wolniej. Pomiar dostępności chromatyny w skali całego genomu (przy użyciu ATAC-seq) wykazał, że utrata C16orf87 powoduje, iż wiele specyficznych regionów DNA staje się bardziej otwartych, szczególnie w miejscach wcześniej znanych jako cele HDAC1/2 i białek MIER. Niektóre z tych regionów leżą blisko genów zaangażowanych w sygnalizację komórkową i reakcje na stres, a zmiany w otwartości chromatyny często współwystępowały ze zmianami w aktywności genów.
Od komórek na szalce do rozwijających się ryb
Ponieważ kompleksy zawierające HDAC są znane z kierowania wczesnym rozwojem, badacze zapytali następnie, czy ten sam łącznik białkowy ma znaczenie w całym organizmie. Uszkodzili w zygotach wersję genu u zebrafish, zwaną C7H16orf87, używając CRISPR. W porównaniu do rodzeństwa, ryby pozbawione funkcjonalnego C7H16orf87 były krótsze, miały mniejsze oczy i powierzchnię ciała oraz wykazywały bardziej zaokrąglone grzbiety i zmieniony kąt głowy względem tułowia. Te wady ujawniają, że białko nie jest absolutnie niezbędne do przeżycia, ale jest ważne dla prawidłowego kształtowania i wzrostu rozwijającego się ciała, co wzmacnia ideę, że precyzyjna kontrola chromatyny jest kluczowa podczas embriogenezy.
Co to znaczy dla przyszłych badań i medycyny
W podsumowaniu wyniki ukazują C16orf87/HDIP jako elastyczny adaptor, który pomaga składać specyficzny kompleks wyciszający geny i kierować go do wybranych miejsc w genomie. Poprzez wpływ na to, które regiony DNA są silnie upakowane, a które dostępne, HDIP kształtuje wzorce aktywności genów, które wpływają na migrację komórek w ludzkich komórkach nowotworowych oraz na formowanie ciała u larw zebrafish. Ponieważ HDACy są już celami leków przeciwnowotworowych, zrozumienie ich wspierających partnerów, takich jak HDIP, może otworzyć drogę do bardziej precyzyjnych terapii, które modyfikują jedynie wybrane programy genowe, zamiast szeroko blokować całą aktywność HDAC. Ta praca zmienia niejasną nazwę genu w funkcjonalną historię, łącząc molekularne połączenia wewnątrz jądra z widocznymi zmianami w tym, jak organizmy rosną i się poruszają.
Cytowanie: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
Słowa kluczowe: regulacja chromatyny, deacetylaza histonowa, rozwój embrionalny, migracja komórek, kompleks MIER