Clear Sky Science · he
חלבון C16orf87 הוא תת-יחידה של קומפלקס המדכא הליבה MIER ששולט בהתפתחות העוברית ובהגירת תאים
מדוע חלבון קטן חשוב לצמיחה ולבריאות
כל תא בגופנו צריך לנהל כמות עצומה של מידע גנטי, ולהדליק או לכבות את הגנים המתאימים בזמנים הנכונים. מאמר זה חושף את תפקידו של חלבון אנושי שהיה קודם לכן מסתורי, C16orf87, שמוצע כעת לקרוא לו חלבון המתווך עם HDAC (HDIP). החוקרים מראים שהמולקולה הקטנה הזאת מסייעת לשלוט בעובי דחיסת ה-DNA שלנו, בתנועת תאי סרטן ובהתפתחות עוברית — וקושרת בין בקרה גנטית בסיסית להתנהגות התא וצורת הגוף בעובד חי. 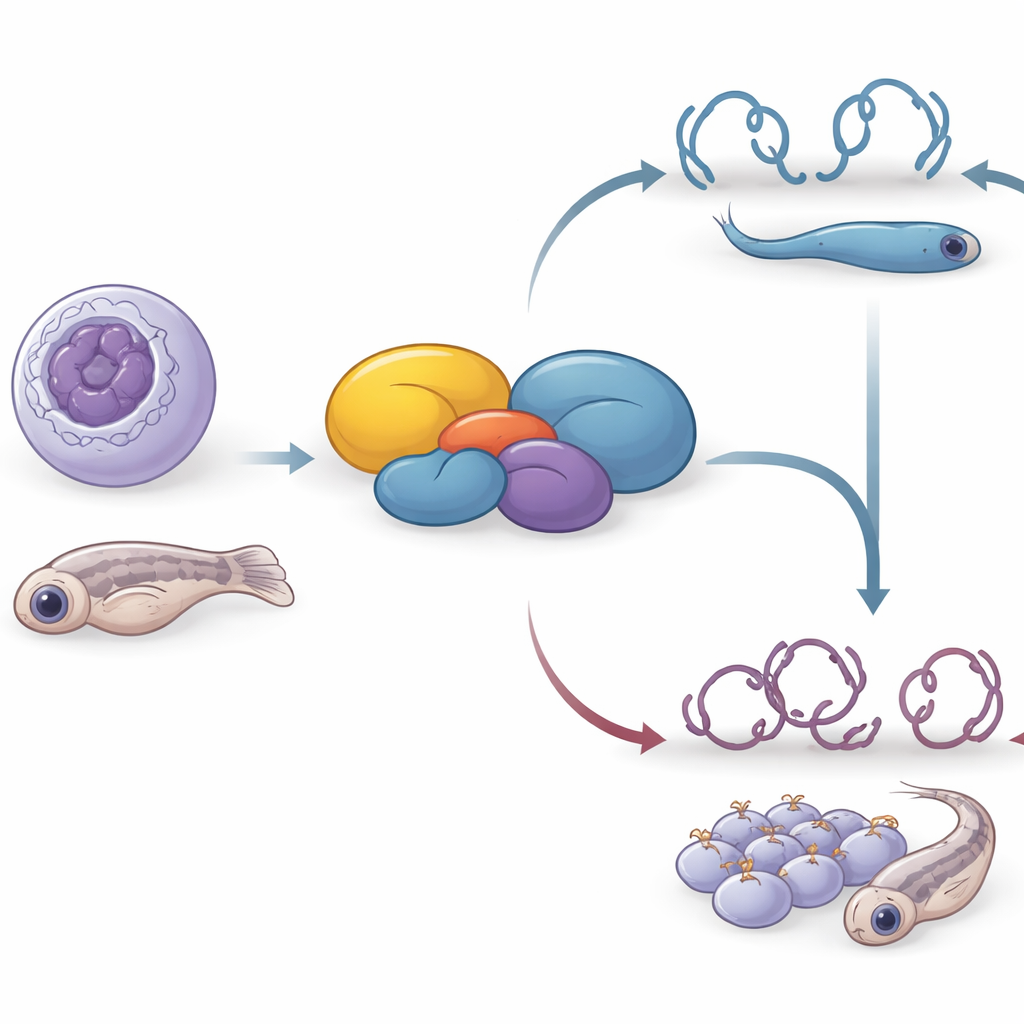
עוזר חבוי באריזת ה-DNA
ה-DNA בתאים שלנו כרוך סביב חלבונים ליצירת מבנה שנקרא כרומטין, שיכול להיות פתוח יותר או דחוס יותר. דחיסה זו משפיעה בחוזקה על האם גנים פעילים או מדוכאים. אנזימים שכונו היסטון דאצילאזים (HDACs) מסייעים להדק את הכרומטין ולכבות פעילות של גנים. הם נדירים כוחות עצמאיים; במקום זאת הם יושבים בתוך צוותי חלבונים גדולים יותר שנקראים קומפלקסי מדכא ליבה. רבים מחברי קומפלקסים אלה עדיין לא מובנים היטב. על ידי שילוב של כימיה חלבונית, חיזוי מבני וניסויים בתאים, המחברים מזהים את C16orf87 כחתיכה חסרה של אחד הקומפלקסים האלה — קומפלקס MIER — הכולל את האנזים המרכזי HDAC1.
כיצד HDIP מקשר מכונת הדיכוי של גנים
החוקרים מצאו ש-C16orf87 קשור פיזית ל-HDAC1, HDAC2 ולחלבוני השלד MIER1 ו-MIER3, שמסייעים להביא את ה-HDAC לאזורים ספציפיים ב-DNA. באמצעות ספקטרומטריה של מסה וניסויי משיכה בתאים אנושיים, הם מראים ש-C16orf87 פועל כמקשר בין HDAC1 ל-MIER1 בתוך קומפלקס MIER. כאשר רמות C16orf87 הופחתו על ידי התערבות RNA, או הוסרו לחלוטין באמצעות עריכה גנטית מבוססת CRISPR, רמות של מספר היסטונים השתנו, מה שמעיד שהמקשר הזה מסייע לשמור על שיווי המשקל הנכון של רכיבי אריזת ה-DNA. חיזויים מבניים מתקדמים עם AlphaFold3 תומכים עוד במודל שבו C16orf87 ברובו גמיש אך משתמש בזנב קצר ובמורכב כדי לעגינה בין HDAC1 לאזור המרכזי של MIER1, מה שמייצב את השותפות שלהם מבלי לשנות ישירות את הפעילות הכימית של HDAC1. 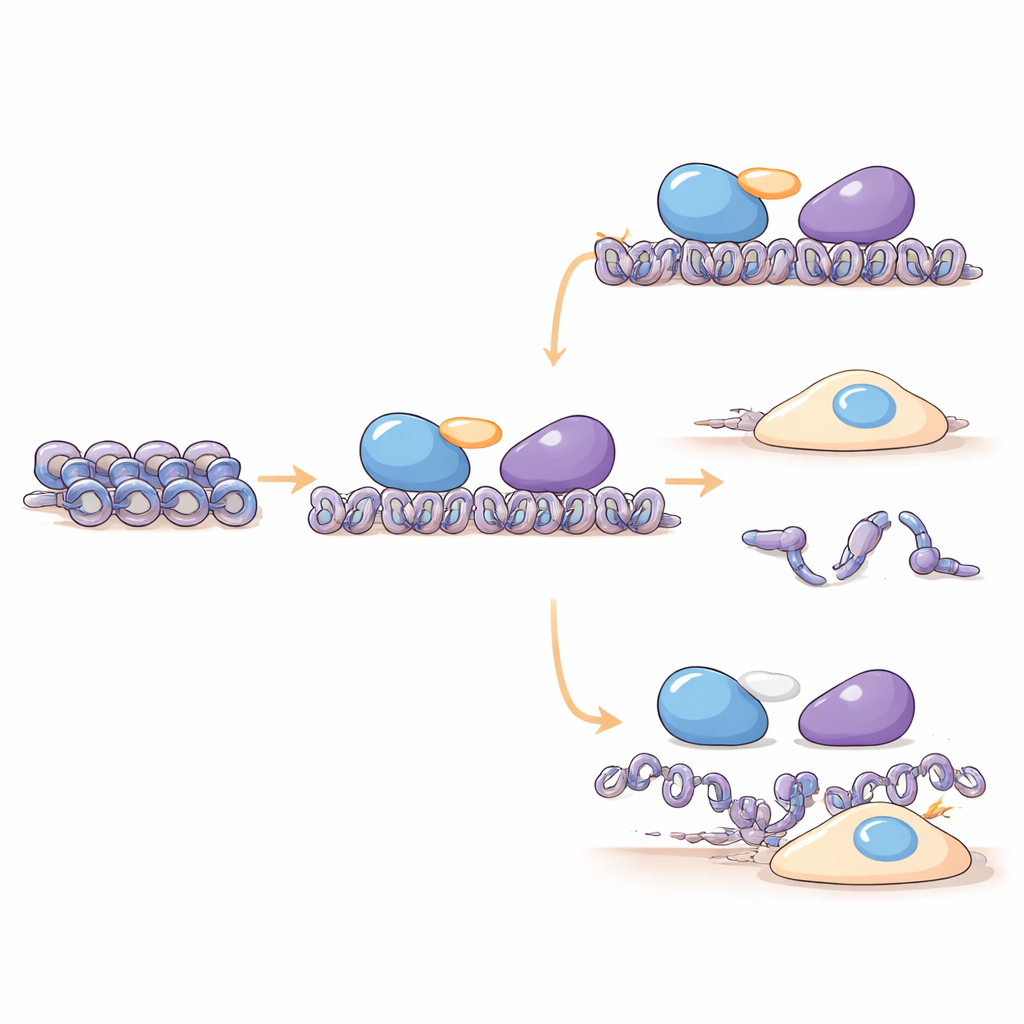
שינוי המקשר משנה את הכרומטין ואת התנהגות התא
כדי לראות מה קורה כאשר חלבון המקשר חסר, הצוות השמיט את C16orf87 בקו תאי סרטן הלבלב האנושי. התאים הערוכים הראו רמות מופחתות של מספר היסטונים מרכזיים אך, אולי באופן מפתיע, נותרו חיים ואף שכפלו את ה-DNA שלהם בקצב מעט מהיר יותר. עם זאת, כשבחנו כיצד תאים אלה נעים על פני משטח — התנהגות מפתח לתהליכים כמו תיקון פצעים ופיזור סרטן — התאים ללא C16orf87 זזו באופן משמעותי לאט יותר. מדידות רוחב-גנומיות של נגישות כרומטין (באמצעות ATAC-seq) חשפו שאיבוד C16orf87 הפך אזורים רבים ספציפיים ב-DNA ליותר פתוחים, במיוחד באתרים שכבר ידועים כיעדים של HDAC1/2 וחלבוני MIER. חלק מהאזורים הללו סמוכים לגןים המעורבים באיתות תאי ובתגובות לחץ, והשינויים בנגישות הכרומטין לעיתים קרובות הולכים יד ביד עם שינויים בפעילות הגנים.
מתאים בצלחת לפיתוח דגים
מכיוון שקומפלקסים המכילים HDAC ידועים כמנחים את ההתפתחות המוקדמת, החוקרים שאלו האם חלבון המקשר הזה חשוב גם באורגניזם שלם. הם הפריעו לגרסה של הגן בדג הזברה, הנקראת C7H16orf87, באמצעות CRISPR בעוברים. בהשוואה לאחים שלהם, הדגים שחסרו פעילות תקינה של C7H16orf87 היו קצרים יותר, בעלי עיניים ושטח גוף קטנים יותר, והראו גב מעוקל יותר וזווית ראש-לגוף משתנה. המומים האלה מגלים שהחלבון אינו הכרחי לחלוטין להישרדות אך חשוב לעיצוב ולצמיחה תקינים של הגוף המתפתח, ומחזק את הרעיון שבקרה עדינה של הכרומטין חיונית במהלך העובריות.
מה משמעות הדבר למחקר ולטיפול עתידי
ביחד, הממצאים מציירים את C16orf87/HDIP כאדפטור גמיש שמסייע להרכיב קומפלקס מדכא גנים ספציפי ולהכוונו לאתרים נבחרים בגנום. על ידי השפעה על אילו אזורים של ה-DNA דחוסים יותר מול נגישים, HDIP מעצב דפוסי פעילות גנטית שמשפיעים על הגירת תאים בתאי סרטן אנושיים ועל עיצוב הגוף בלארוות דג הזברה. מאחר ש-HDACs הם כבר מטרות של תרופות נגד סרטן, הבנת שותפיהם התומכים כמו HDIP עשויה לפתוח דלתות לטיפולים מדויקים יותר שיפעילו רק תכניות גנטיות מסוימות, במקום לחסום באופן כולל את כל פעילות ה-HDAC. עבודה זו הופכת שם גן עמום לסיפור פונקציונלי, וקושרת חיבורים מולקולריים בתוך הגרעין לשינויים נראים באופן שבו אורגניזמים גדלים ונעים.
ציטוט: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
מילות מפתח: וויסות כרומטין, היסטון דאצילאז, התפתחות עוברית, הגירת תאים, קומפלקס MIER