Clear Sky Science · de
Das C16orf87-Protein ist eine Untereinheit des MIER-Korrepressor-Komplexes, der die Embryonalentwicklung und Zellmigration steuert
Warum ein kleines Protein für Wachstum und Gesundheit wichtig ist
Jede Zelle in unserem Körper muss eine enorme Menge genetischer Information verwalten und die richtigen Gene zur richtigen Zeit ein- oder ausschalten. Diese Studie entfaltet die Rolle eines bislang rätselhaften menschlichen Proteins, C16orf87, das nun vorgeschlagen wird, in HDAC-interagierendes Protein (HDIP) umbenannt zu werden. Die Forschenden zeigen, dass dieses kleine Molekül beeinflusst, wie dicht unsere DNA verpackt ist, wie sich Krebszellen bewegen und wie Embryonen sich entwickeln – und damit grundlegende Genregulation mit Zellverhalten und Körperform in einem lebenden Organismus verbindet. 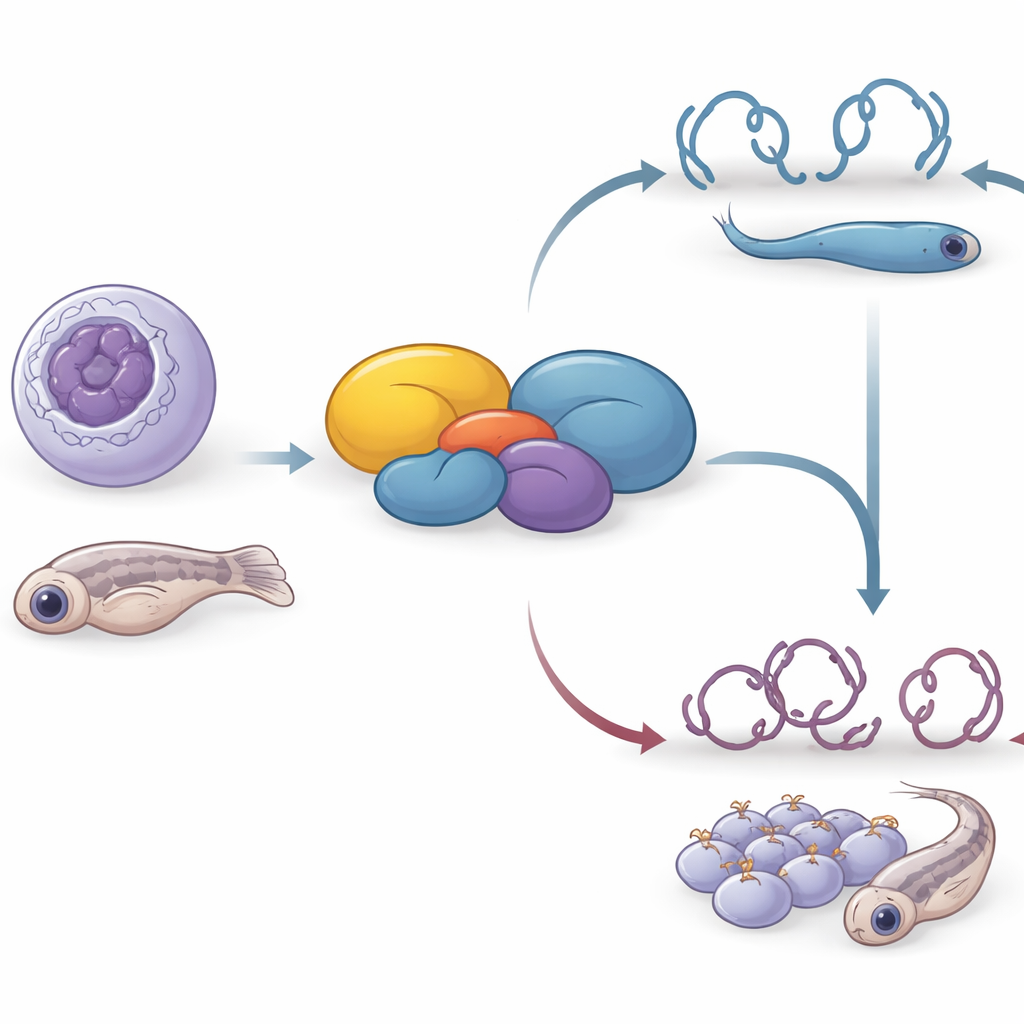
Ein verborgener Helfer bei der DNA-Verpackung
Die DNA in unseren Zellen ist um Proteine gewickelt und bildet so das Chromatin, das offener oder kompakter sein kann. Diese Verpackung beeinflusst stark, ob Gene aktiv oder stillgelegt sind. Enzyme, die als Histon-Deacetylasen (HDACs) bekannt sind, tragen dazu bei, Chromatin zu verdichten und Genaktivität zu unterdrücken. Sie arbeiten selten allein; stattdessen sind sie Teil größerer Proteinteams, so genannter Korrepressor-Komplexe. Viele Mitglieder dieser Komplexe sind noch wenig verstanden. Mithilfe von Proteinchemie, Strukturvorhersage und Zellexperimenten identifizieren die Autorinnen und Autoren C16orf87 als fehlendes Bauteil eines solchen Teams, des MIER-Korrepressor-Komplexes, zu dem auch das Schlüsselenzym HDAC1 gehört.
Wie HDIP eine Genabschalt-Maschine verbindet
Die Forschenden fanden heraus, dass C16orf87 physikalisch mit HDAC1, HDAC2 und den Gerüstproteinen MIER1 und MIER3 assoziiert, die HDACs zu bestimmten DNA-Abschnitten bringen. Mit Massenspektrometrie und Pull-down-Experimenten in menschlichen Zellen zeigen sie, dass C16orf87 als Verbindungsglied zwischen HDAC1 und MIER1 innerhalb des MIER-Komplexes fungiert. Wenn C16orf87 durch RNA-Interferenz reduziert oder mittels CRISPR vollständig entfernt wurde, änderten sich die Mengen mehrerer Histonproteine, was darauf hindeutet, dass dieses Verbindungselement hilft, das richtige Gleichgewicht der DNA-Verpackungskomponenten aufrechtzuerhalten. Fortgeschrittene Strukturvorhersagen mit AlphaFold3 stützen ferner ein Modell, in dem C16orf87 größtenteils flexibel ist, aber einen kurzen, gut geformten Schwanz nutzt, um zwischen HDAC1 und dem zentralen MIER1-Bereich anzudocken und deren Partnerschaft zu stabilisieren, ohne die chemische Aktivität von HDAC1 direkt zu verändern. 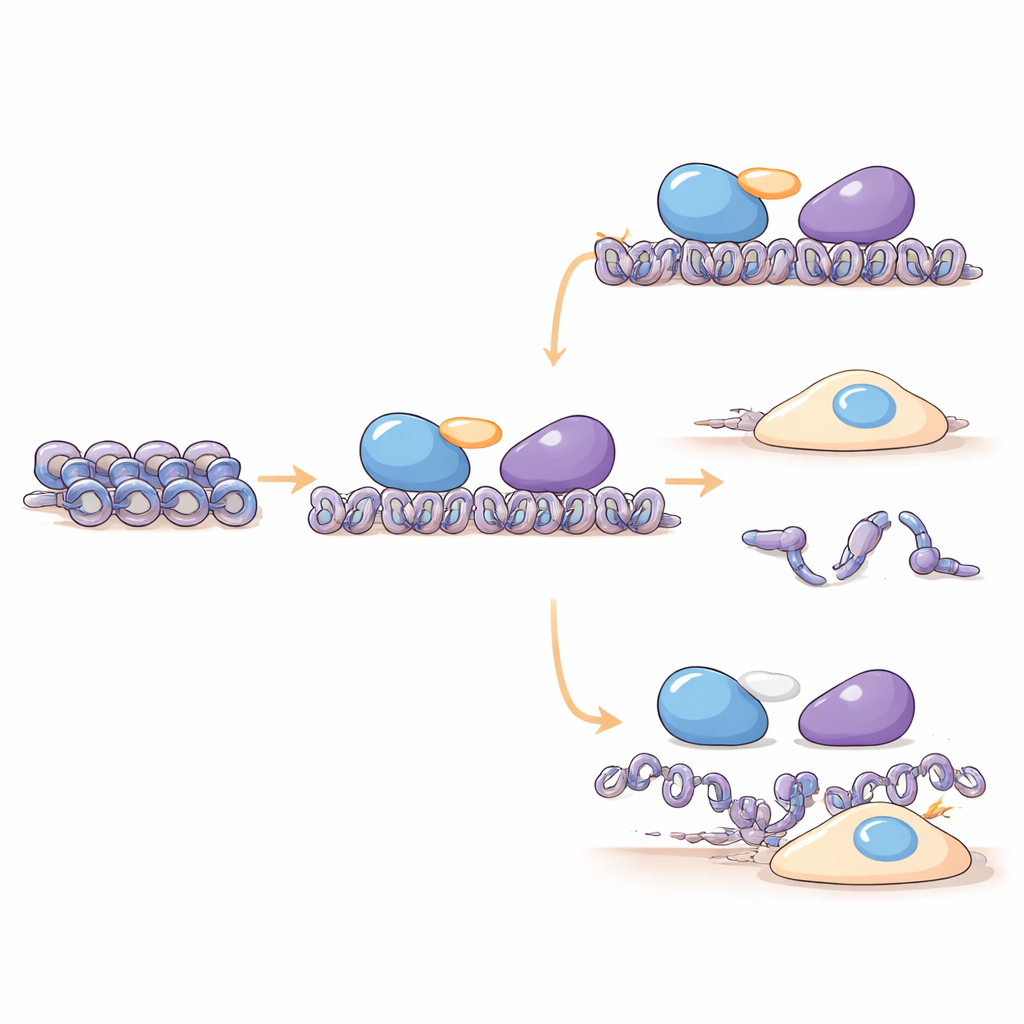
Ändert man das Verbindungselement, ändern sich Chromatin und Zellverhalten
Um zu prüfen, was passiert, wenn dieses Verbindungsprotein fehlt, löschte das Team C16orf87 in einer menschlichen Zelllinie des Pankreaskarzinoms. Die editierten Zellen zeigten reduzierte Mengen mehrerer Kernhistone, blieben aber, vielleicht überraschend, lebensfähig und replizierten sogar etwas schneller ihre DNA. Testeten die Wissenschaftler jedoch die Migration dieser Zellen über eine Oberfläche – ein wichtiges Verhalten für Prozesse wie Wundheilung und Krebsmetastasierung – bewegten sich die Zellen ohne C16orf87 deutlich langsamer. Genomweite Messungen der Chromatinzugänglichkeit (mittels ATAC-seq) zeigten, dass der Verlust von C16orf87 viele spezifische DNA-Regionen offener machte, insbesondere an Stellen, die zuvor als Ziele von HDAC1/2 und MIER-Proteinen bekannt waren. Einige dieser Regionen liegen in der Nähe von Genen, die an Zellsignalgebung und Stressantworten beteiligt sind, und Änderungen in der Chromatinöffnung gingen häufig mit Verschiebungen in der Genaktivität einher.
Von Zellen in der Schale zu sich entwickelnden Fischen
Da HDAC-haltige Komplexe bekanntlich die frühe Entwicklung steuern, fragten die Forschenden als Nächstes, ob dasselbe Verbindungsprotein in einem ganzen Organismus eine Rolle spielt. Sie störten die Zebrafisch-Version des Gens, C7H16orf87 genannt, mittels CRISPR in Embryonen. Im Vergleich zu ihren Geschwistern waren Fische ohne funktionelles C7H16orf87 kürzer, hatten kleinere Augen und eine geringere Körperoberfläche sowie einen stärker gekrümmten Rücken und einen veränderten Kopf-Körper-Winkel. Diese Defekte zeigen, dass das Protein nicht absolut überlebensnotwendig ist, wohl aber wichtig für die richtige Formung und das Wachstum des sich entwickelnden Körpers und unterstreichen die Vorstellung, dass fein abgestimmte Chromatinkontrolle während der Embryogenese essenziell ist.
Was das für künftige Forschung und Medizin bedeutet
Insgesamt zeichnen die Ergebnisse C16orf87/HDIP als flexiblen Adapter, der hilft, einen spezifischen Genabschalt-Komplex zusammenzubauen und ihn zu ausgewählten Stellen im Genom zu dirigieren. Indem HDIP beeinflusst, welche DNA-Regionen dicht gepackt versus zugänglich sind, formt es Muster der Genaktivität, die die Zellmigration in menschlichen Krebszellen und die Körperformung in Zebrafisch-Larven beeinflussen. Da HDACs bereits Ziele von Krebsmedikamenten sind, könnte das Verständnis ihrer unterstützenden Partner wie HDIP Wege zu präziseren Therapien eröffnen, die nur bestimmte Genprogramme lenken, statt die gesamte HDAC-Aktivität breit zu blockieren. Diese Arbeit verwandelt einen obskuren Gen-Namen in eine funktionale Geschichte und verknüpft molekulare Verbindungen im Zellkern mit sichtbaren Veränderungen im Wachstum und Verhalten von Organismen.
Zitation: Punga, T., Larsson, M., Mujica, E. et al. The C16orf87 protein is a subunit of the MIER corepressor complex controlling embryonic development and cell migration. Sci Rep 16, 13907 (2026). https://doi.org/10.1038/s41598-026-50740-7
Schlüsselwörter: Chromatinregulation, Histon-Deacetylase, Embryonalentwicklung, Zellmigration, MIER-Komplex