Clear Sky Science · zh
培养维度与基质组成对胰腺癌模型形态、表型及药物反应的影响
为何以新方式培养肿瘤很重要
胰腺癌是最致命的癌症之一,部分原因在于常常发现较晚且对许多常用药物有抵抗性。为了研发更好的治疗方法,研究人员依赖于在实验室中培养的肿瘤细胞作为真实肿瘤的替代模型。但这一方法背后有一个基本问题:我们培养这些细胞的方式是否会改变它们的行为及对药物的反应?本研究探讨了将胰腺肿瘤细胞以二维平面或三维簇状生长,以及在不同凝胶样基质中培养,是否真正改变了我们对疾病及其治疗的认识。
从患者肿瘤到实验室模型
研究者从 12 名胰腺导管腺癌患者采集了肿瘤样本,胰腺导管腺癌是最常见的胰腺癌类型。每个肿瘤样本都尝试建立三种实验室模型:经典的平板单层细胞(2D 培养),以及在两种商业凝胶基质(Matrigel 和 Cultrex)中生长的两类三维“微肿瘤”或类器官。这些凝胶模拟了体内围绕细胞的柔软、富含蛋白的基质。研究团队还检测了样本中的基因突变,以确认这些实验室模型确实来源于肿瘤细胞并携带已知的驱动性突变。 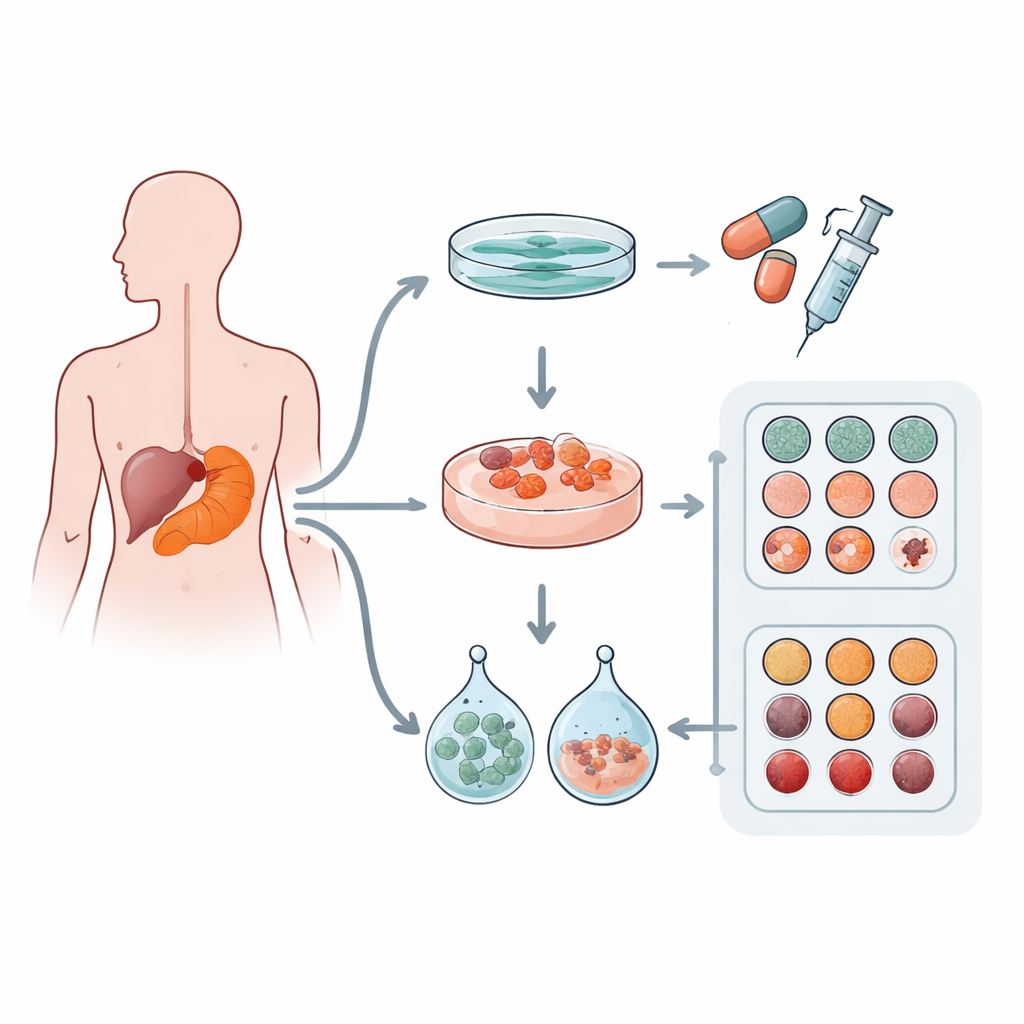
肿瘤细胞在实验室中的生长与形态
在比较细胞生长方式时,二维和平面与三维培养间的差异显著。在 2D 中,细胞展开成薄片状、很少聚集,远离体内肿瘤的外观。相比之下,在 3D 凝胶中生长的类器官形成致密的球状或中空囊泡样结构,更接近真实胰腺肿瘤的腺样构造。有趣的是,这些类器官的具体形态更多取决于个体患者的肿瘤特性,而非所用凝胶:分化较好的肿瘤形成腺样的类器官,而更具侵袭性的、分化差的肿瘤则产生致密的巢状团簇。总体而言,3D 培养的分裂速度更快,首次分裂所需时间较短,这与其增殖标志物 Ki‑67 显示的更高活性相呼应。
保持肿瘤身份的一致性
研究团队接着询问,这些不同的培养方式是否会扭曲细胞的基本身份。使用与医院病理实验室相似的染色技术,他们检查了定义胰腺导管癌的关键蛋白。像 CK19 和 GATA6 这样的标志物(表明导管样细胞类型)在 2D 和 3D 系统中均被保留。与肿瘤基因组相关的蛋白,包括 p53 和 SMAD4,呈现出与原始肿瘤一致的模式。细胞分裂标志物 Ki‑67 在所有实验室模型中均高于原始组织,反映了培养条件下促进生长的环境。另一个标志物 CDX2 在平面培养中尤其升高,提示某些细胞身份特征可能在体外发生改变。然而总体而言,2D 和 3D 方法都维持了患者肿瘤的核心特征。
在不同实验环境中测试化疗药物
研究的核心是评估培养形式(平面 vs 3D)和基质选择是否改变肿瘤细胞对胰腺癌常用化疗药物的反应,这些药物包括吉西他滨、5‑氟尿嘧啶、奥沙利铂、SN‑38 和紫杉醇。在这组小规模患者样本中,2D 细胞培养与两种类型的类器官之间的药物敏感性模式非常相似。三维模型通常略显更耐药,这与其更像肿瘤的结构和药物渗透受限相符,但这些差异较小且统计学上不显著。显著的则是患者间反应的高度差异:对几种药物(尤其是吉西他滨),不同患者的细胞耐药性相差很大,而这种差异与培养方式无关。在两名术后实际接受吉西他滨治疗的患者中,体外模型的结果与临床结局相呼应:其一模型更耐药的患者复发更快,其培养物中 MDR1(一种已知将药物泵出细胞的蛋白)水平更高。 
对未来癌症检测的意义
对普通读者而言,关键结论令人安心:标准化疗药物的体外测试结果主要受个体患者肿瘤本身差异的影响,远比细胞是以平面还是三维生长、或使用哪种常用凝胶更重要。这意味着现有的实验室系统在比较患者肿瘤对这些药物反应方面相对稳健。与此同时,3D 类器官更好地模拟了真实肿瘤的结构和生长行为,使其在研究疾病生物学以及用于更复杂或靶向治疗的研究中具有特殊价值。综合来看,这些发现支持越来越多地使用来源于患者的类器官作为现实且个体化的测试平台,未来有望帮助医生为胰腺癌患者量身定制治疗方案。
引用: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
关键词: 胰腺癌, 来源于患者的类器官, 3D 细胞培养, 化疗反应, 药物耐受性