Clear Sky Science · sv
Påverkan av odlingsdimensionalitet och matrixsammansättning på morfologi, fenotyp och läkemedelssvar i pankreascancermodeller
Varför nya sätt att odla tumörer spelar roll
Pankreascancer är en av de dödligaste cancerformerna, delvis därför att den ofta upptäcks sent och är resistent mot många vanliga läkemedel. För att utveckla bättre behandlingar förlitar sig forskare på tumörceller odlade i laboratoriet som modeller för verkliga cancerformer. Men en grundläggande fråga bakom detta angreppssätt är: förändrar sättet vi odlar dessa celler hur de beter sig och svarar på läkemedel? Denna studie undersöker huruvida odling av pankreastumörceller i plana lager eller i tredimensionella kluster, och i olika geléliknande material, verkligen förändrar vad vi lär oss om sjukdomen och dess behandling.
Från patienttumör till laboratoriemodeller
Forskarlaget samlade tumörprover från 12 patienter med pankreasslemhinnekörteladenokarcinom, den vanligaste formen av pankreascancer. Från varje tumör försökte de skapa tre typer av laboratoriemodeller: ett klassiskt platt cellskikt i en odlingsskål (2D-kultur) och två typer av tredimensionella ”mini‑tumörer”, eller organoider, odlade i två olika kommersiella gelmatriser kallade Matrigel och Cultrex. Dessa geler efterliknar det mjuka, proteinrika material som omger celler i kroppen. Teamet kontrollerade också vilka genetiska mutationer som fanns för att bekräfta att de laboratorieodlade modellerna verkligen kom från cancerceller och bar välkända drivermutationer. 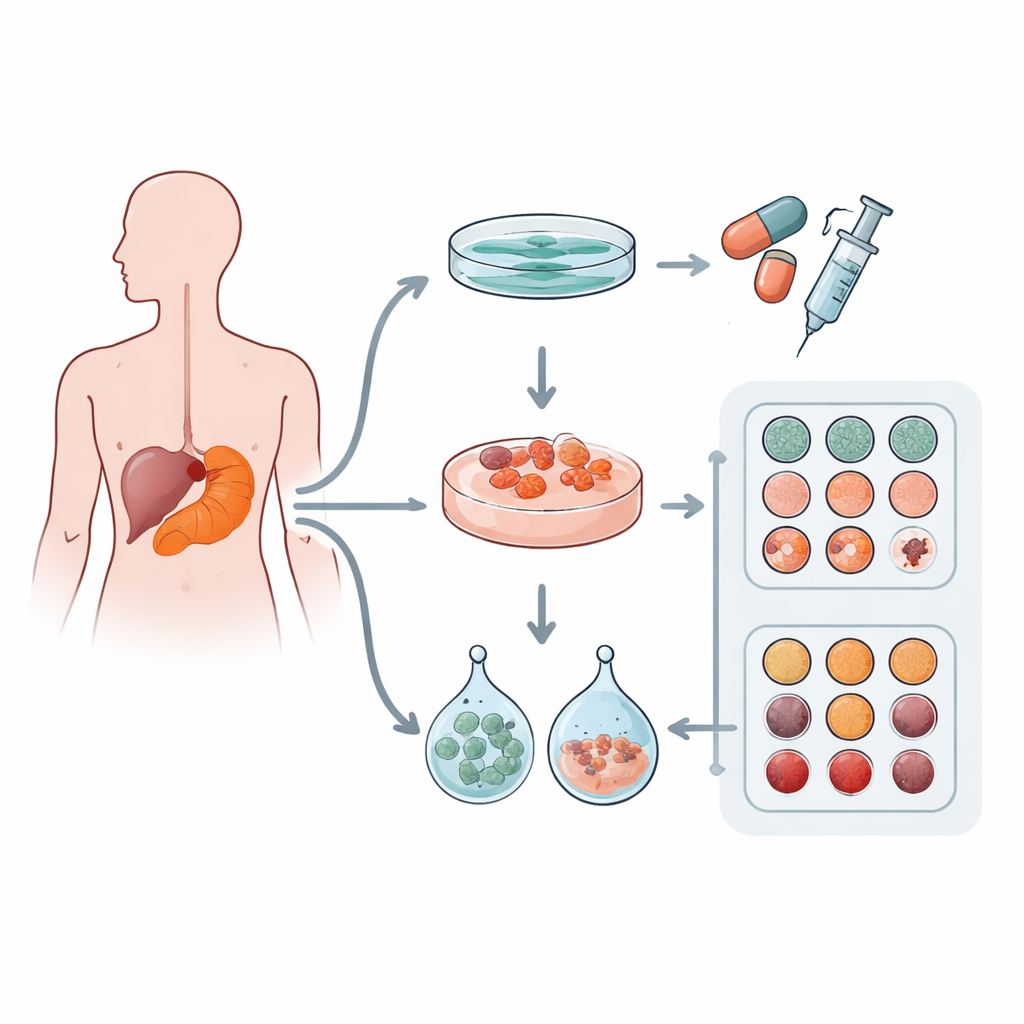
Hur tumörceller växer och ser ut i labbet
När de jämförde cellernas tillväxt var skillnaderna mellan plana och 3D‑kulturer slående. I 2D spred sig cellerna ut som tunna ark med liten ansamling, ett mönster som ligger långt från hur tumörer ser ut i kroppen. I kontrast bildade organoider odlade i 3D‑geler kompakta sfärer eller ihåliga, cystliknande strukturer som mer liknade de körtelliknande arkitekturerna hos verkliga pankreastumörer. Intressant nog berodde organoidernas exakta form mer på den enskilda patientens tumör än på vilken gel som användes: de bättre differentierade cancerformerna bildade körtelliknande organoider, medan en mer aggressiv, dåligt differentierad tumör producerade täta, näst‑liknande kluster. Över alla villkor delade 3D‑kulturer sig snabbare och behövde mindre tid innan första delningen än de plana kulturerna, vilket återspeglas i högre aktivitet i deras cellcykelmarkör, Ki‑67.
Att bevara tumörens identitet
Teamet frågade sedan om dessa olika odlingssätt kunde förvränga cellernas grundläggande identitet. Med hjälp av färgningstekniker liknande dem som används i patologiska laboratorier undersökte de viktiga proteiner som definierar pankreasslemhinnetumörer. Markörer som CK19 och GATA6, som signalerar en gånglik celltyp, bevarades i både plana och 3D‑system. Proteiner kopplade till tumörernas genetiska uppsättning, inklusive p53 och SMAD4, visade mönster som stämde överens med de ursprungliga tumörerna. En markör för celldelning, Ki‑67, var högre i alla laboratoriemodeller än i det ursprungliga vävnadsprovet, vilket speglar de odlingsfrämjande förhållandena i kultur. En annan markör, CDX2, ökade särskilt i platta kulturer, vilket antyder att vissa aspekter av cellidentitet kan skifta i labbet. Sammantaget upprätthöll dock både 2D‑ och 3D‑metoderna de grundläggande dragen hos patienternas cancerformer.
Test av kemoterapi i olika laboratorievärldar
Studiens kärna var att se om odlingsformat—platt kontra 3D, och val av gel—ändrar hur tumörceller svarar på vanliga cytostatika som används vid pankreascancer, inklusive gemcitabin, 5‑fluorouracil, oxaliplatin, SN‑38 och paklitaxel. I det begränsade patientmaterialet var läkemedelskänslighetsmönstren anmärkningsvärt lika mellan 2D‑kulturer och båda typerna av organoider. Tredimensionella modeller tenderade att vara något mer läkemedelsresistenta, vilket överensstämmer med deras mer tumörlika struktur och begränsad läkemedelspenetration, men dessa skillnader var måttliga och inte statistiskt starka. Det som verkligen utmärkte sig var hur mycket svaren varierade från patient till patient: för flera läkemedel, särskilt gemcitabin, var vissa patienters celler avsevärt mer resistenta än andra, oberoende av odlingssätt. Hos två patienter som faktiskt fick gemcitabin efter operation speglade laboratorieresultaten verkligheten: patienten vars modeller var mer resistenta fick tidigare recidiv, och deras kulturer visade högre nivåer av MDR1, ett protein som är känt för att pumpa ut läkemedel ur celler. 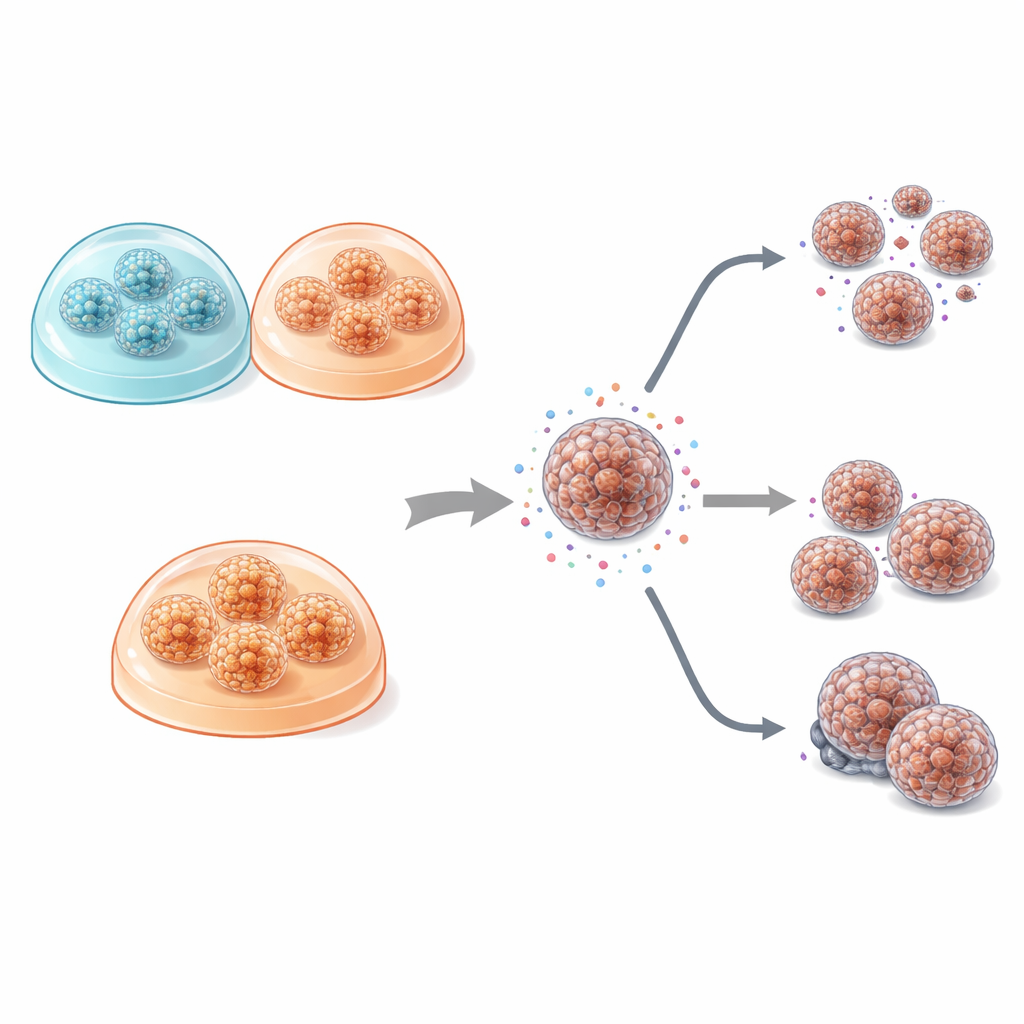
Vad detta betyder för framtida cancerprovning
För en allmän läsare är huvudslutsatsen lugnande: huvudbudskapet från laboratorietester av standardkemoterapier verkar bero mycket mer på den enskilda patientens tumör än på om cellerna odlas platt eller som 3D‑kluster, eller vilken vanlig gel som används. Det betyder att befintliga labsystem är rimligt robusta för att jämföra hur patienters tumörer svarar på dessa läkemedel. Samtidigt efterliknar 3D‑organoider bättre den verkliga tumörens struktur och tillväxtbeteende, vilket gör dem särskilt värdefulla för att studera sjukdomsbiologi och eventuellt för mer komplexa eller riktade terapier. Tillsammans stöder dessa fynd den växande användningen av patientavledda organoider som realistiska, patientanpassade testbäddar som en dag skulle kunna hjälpa läkare att skräddarsy behandlingar för personer med pankreascancer.
Citering: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
Nyckelord: pankreascancer, patientavledda organoider, 3D cellkultur, kemoterapysvar, läkemedelsresistens