Clear Sky Science · it
Impatto della dimensionalità della coltura e della composizione della matrice su morfologia, fenotipo e risposta ai farmaci nei modelli del cancro al pancreas
Perché coltivare i tumori in modi nuovi è importante
Il cancro del pancreas è uno dei tumori più letali, in parte perché spesso viene diagnosticato tardivamente e resiste a molti farmaci comuni. Per sviluppare terapie migliori, i ricercatori si affidano a cellule tumorali coltivate in laboratorio come sostituti dei tumori reali. Ma dietro questo approccio c’è una domanda fondamentale: il modo in cui coltiviamo queste cellule cambia il loro comportamento e la loro risposta ai farmaci? Questo studio esplora se crescere le cellule tumorali pancreatiche in strati piatti o in aggregati tridimensionali, e in diversi materiali gel‑like, cambi davvero ciò che impariamo sulla malattia e sul suo trattamento.
Dal tumore del paziente ai modelli coltivati in laboratorio
I ricercatori hanno raccolto campioni tumorali da 12 pazienti con adenocarcinoma duttale pancreatico, la forma più comune di cancro al pancreas. Da ciascun tumore hanno cercato di creare tre tipi di modelli di laboratorio: uno strato classico di cellule su piastra (coltura 2D) e due tipi di “mini‑tumori” tridimensionali, o organoidi, coltivati in due differenti matrici gel commerciali chiamate Matrigel e Cultrex. Questi gel imitano il materiale morbido e ricco di proteine che circonda le cellule nell’organismo. Il gruppo ha inoltre verificato quali mutazioni genetiche erano presenti per confermare che i modelli coltivati provenissero davvero da cellule tumorali e conservassero note mutazioni driver. 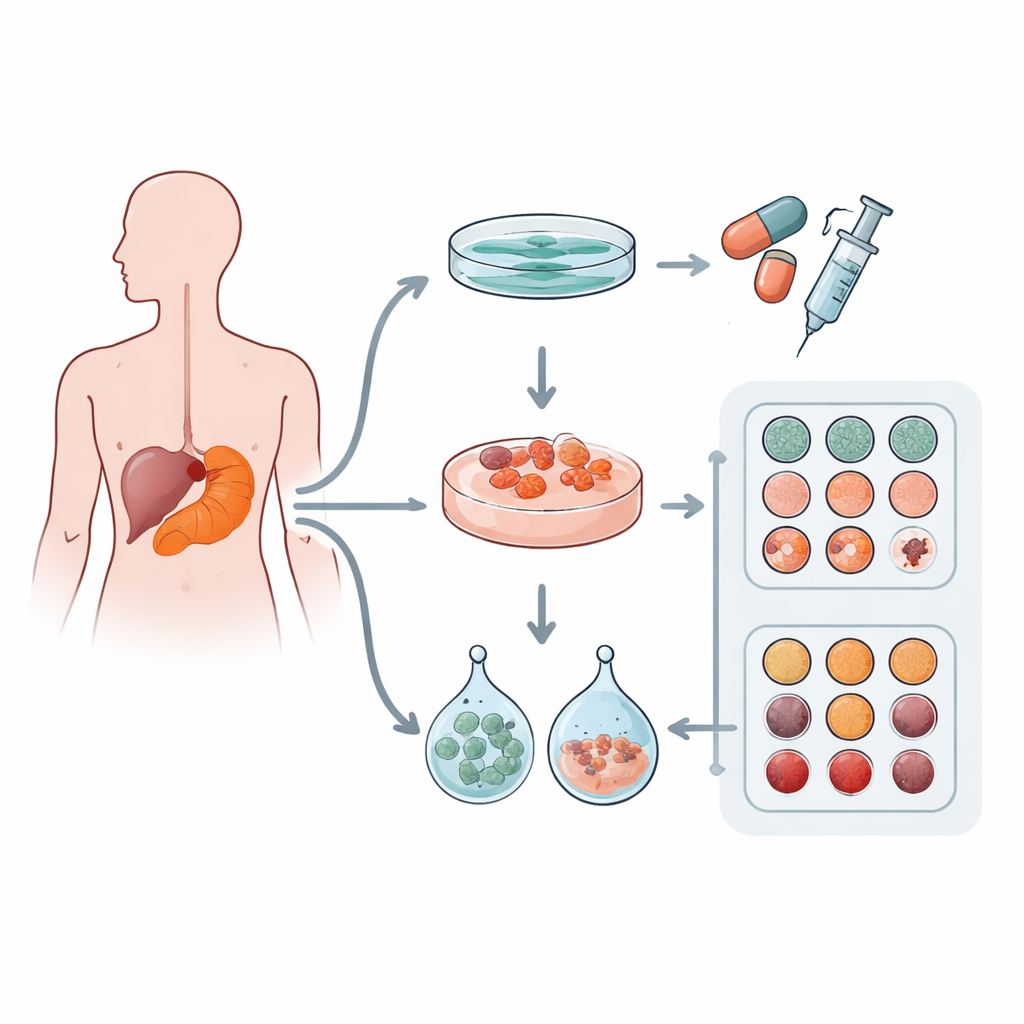
Come le cellule tumorali crescono e appaiono in laboratorio
Confrontando la crescita cellulare, le differenze tra colture piatte e 3D sono risultate marcate. In 2D le cellule si dispongono in sottili foglietti con scarsa tendenza ad aggregarsi, un profilo molto diverso dall’aspetto dei tumori in vivo. Al contrario, gli organoidi coltivati in gel 3D formano sfere compatte o strutture cave simili a cisti che somigliano maggiormente all’architettura ghiandolare dei tumori pancreatici reali. Interessante notare che la forma esatta di questi organoidi dipendeva più dal tumore del singolo paziente che dal tipo di gel utilizzato: i tumori meglio differenziati generavano organoidi con aspetto ghiandolare, mentre un tumore più aggressivo e poco differenziato dava origine a aggregati densi a nido. In tutte le condizioni, le colture 3D si dividevano più rapidamente e richiedevano meno tempo fino alla prima divisione rispetto alle colture piatte, in linea con livelli più elevati del marcatore di proliferazione Ki‑67.
Mantenere intatta l’identità del tumore
Il gruppo ha quindi verificato se questi diversi metodi di coltura potessero alterare l’identità di base delle cellule. Usando tecniche di colorazione simili a quelle dei laboratori di anatomia patologica, hanno analizzato proteine chiave che definiscono i tumori duttali pancreatici. Marcatori come CK19 e GATA6, che segnalano un tipo cellulare duttale, sono risultati preservati sia nei sistemi 2D sia in quelli 3D. Proteine legate al profilo genetico del tumore, inclusi p53 e SMAD4, hanno mostrato pattern coerenti con i tumori originali. Un marcatore della divisione cellulare, Ki‑67, era più elevato in tutti i modelli di laboratorio rispetto al tessuto originale, riflettendo le condizioni favorevoli alla crescita in coltura. Un altro marcatore, CDX2, aumentava in particolare nelle colture piatte, suggerendo che alcuni aspetti dell’identità cellulare possono spostarsi in laboratorio. Nel complesso, tuttavia, sia l’approccio 2D che quello 3D hanno mantenuto le caratteristiche fondamentali dei tumori dei pazienti.
Testare la chemioterapia in diversi mondi di laboratorio
Il fulcro dello studio era capire se il formato di coltura — piatto versus 3D, e la scelta della matrice — modificasse la risposta delle cellule tumorali ai farmaci chemioterapici comuni per il cancro pancreatico, inclusi gemcitabina, 5‑fluorouracile, oxaliplatino, SN‑38 e paclitaxel. Nel piccolo gruppo di pazienti, i pattern di sensibilità ai farmaci sono risultati sorprendentemente simili tra le colture 2D e entrambi i tipi di organoidi. I modelli tridimensionali tendevano a essere leggermente più resistenti ai farmaci, coerente con la loro struttura più simile al tumore e una penetrazione dei farmaci più limitata, ma queste differenze erano modeste e non statisticamente robuste. Ciò che è emerso con chiarezza è stata la grande variabilità delle risposte da paziente a paziente: per diversi farmaci, in particolare la gemcitabina, le cellule di alcuni pazienti erano molto più resistenti di altre, indipendentemente dal modo di coltura. In due pazienti che hanno ricevuto effettivamente gemcitabina dopo l’intervento chirurgico, i risultati di laboratorio hanno rispecchiato la realtà clinica: il paziente i cui modelli erano più resistenti è recidivato prima, e le loro colture mostravano livelli più elevati di MDR1, una proteina nota per espellere i farmaci dalle cellule. 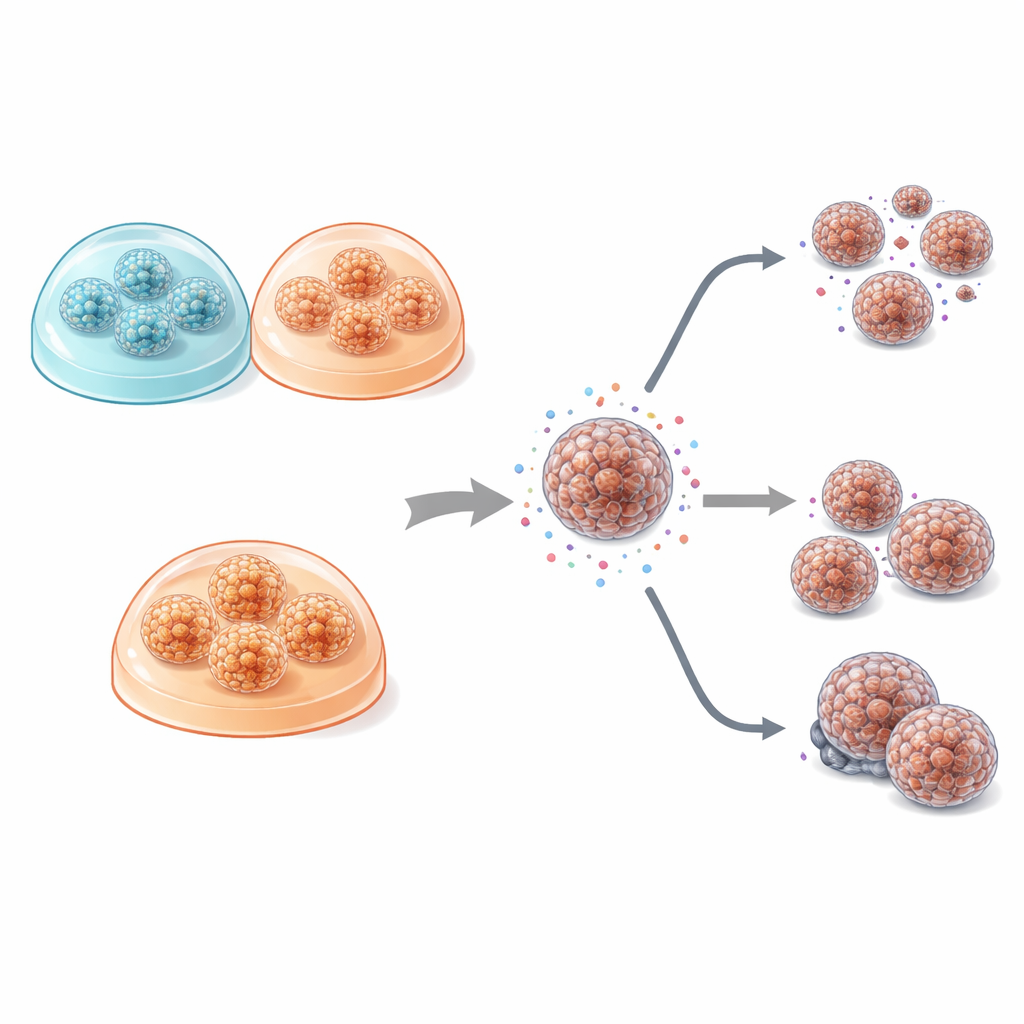
Cosa significa per i test sul cancro futuri
Per il lettore non specialistico, la conclusione principale è rassicurante: il messaggio principale che emerge dai test di laboratorio sui chemioterapici standard sembra dipendere molto più dal tumore del singolo paziente che dal fatto che le cellule siano coltivate in modo piatto o come aggregati 3D, o dal tipo di gel comunemente usato. Ciò significa che i sistemi di laboratorio esistenti sono ragionevolmente robusti per confrontare come i tumori dei pazienti rispondono a questi farmaci. Allo stesso tempo, gli organoidi 3D ricreano meglio la struttura e il comportamento di crescita del tumore reale, rendendoli particolarmente utili per studiare la biologia della malattia e, forse, per terapie più complesse o mirate. Nel complesso, questi risultati supportano l’uso crescente di organoidi derivati dai pazienti come piattaforme realistiche e specifiche per paziente che potrebbero un giorno aiutare i medici a personalizzare i trattamenti per le persone con cancro al pancreas.
Citazione: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
Parole chiave: cancro del pancreas, organoidi derivati da paziente, coltura cellulare 3D, risposta alla chemioterapia, resistenza ai farmaci