Clear Sky Science · fr
Impact de la dimensionnalité du modèle de culture et de la composition de la matrice sur la morphologie, le phénotype et la réponse aux médicaments dans des modèles du cancer du pancréas
Pourquoi il est important de cultiver les tumeurs autrement
Le cancer du pancréas figure parmi les cancers les plus meurtriers, en partie parce qu’il est souvent détecté tardivement et résiste à de nombreux traitements courants. Pour mettre au point de meilleures thérapies, les chercheurs s’appuient sur des cellules tumorales cultivées en laboratoire comme substituts des tumeurs réelles. Mais une question fondamentale se pose : la façon dont nous cultivons ces cellules modifie‑t‑elle leur comportement et leur réponse aux médicaments ? Cette étude examine si la culture des cellules tumorales pancréatiques en couches plates ou en amas tridimensionnels, et dans différents gels, change réellement ce que l’on apprend sur la maladie et son traitement.
Du prélèvement tumoral aux modèles cultivés en laboratoire
Les chercheurs ont recueilli des échantillons tumoraux chez 12 patients atteints d’adénocarcinome canalaire pancréatique, la forme la plus fréquente du cancer du pancréas. Pour chaque tumeur, ils ont essayé de créer trois types de modèles : une culture classique en couche plate dans une boîte (culture 2D) et deux types de « mini‑tumeurs » tridimensionnelles, ou organoïdes, cultivés dans deux matrices gélifiées commerciales appelées Matrigel et Cultrex. Ces gels imitent le matériau mou et riche en protéines qui entoure les cellules dans l’organisme. L’équipe a également vérifié les mutations génétiques présentes pour confirmer que ces modèles dérivés en laboratoire provenaient bien des cellules tumorales et portaient des mutations connues comme drivers. 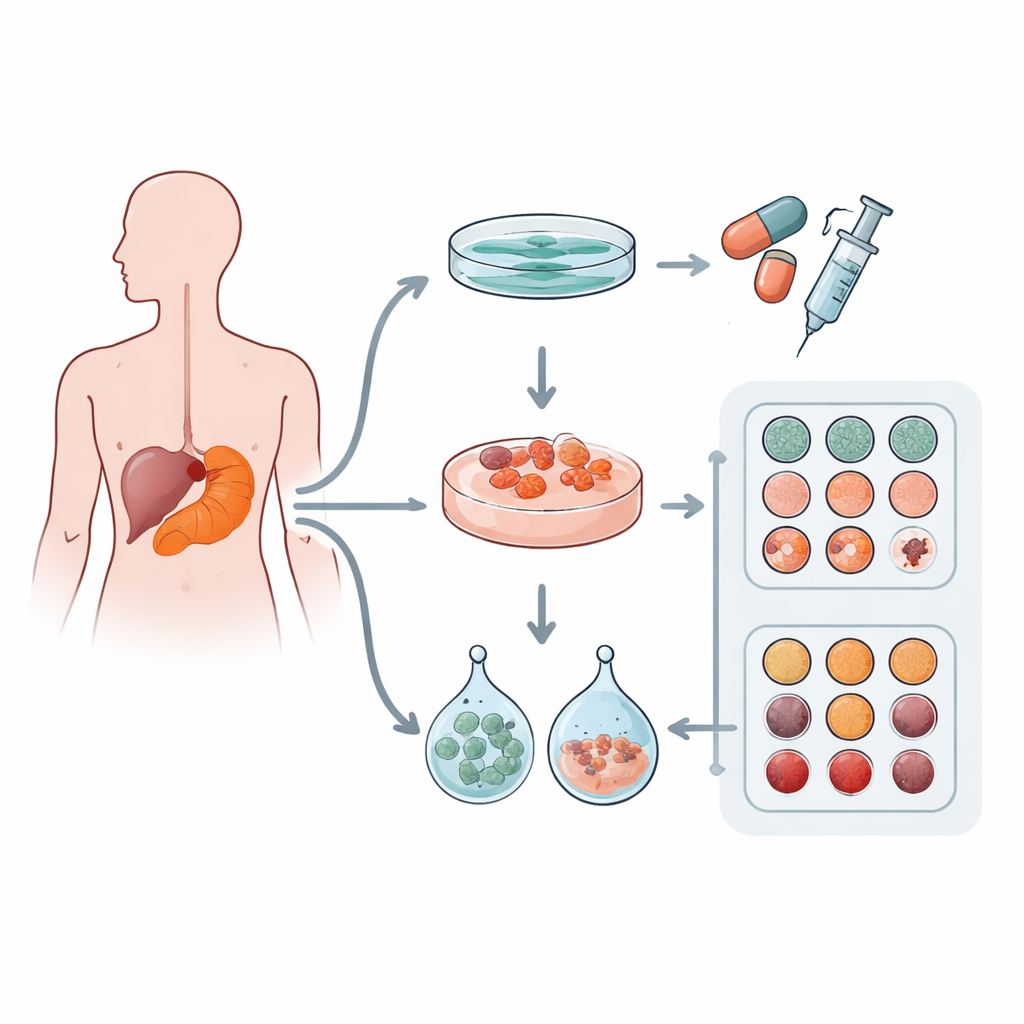
Comment les cellules tumorales poussent et s’organisent en laboratoire
En comparant la croissance cellulaire, les différences entre cultures plates et 3D sont apparues frappantes. En 2D, les cellules s’étalaient en feuillets minces avec peu de regroupement, un schéma éloigné de l’apparence des tumeurs in vivo. En revanche, les organoïdes en 3D formés dans les gels constituaient des sphères compactes ou des structures creuses en forme de kyste qui ressemblaient davantage à l’architecture glandulaire des tumeurs pancréatiques réelles. Fait intéressant, la forme exacte de ces organoïdes dépendait davantage de la tumeur du patient que du gel utilisé : les cancers mieux différenciés donnaient des organoïdes de type glandulaire, tandis qu’une tumeur plus agressive et peu différenciée produisait des amas denses en nids. Toutes conditions confondues, les cultures 3D se divisaient plus rapidement et nécessitaient moins de temps avant leur première division que les cultures plates, ce qui se retrouvait dans des niveaux plus élevés du marqueur de prolifération Ki‑67.
Conserver l’identité tumorale
L’équipe a ensuite examiné si ces différentes méthodes de culture pouvaient altérer l’identité fondamentale des cellules. À l’aide de techniques de coloration similaires à celles des laboratoires de pathologie hospitaliers, ils ont étudié des protéines clés qui définissent les cancers canalaires pancréatiques. Des marqueurs tels que CK19 et GATA6, indicateurs d’un phénotype de type canal, ont été préservés tant en 2D qu’en 3D. Des protéines liées au profil génétique de la tumeur, y compris p53 et SMAD4, montraient des schémas concordant avec les tumeurs d’origine. Un marqueur de prolifération, Ki‑67, était plus élevé dans tous les modèles en laboratoire que dans le tissu initial, reflet des conditions de culture favorisant la croissance. Un autre marqueur, CDX2, augmentait particulièrement en culture plate, laissant entendre que certains aspects de l’identité cellulaire peuvent évoluer en laboratoire. Dans l’ensemble, toutefois, les approches 2D et 3D ont conservé les caractéristiques centrales des cancers des patients.
Tester la chimiothérapie dans différents environnements de laboratoire
Le cœur de l’étude a consisté à déterminer si le format de culture — plat versus 3D, et le choix du gel — modifie la sensibilité des cellules tumorales aux médicaments de chimiothérapie couramment utilisés pour le cancer du pancréas, notamment la gemcitabine, le 5‑fluorouracile, l’oxaliplatine, le SN‑38 et le paclitaxel. Dans cet ensemble restreint de patients, les profils de sensibilité aux médicaments étaient remarquablement semblables entre les cultures 2D et les deux types d’organoïdes. Les modèles 3D montraient une tendance à une résistance légèrement plus élevée, cohérente avec leur structure plus proche de la tumeur et une pénétration limitée des médicaments, mais ces différences restaient modestes et peu robustes statistiquement. Ce qui ressortait surtout, c’est l’importante variabilité d’un patient à l’autre : pour plusieurs médicaments, en particulier la gemcitabine, certaines lignées issues de patients étaient beaucoup plus résistantes que d’autres, indépendamment du mode de culture. Chez deux patients ayant effectivement reçu de la gemcitabine après chirurgie, les résultats in vitro reflétaient la réalité clinique : le patient dont les modèles étaient plus résistants a rechuté plus rapidement, et ses cultures présentaient des niveaux plus élevés de MDR1, une protéine connue pour expulser les médicaments hors des cellules. 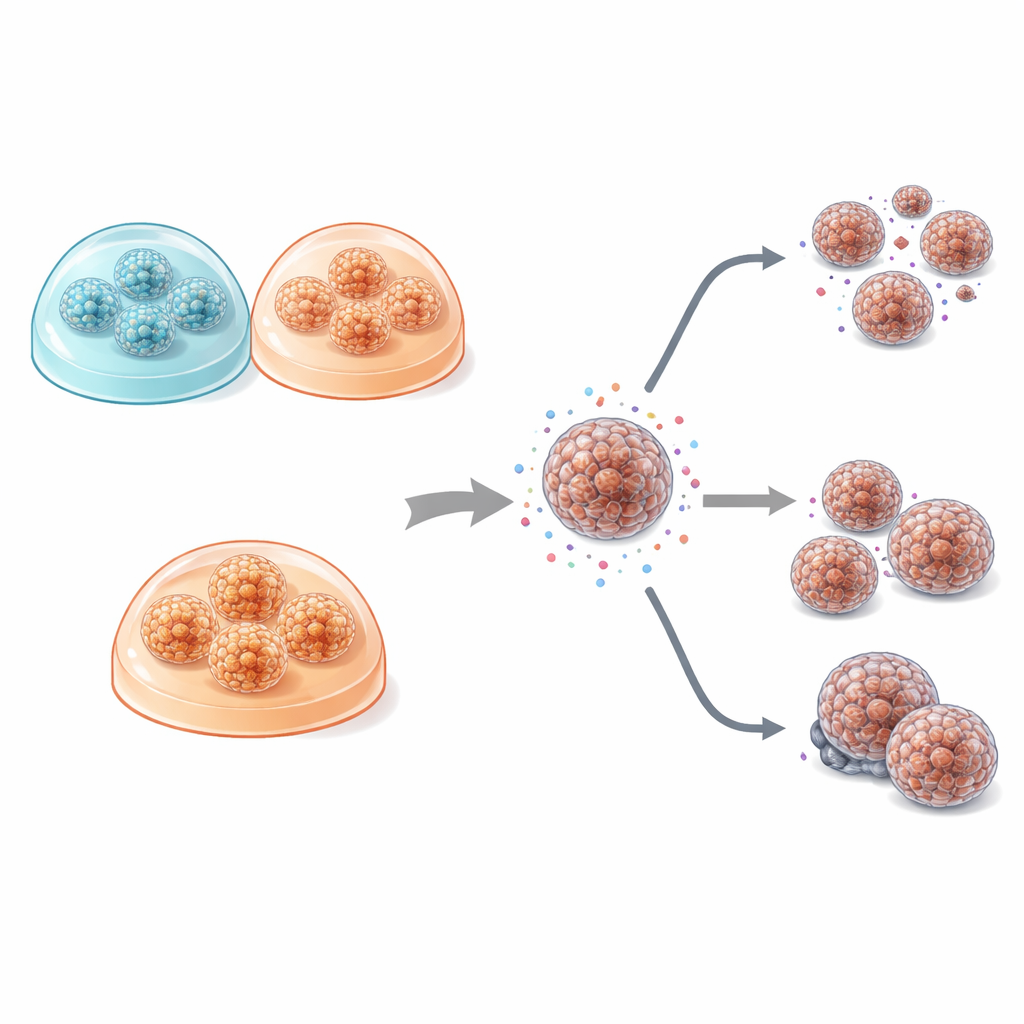
Ce que cela implique pour les tests oncologiques futurs
Pour un lecteur non spécialiste, la conclusion principale est rassurante : les résultats des tests en laboratoire sur des médicaments de chimiothérapie standards semblent dépendre bien plus de la tumeur individuelle du patient que du fait que les cellules soient cultivées à plat ou en amas 3D, ou du gel utilisé. Cela signifie que les systèmes de laboratoire actuels sont relativement robustes pour comparer la réponse des tumeurs des patients à ces traitements. En même temps, les organoïdes 3D reproduisent mieux la structure et le comportement de croissance des tumeurs réelles, ce qui les rend particulièrement utiles pour étudier la biologie de la maladie et, potentiellement, pour des thérapies plus ciblées ou complexes. Ensemble, ces résultats étayent l’utilisation croissante des organoïdes dérivés de patients comme plateformes réalistes et personnalisées qui pourraient, un jour, aider les cliniciens à adapter les traitements pour les personnes atteintes d’un cancer du pancréas.
Citation: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
Mots-clés: cancer du pancréas, organoïdes dérivés de patients, culture cellulaire 3D, réponse à la chimiothérapie, résistance aux médicaments