Clear Sky Science · ru
Влияние размерности культивирования и состава матрикса на морфологию, фенотип и реакцию на лекарства в моделях рака поджелудочной железы
Почему важно по‑новому выращивать опухоли
Рак поджелудочной железы — один из самых смертельных видов рака, отчасти потому, что часто выявляется на поздних стадиях и устойчив ко многим обычным лекарствам. Для разработки лучших подходов ученые используют опухолевые клетки, выращенные в лаборатории, как замену реальным опухолям. Но в основе этого подхода лежит простой вопрос: меняет ли способ выращивания этих клеток их поведение и ответ на лекарства? В этом исследовании изучали, действительно ли выращивание опухолевых клеток поджелудочной железы в плоских слоях или в трехмерных скоплениях, а также в разных гелеподобных материалах, меняет выводы о болезни и её лечении.
От опухоли пациента к лабораторным моделям
Исследователи собрали образцы опухолей у 12 пациентов с аденокарциномой протоков поджелудочной железы — самой распространенной формой рака поджелудочной железы. Из каждой опухоли они пытались получить три типа лабораторных моделей: классический плоский слой клеток в чашке (2D культура) и два типа трехмерных «мини‑опухолей», или органоидов, выращенных в разных коммерческих матриксах — Matrigel и Cultrex. Эти гели имитируют мягкую белковую среду, окружающую клетки в организме. Команда также проверяла наличие генетических мутаций, чтобы подтвердить, что лабораторные модели действительно происходят из раковых клеток и несут хорошо известные драйверные мутации. 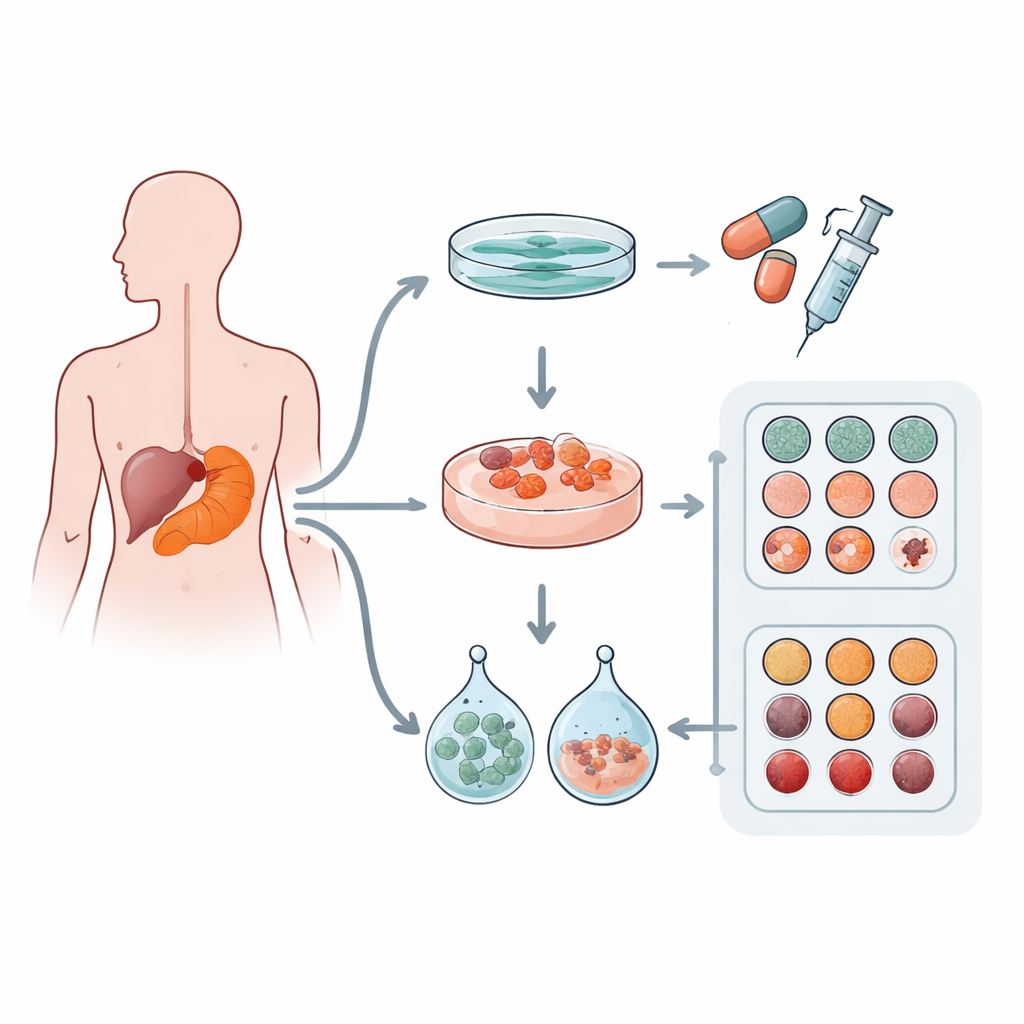
Как опухолевые клетки растут и выглядят в лаборатории
При сравнении роста клеток различия между плоскими и 3D культурами были заметны. В 2D клетки распространялись тонкими пластами с малым скоплением, что сильно отличалось от того, как опухоли выглядят в организме. Напротив, органоиды, выращенные в 3D гелях, формировали компактные сферы или полые, кистой подобные структуры, ближе по форме к железистому строению настоящих опухолей поджелудочной. Любопытно, что точная форма органоидов больше зависела от опухоли конкретного пациента, чем от типа геля: лучше дифференцированные опухоли формировали железистоподобные органоиды, тогда как более агрессивная, плохо дифференцированная опухоль давала плотные, гнездовые скопления. Во всех условиях 3D культуры делились быстрее и требовали меньше времени до первого расщепления, что соответствовало повышенной активности по маркеру деления клеток Ki‑67.
Сохранение идентичности опухоли
Далее команда проверила, не искажают ли разные способы выращивания базовую идентичность клеток. С помощью окрашивания, схожего с используемым в патологических лабораториях, они изучали ключевые белки, определяющие протоковую природу рака поджелудочной. Маркеры такие как CK19 и GATA6, указывающие на протоковый фенотип, сохранялись и в плоских, и в 3D системах. Белки, связанные с генетическим профилем опухоли, включая p53 и SMAD4, показывали паттерны, соответствующие исходным опухолям. Маркер деления клеток Ki‑67 оказался выше во всех лабораторных моделях по сравнению с исходной тканью, что отражает стимулирующие рост условия культивирования. Другой маркер, CDX2, особенно повышался в плоских культурах, что намекает на то, что некоторые аспекты идентичности клетки могут смещаться в лаборатории. В целом же и 2D, и 3D подходы сохраняли ключевые особенности опухолей пациентов.
Тестирование химиотерапии в разных лабораторных «мирах»
Главная цель исследования — выяснить, меняет ли формат культивирования (плоский против 3D) и выбор геля чувствительность опухолевых клеток к обычным химиотерапевтическим препаратам, применяемым при раке поджелудочной, включая гемцитабин, 5‑фторурацил, оксалиплатин, SN‑38 и паклитаксел. В рамках небольшой когорты пациентов паттерны чувствительности к препаратам оказались поразительно схожи между 2D культурами и обоими типами органоидов. Трехмерные модели в целом были немного более устойчивы к препаратам, что согласуется с их более опухолеподобной структурой и ограниченным проникновением лекарств, но эти различия были умеренными и статистически незначимыми. Более заметным оказалось межпациентное разнообразие ответов: для нескольких препаратов, особенно гемцитабина, клетки некоторых пациентов были значительно более устойчивы, чем у других, независимо от способа культивирования. У двух пациентов, которые действительно получали гемцитабин после операции, лабораторные результаты отражали клиническую картину: у пациента, чьи модели были более устойчивы, рецидив наступил раньше, и в культурах был выше уровень MDR1 — белка, известного выталкивающего лекарства из клетки. 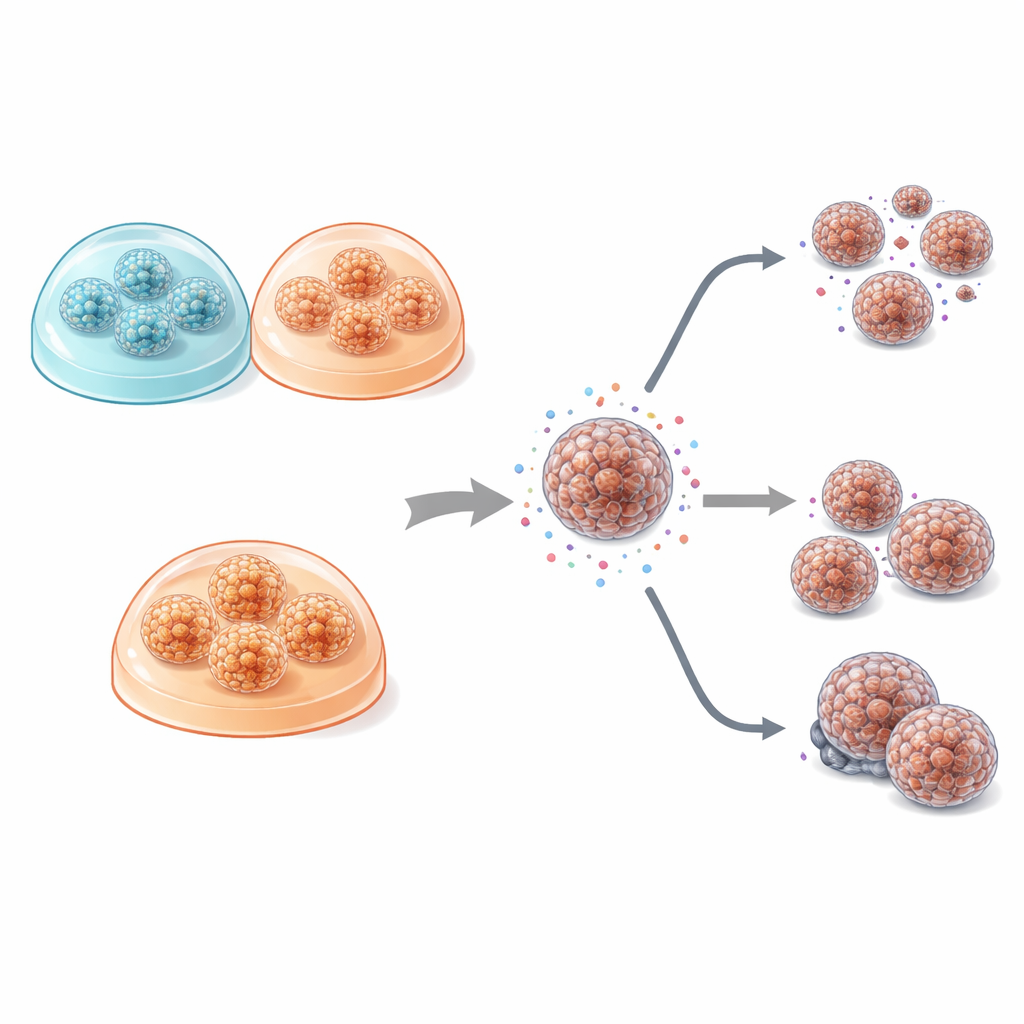
Что это означает для будущих тестов рака
Для непрофессионального читателя главный вывод ободряющий: результаты лабораторных тестов стандартных химиопрепаратов кажутся в большей степени зависящими от индивидуальной опухоли пациента, а не от того, выращивают ли клетки в плоском виде или как 3D скопления, и не от того, какой из распространенных гелей применяется. Это означает, что существующие лабораторные системы достаточно надежны для сравнения ответов опухолей пациентов на эти препараты. В то же время 3D органоиды лучше имитируют структуру и поведение настоящей опухоли, что делает их особенно полезными для изучения биологии болезни и, возможно, для сложных или таргетных терапий. В совокупности эти результаты поддерживают растущее использование органоидов, полученных от пациентов, как реалистичных, персонализированных тестовых платформ, которые однажды могут помочь врачам подбирать лечение для людей с раком поджелудочной железы.
Цитирование: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
Ключевые слова: рак поджелудочной железы, органыды, полученные от пациента, 3D клеточная культура, реакция на химиотерапию, лекарственная устойчивость