Clear Sky Science · es
Impacto de la dimensionalidad del cultivo y la composición de la matriz en la morfología, el fenotipo y la respuesta a fármacos en modelos de cáncer de páncreas
Por qué importa cultivar tumores de nuevas maneras
El cáncer de páncreas es uno de los más letales, en parte porque a menudo se detecta tarde y resiste muchos fármacos habituales. Para desarrollar mejores tratamientos, los investigadores utilizan células tumorales cultivadas en el laboratorio como sustitutos de los cánceres reales. Pero hay una cuestión básica detrás de este enfoque: ¿cambia la forma en que cultivamos estas células el modo en que se comportan y responden a los medicamentos? Este estudio explora si cultivar células tumorales pancreáticas en capas planas o en agregados tridimensionales, y en diferentes materiales tipo gel, modifica de verdad lo que aprendemos sobre la enfermedad y su tratamiento.
Del tumor del paciente a los modelos cultivados en el laboratorio
Los investigadores obtuvieron muestras tumorales de 12 pacientes con adenocarcinoma ductal pancreático, la forma más común de cáncer de páncreas. De cada tumor intentaron crear tres tipos de modelos de laboratorio: una capa clásica de células en una placa (cultivo 2D) y dos tipos de “mini‑tumores” tridimensionales, u organoides, cultivados en dos matrices comerciales en gel llamadas Matrigel y Cultrex. Estos geles imitan el material blando y rico en proteínas que rodea a las células en el organismo. El equipo también comprobó qué mutaciones genéticas estaban presentes para confirmar que estos modelos cultivados procedían realmente de células cancerosas y mantenían mutaciones conductoras bien conocidas. 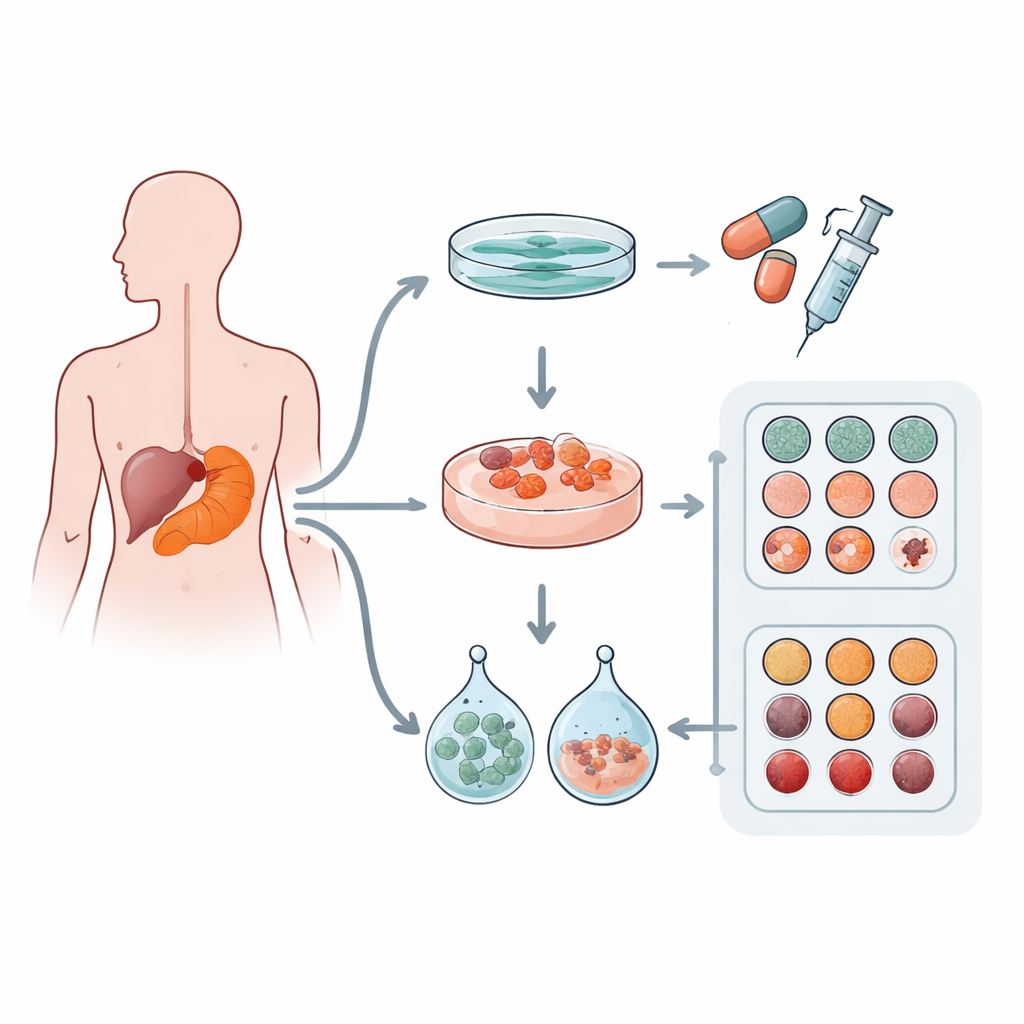
Cómo crecen y cómo se ven las células tumorales en el laboratorio
Al comparar el crecimiento, las diferencias entre los cultivos planos y los 3D fueron llamativas. En 2D, las células se extendían en láminas delgadas con poco agrupamiento, un patrón muy distante de la apariencia tumoral in vivo. En contraste, los organoides en gel 3D formaron esferas compactas o estructuras huecas similares a quistes que se asemejaban más a la arquitectura glandular de los tumores pancreáticos reales. Curiosamente, la forma exacta de estos organoides dependía más del tumor individual del paciente que del gel utilizado: los cánceres mejor diferenciados dieron lugar a organoides con aspecto glandular, mientras que un tumor más agresivo y pobremente diferenciado produjo agregados densos en forma de nido. En todas las condiciones, los cultivos 3D se dividieron más rápido y necesitaron menos tiempo antes de su primera división que los cultivos planos, lo que se reflejó en niveles superiores de su marcador de proliferación, Ki‑67.
Preservando la identidad del tumor
El equipo se preguntó luego si estas distintas formas de cultivo podían distorsionar la identidad básica de las células. Usando técnicas de tinción similares a las empleadas en laboratorios de patología hospitalaria, examinaron proteínas clave que definen los adenocarcinomas ductales pancreáticos. Marcadores como CK19 y GATA6, que señalan un tipo celular ductal, se conservaron tanto en sistemas 2D como 3D. Proteínas relacionadas con el perfil genético del tumor, incluidas p53 y SMAD4, mostraron patrones acordes con los tumores originales. Un marcador de la división celular, Ki‑67, fue más alto en todos los modelos de laboratorio que en el tejido original, reflejando las condiciones en el cultivo que favorecen el crecimiento. Otro marcador, CDX2, aumentó especialmente en los cultivos planos, lo que sugiere que algunos aspectos de la identidad celular pueden desplazarse en el laboratorio. En conjunto, sin embargo, tanto los enfoques 2D como 3D mantuvieron las características centrales de los cánceres de los pacientes.
Evaluando la quimioterapia en distintos mundos de laboratorio
El núcleo del estudio fue determinar si el formato de cultivo—plano frente a 3D, y la elección del gel—modifica la respuesta de las células tumorales a fármacos quimioterápicos habituales para el cáncer de páncreas, incluidos gemcitabina, 5‑fluorouracilo, oxaliplatino, SN‑38 y paclitaxel. En este pequeño grupo de pacientes, los patrones de sensibilidad a los fármacos fueron notablemente similares entre los cultivos 2D y ambos tipos de organoides. Los modelos tridimensionales tendieron a ser algo más resistentes a los fármacos, lo que concuerda con su estructura más parecida a un tumor y con una penetración de fármaco más limitada, pero estas diferencias fueron modestas y no estadísticamente contundentes. Lo que sí destacó fue la gran variación entre pacientes: para varios fármacos, especialmente gemcitabina, las células de algunos pacientes eran mucho más resistentes que las de otros, independientemente del formato de cultivo. En dos pacientes que recibieron gemcitabina tras la cirugía, los resultados de laboratorio reflejaron la realidad clínica: el paciente cuyos modelos eran más resistentes sufrió una recidiva más precoz, y sus cultivos mostraron niveles más altos de MDR1, una proteína conocida por expulsar fármacos de las células. 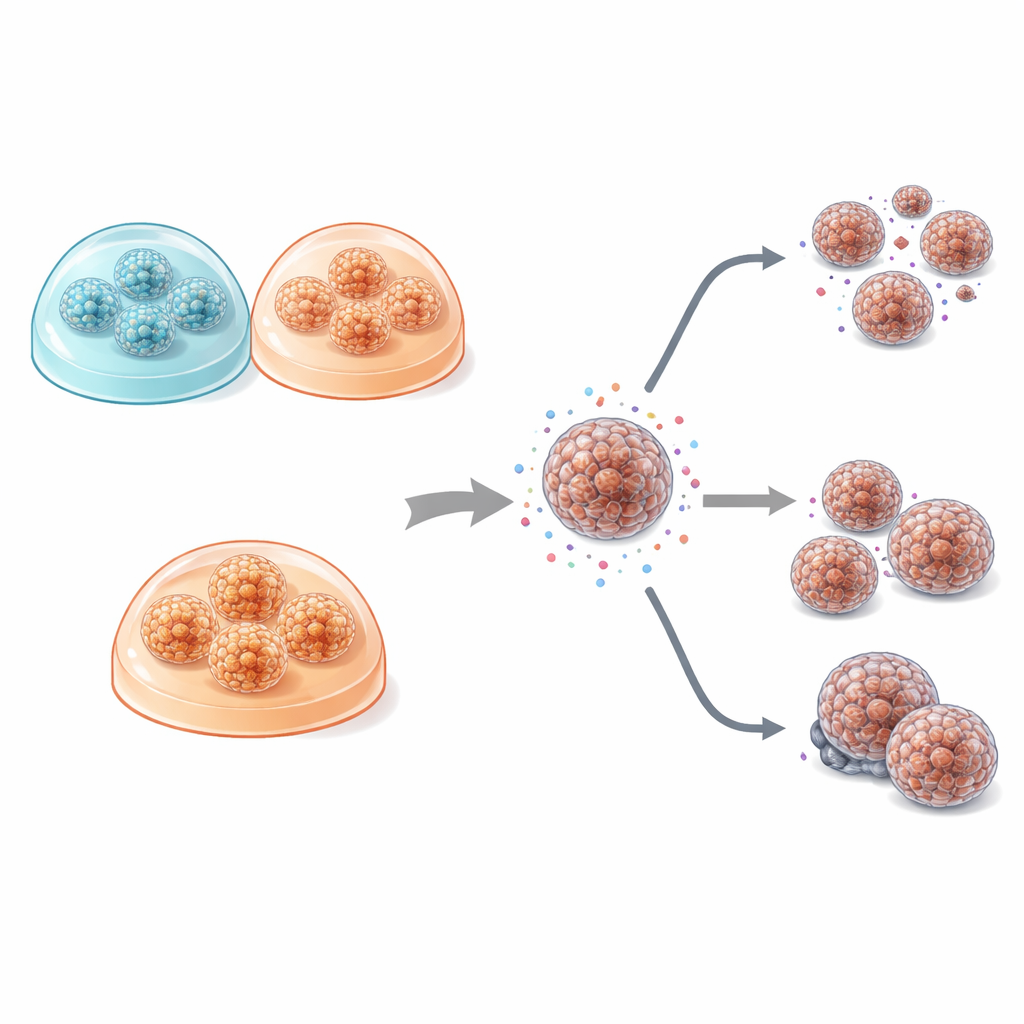
Qué significa esto para las pruebas futuras del cáncer
Para un lector general, la conclusión principal es tranquilizadora: el mensaje central obtenido de las pruebas de laboratorio con quimioterápicos estándar parece depender mucho más del tumor individual del paciente que de si las células se cultivan en plano o en racimos 3D, o de cuál de los geles comunes se utiliza. Eso implica que los sistemas de laboratorio existentes son razonablemente robustos para comparar cómo responden los tumores de distintos pacientes a estos fármacos. Al mismo tiempo, los organoides 3D imitan mejor la estructura y el comportamiento de crecimiento del tumor real, lo que los hace especialmente valiosos para estudiar la biología de la enfermedad y, posiblemente, para terapias más complejas o dirigidas. En conjunto, estos hallazgos respaldan el creciente uso de organoides derivados de pacientes como bancos de ensayo realistas y específicos de cada paciente que podrían, algún día, ayudar a los médicos a personalizar tratamientos para personas con cáncer de páncreas.
Cita: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
Palabras clave: cáncer de páncreas, organoides derivados de pacientes, cultivo celular 3D, respuesta a quimioterapia, resistencia a fármacos