Clear Sky Science · pl
Wpływ wymiarowości hodowli i składu matrycy na morfologię, fenotyp i odpowiedź na leki w modelach raka trzustki
Dlaczego nowe sposoby hodowli guzów mają znaczenie
Rak trzustki należy do najgroźniejszych nowotworów, częściowo dlatego, że często jest wykrywany późno i wykazuje oporność na wiele powszechnie stosowanych leków. Aby opracować lepsze terapie, badacze polegają na komórkach nowotworowych hodowanych w laboratorium jako modelach zastępujących prawdziwe guzy. Jednak kryje się za tym podstawowe pytanie: czy sposób, w jaki hodujemy te komórki, zmienia ich zachowanie i odpowiedź na leki? W tym badaniu sprawdzono, czy hodowla komórek raka trzustki w płaskich monowarstwach czy w trójwymiarowych skupiskach oraz w różnych żelopodobnych materiałach rzeczywiście wpływa na wnioski dotyczące choroby i jej leczenia.
Od guza pacjenta do modeli hodowanych w laboratorium
Badacze pobrali próbki guzów od 12 pacjentów z gruczolakorakiem przewodowym trzustki, najczęstszą postacią raka trzustki. Z każdego guza próbowali stworzyć trzy rodzaje modeli laboratoryjnych: klasyczną płaską warstwę komórek na szalce (hodowla 2D) oraz dwa typy trójwymiarowych „mini‑guzów”, czyli organoidów, hodowanych w różnych komercyjnych matrycach żelowych zwanych Matrigel i Cultrex. Te żele naśladują miękką, bogatobiałkową substancję otaczającą komórki w organizmie. Zespół sprawdził też obecność mutacji genetycznych, by potwierdzić, że modele pochodzą od komórek nowotworowych i zawierają znane mutacje sprawcze. 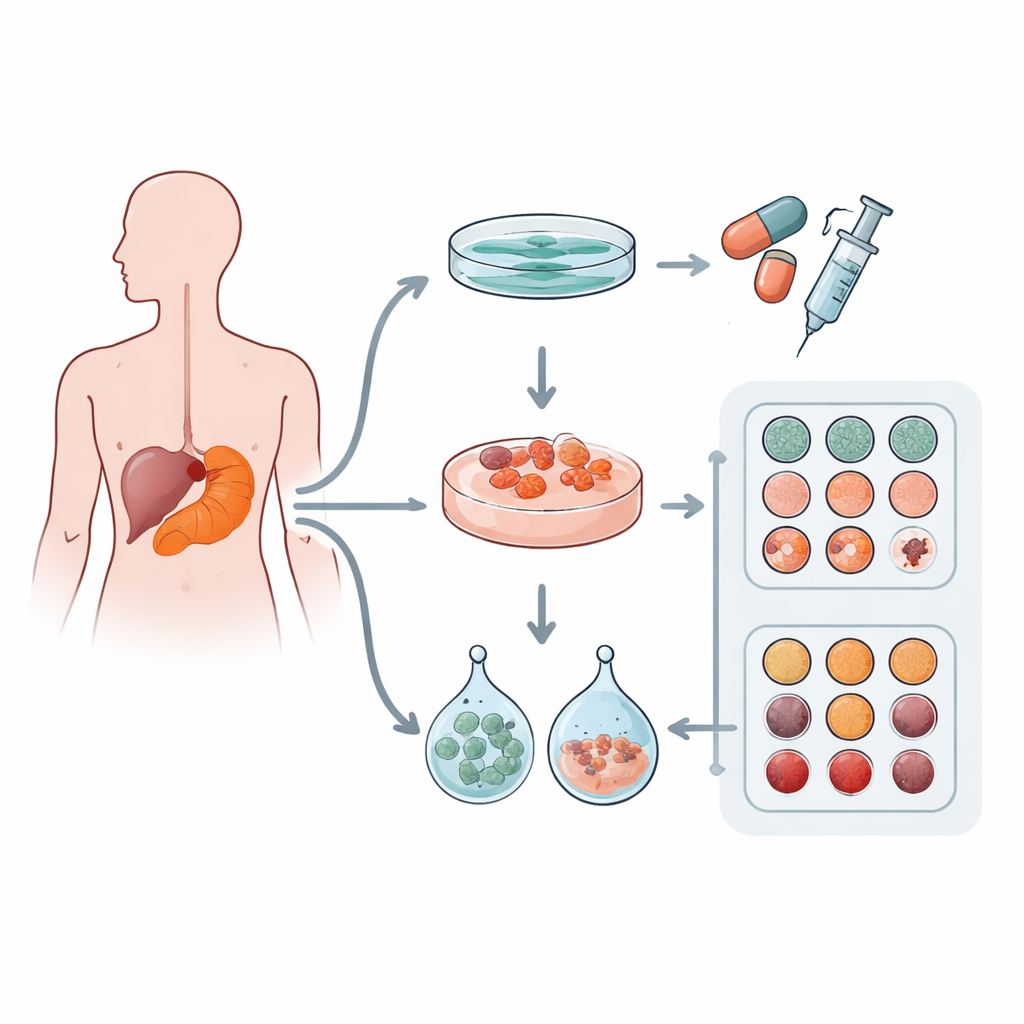
Jak komórki guza rosną i wyglądają w laboratorium
Porównanie wzrostu komórek ujawniło wyraźne różnice między hodowlami 2D a 3D. W 2D komórki rozkładały się w cienkie warstwy z niewielkim zagęszczeniem, co znacznie odbiega od wyglądu guzów w organizmie. Natomiast organoidy hodowane w żelach 3D tworzyły zwarte kule lub puste, torbielowate struktury, które bardziej przypominały gruczołową architekturę prawdziwych guzów trzustki. Co interesujące, dokładny kształt organoidów zależał bardziej od guza konkretnego pacjenta niż od użytego żelu: nowotwory lepiej zróżnicowane tworzyły struktury przypominające gruczoły, podczas gdy bardziej agresywny, słabo zróżnicowany guz dał gęste, gniazdowe skupiska. We wszystkich warunkach hodowle 3D dzieliły się szybciej i potrzebowały mniej czasu do pierwszego podziału niż hodowle płaskie, co odpowiada wyższym poziomom markera podziału komórkowego Ki‑67.
Utrzymanie tożsamości guza
Zespół sprawdził następnie, czy różne sposoby hodowli mogą zniekształcać podstawową tożsamość komórek. Przy użyciu barwień podobnych do tych stosowanych w patomorfologii szpitalnej badano kluczowe białka definiujące raka przewodowego trzustki. Markery takie jak CK19 i GATA6, sygnalizujące typ komórek przewodowych, były zachowane zarówno w systemach 2D, jak i 3D. Białka powiązane z profilem genetycznym guza, w tym p53 i SMAD4, wykazywały wzory zgodne z guzami pierwotnymi. Marker podziału komórek Ki‑67 był wyższy we wszystkich modelach laboratoryjnych niż w tkance wyjściowej, co odzwierciedla sprzyjające wzrostowi warunki hodowli. Inny marker, CDX2, wzrastał szczególnie w hodowlach płaskich, co sugeruje, że niektóre aspekty tożsamości komórek mogą się przesuwać w warunkach laboratoryjnych. Ogólnie jednak zarówno podejścia 2D, jak i 3D zachowały podstawowe cechy nowotworów pochodzących od pacjentów.
Testowanie chemioterapii w różnych światach laboratoryjnych
Głównym celem badania było sprawdzenie, czy format hodowli — płaski kontra 3D oraz wybór żelu — zmienia odpowiedź komórek guza na powszechnie stosowane leki chemioterapeutyczne w raku trzustki, w tym gemcytabinę, 5‑fluorouracyl, oksaliplatynę, SN‑38 i paklitaksel. W badanej niewielkiej grupie pacjentów wzorce wrażliwości na leki były zaskakująco podobne między hodowlami 2D a oboma typami organoidów. Modele trójwymiarowe miały tendencję do nieco większej oporności na leki, co odpowiada ich bardziej guzopodobnej strukturze i ograniczonemu przenikaniu leków, lecz różnice te były niewielkie i statystycznie słabe. Wyraźnie natomiast dawała się zauważyć duża zmienność odpowiedzi między pacjentami: dla kilku leków, zwłaszcza gemcytabiny, komórki od niektórych pacjentów były znacznie bardziej oporne niż od innych, niezależnie od sposobu hodowli. U dwóch pacjentów, którzy po operacji rzeczywiście otrzymali gemcytabinę, wyniki laboratoryjne odzwierciedliły przebieg kliniczny: pacjent, którego modele wykazywały większą oporność, nawrocił wcześniej, a jego hodowle wykazywały wyższe poziomy MDR1, białka znanego z usuwania leków z komórek. 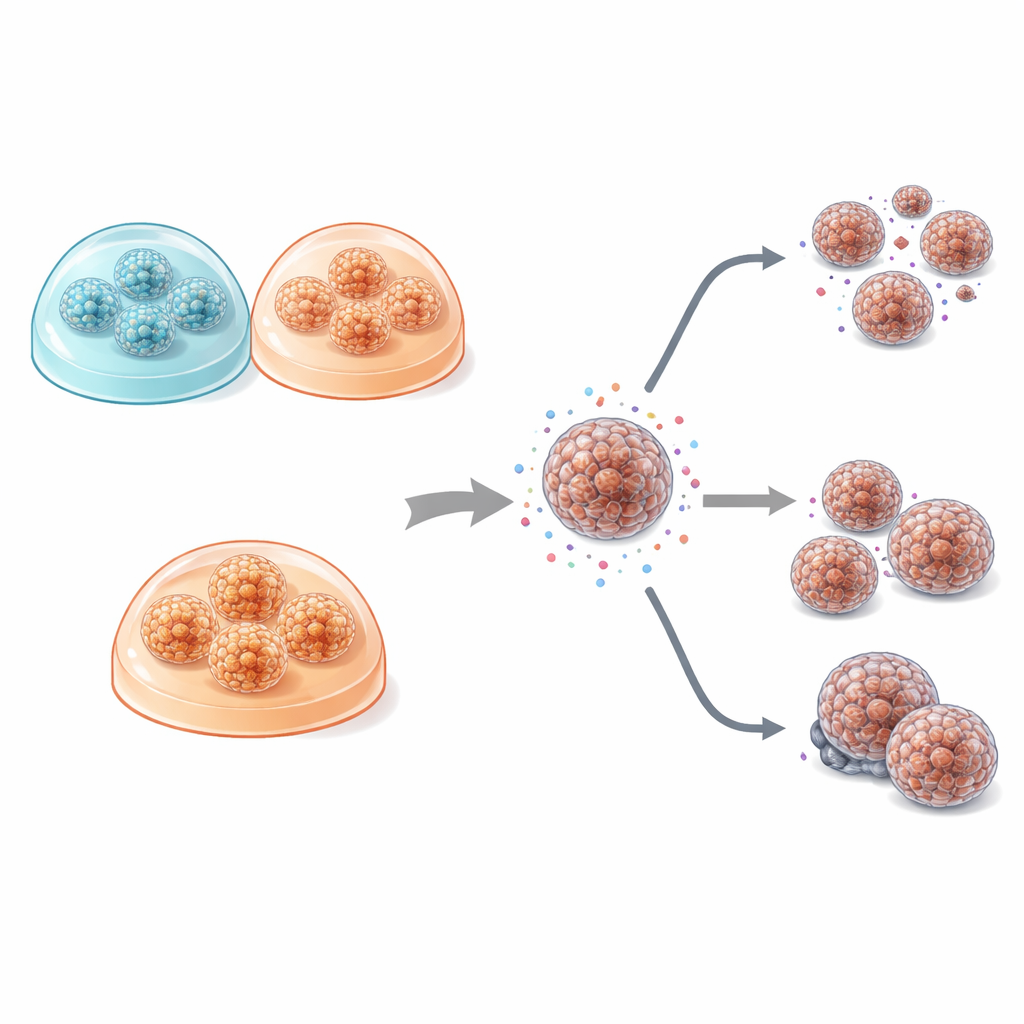
Co to oznacza dla przyszłych badań nad rakiem
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest pocieszający: główne informacje płynące z testów laboratoryjnych standardowych leków chemioterapeutycznych wydają się zależeć znacznie bardziej od indywidualnego guza pacjenta niż od tego, czy komórki są hodowane płasko czy jako skupiska 3D oraz od wyboru powszechnego żelu. Oznacza to, że istniejące systemy laboratoryjne są stosunkowo odporne jako narzędzia do porównywania odpowiedzi guzów pacjentów na te leki. Jednocześnie organoidy 3D lepiej naśladują rzeczywistą strukturę i zachowanie wzrostowe guza, co czyni je szczególnie cennymi do badania biologii choroby i potencjalnie do testów bardziej złożonych lub ukierunkowanych terapii. W świetle tych ustaleń użycie organoidów pochodzących od pacjentów jako realistycznych, specyficznych dla pacjenta platform testowych wydaje się rosnąć — mogą one w przyszłości pomóc lekarzom dostosowywać leczenie pacjentów z rakiem trzustki.
Cytowanie: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
Słowa kluczowe: rak trzustki, organoidy pochodzące od pacjentów, hodowla komórek 3D, odpowiedź na chemioterapię, oporność na leki