Clear Sky Science · de
Einfluss der Kultur‑Dimensionalität und der Matrixzusammensetzung auf Morphologie, Phänotyp und Medikamentenresponse in Pankreaskarzinom‑Modellen
Warum es wichtig ist, Tumoren auf neue Weise zu züchten
Pankreaskrebs zählt zu den tödlichsten Krebsarten, teilweise weil er häufig spät entdeckt wird und vielen gängigen Medikamenten widersteht. Um bessere Therapien zu entwickeln, nutzen Forschende im Labor gezüchtete Tumorzellen als Stellvertreter für echte Tumore. Dahinter steht jedoch eine grundlegende Frage: Verändert die Art, wie wir diese Zellen kultivieren, ihr Verhalten und ihre Reaktion auf Medikamente? Diese Studie untersucht, ob das Wachstum von Pankreastumorzellen in flachen Schichten oder in dreidimensionalen Verbänden und in unterschiedlichen gelartigen Matrizes tatsächlich beeinflusst, was wir über die Krankheit und ihre Behandlung lernen.
Vom Patiententumor zum im Labor gezüchteten Modell
Die Wissenschaftlerinnen und Wissenschaftler entnahmen Tumorproben von 12 Patientinnen und Patienten mit duktalem Adenokarzinom des Pankreas, der häufigsten Form von Pankreaskrebs. Aus jedem Tumor versuchten sie, drei Modelltypen zu etablieren: eine klassische flache Zellschicht in einer Schale (2D‑Kultur) sowie zwei Arten von dreidimensionalen „Mini‑Tumoren“ oder Organoiden, die in unterschiedlichen kommerziellen Gelmatrices, Matrigel und Cultrex, gezüchtet wurden. Diese Gele ahmen das weiche, proteinreiche Material nach, das Zellen im Körper umgibt. Das Team prüfte außerdem die vorhandenen genetischen Veränderungen, um zu bestätigen, dass die im Labor gezüchteten Modelle tatsächlich von Krebszellen stammen und bekannte Treibermutationen tragen. 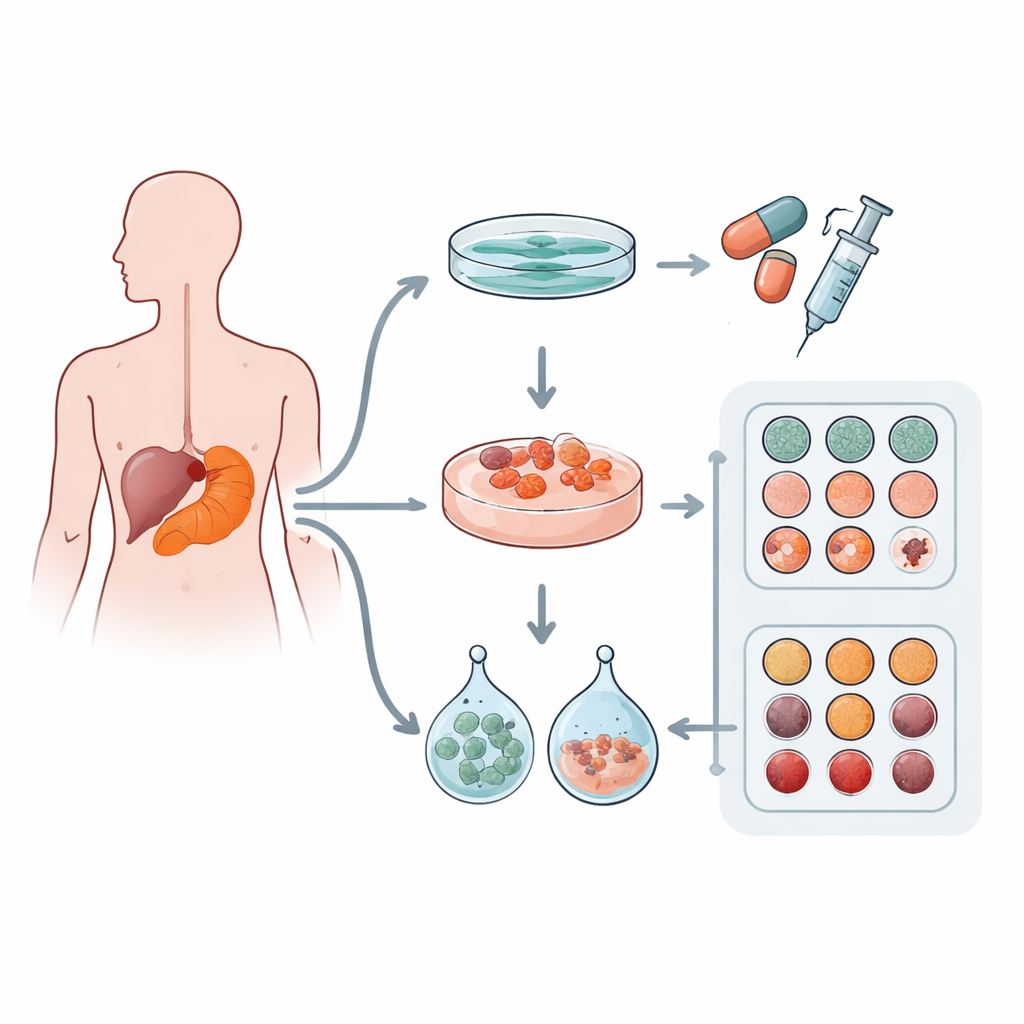
Wie Tumorzellen im Labor wachsen und aussehen
Beim Vergleich des Zellwachstums zeigten sich deutliche Unterschiede zwischen flachen und 3D‑Kulturen. In 2D breiteten sich die Zellen als dünne Schichten mit wenig Clusterbildung aus — ein Muster, das weit von der Erscheinung von Tumoren im Körper entfernt ist. Im Gegensatz dazu bildeten in 3D‑Gelen gezüchtete Organoide kompakte Kugeln oder hohle, zystenartige Strukturen, die der drüsenartigen Architektur echter Pankreastumore näher kamen. Interessanterweise hing die genaue Form dieser Organoide stärker vom Tumor der jeweiligen Patientin oder des jeweiligen Patienten ab als von der verwendeten Gelmatrix: besser differenzierte Tumore bildeten drüsenähnliche Organoide, während ein aggressiver, schlecht differenzierter Tumor dichte, nestartige Verbände hervorbrachte. Unter den Bedingungen teilten sich 3D‑Kulturen schneller und benötigten weniger Zeit bis zur ersten Zellteilung als die flachen Kulturen, was sich auch in höheren Werten des Proliferationsmarkers Ki‑67 widerspiegelte.
Die Identität des Tumors bewahren
Das Team fragte weiter, ob diese unterschiedlichen Kulturmethoden die grundlegende Identität der Zellen verzerren könnten. Mit Färbeverfahren, wie sie in pathologischen Labors angewandt werden, untersuchten sie Schlüssleproteine, die duktale Pankreastumoren charakterisieren. Marker wie CK19 und GATA6, die auf einen duktalen Zelltyp hinweisen, blieben sowohl in flachen als auch in 3D‑Systemen erhalten. Proteine, die mit der genetischen Ausstattung des Tumors verknüpft sind, darunter p53 und SMAD4, zeigten Muster, die mit den Originaltumoren übereinstimmten. Der Teilungsmarker Ki‑67 war in allen Labormodellen höher als im Ausgangsgewebe, was die wachstumsfördernden Bedingungen in Kultur widerspiegelt. Ein weiterer Marker, CDX2, stieg insbesondere in den 2D‑Kulturen an, was darauf hindeutet, dass sich manche Aspekte der Zellidentität im Labor verschieben können. Insgesamt bewahrten jedoch sowohl 2D‑ als auch 3D‑Ansätze die Kernmerkmale der Tumore der Patientinnen und Patienten.
Chemotherapie testen in unterschiedlichen Laborwelten
Der Kern der Studie bestand darin zu prüfen, ob das Kulturformat — flach versus 3D und die Wahl der Gelmatrix — die Reaktion der Tumorzellen auf gängige Chemotherapeutika verändert, die beim Pankreaskrebs eingesetzt werden, darunter Gemcitabin, 5‑Fluorouracil, Oxaliplatin, SN‑38 und Paclitaxel. Im untersuchten Patientenkollektiv waren die Muster der Arzneimittelempfindlichkeit zwischen 2D‑Kulturen und beiden Organoidtypen bemerkenswert ähnlich. 3D‑Modelle zeigten tendenziell eine etwas höhere Medikamentenresistenz, was mit ihrer tumorähnlicheren Struktur und der eingeschränkteren Wirkstoffpenetration übereinstimmt, doch diese Unterschiede waren gering und statistisch nicht stark. Auffällig war hingegen die große interindividuelle Variabilität: Bei mehreren Wirkstoffen, insbesondere Gemcitabin, waren die Zellen mancher Patientinnen und Patienten deutlich resistenter als die anderer, unabhängig von der Kultivierungsart. Bei zwei Patientinnen bzw. Patienten, die nach der Operation tatsächlich Gemcitabin erhielten, spiegelten die Laborbefunde die klinische Realität wider: Der Patient mit resistenteren Modellen erlitt schneller ein Rezidiv, und seine Kulturen zeigten höhere Werte von MDR1, einem Protein, das bekanntlich Arzneimittel aus Zellen herauspumpt. 
Folgen für die künftige Krebsdiagnostik
Für eine breitere Leserschaft ist die wichtigste Erkenntnis beruhigend: Die zentralen Aussagen aus Labortests mit Standard‑Chemotherapeutika scheinen sich weit stärker an den Eigenschaften des individuellen Tumors zu orientieren als daran, ob die Zellen flach oder als 3D‑Verbände wachsen oder welches der gängigen Gele verwendet wird. Das deutet darauf hin, dass bestehende Laborsysteme für den Vergleich der Medikamentenreaktionen von Patiententumoren recht robust sind. Zugleich ahmen 3D‑Organoide die Struktur und das Wachstumsverhalten realer Tumore besser nach, was sie besonders wertvoll für die Untersuchung der Krankheitsbiologie und möglicherweise für komplexere oder zielgerichtete Therapien macht. Zusammengenommen stützen diese Ergebnisse die zunehmende Verwendung patientenabgeleiteter Organoide als realistische, patientenspezifische Testplattformen, die eines Tages Ärzten helfen könnten, Behandlungen für Menschen mit Pankreaskrebs individueller zu gestalten.
Zitation: Doelvers, F., Wansch, K., Kuehn, A. et al. Impact of culture dimensionality and matrix composition on morphology, phenotype and drug response in pancreatic cancer models. Sci Rep 16, 12346 (2026). https://doi.org/10.1038/s41598-026-47856-1
Schlüsselwörter: Pankreaskrebs, patientenabgeleitete Organoide, 3D‑Zellkultur, Chemotherapie‑Response, Medikamentenresistenz