Clear Sky Science · zh
用于多中心检测胰腺癌淋巴结转移的联邦CT基础模型
这对患者意味着什么
胰腺癌是最致命的癌症之一,部分原因在于常常发现较晚且已扩散到邻近淋巴结。术前判断是否发生转移至关重要:它决定了手术的激进程度以及患者是否应先接受化疗。然而,目前由专家解读的CT扫描仍漏诊许多隐匿的转移。本研究探讨了新一代大型医学AI模型的潜力,这些模型在不共享原始患者数据的前提下由多家医院协作训练,能否使这些影响生命的决策更准确、更公平。
一种难缠的癌症与影像学的盲点
大多数胰腺癌属于胰腺导管腺癌,这类癌症以生存率低著称。疾病严重的一个关键迹象是胰腺周围淋巴结的转移。放射科医生通常通过观察淋巴结的大小和形态在CT上识别这种转移。不幸的是,这些视觉线索并不可靠:许多存在微观转移的患者在CT上看起来“正常”,不同专家之间也常有分歧。因此,肿瘤可能被低估,一些患者可能无法获得他们实际上需要的强化治疗。
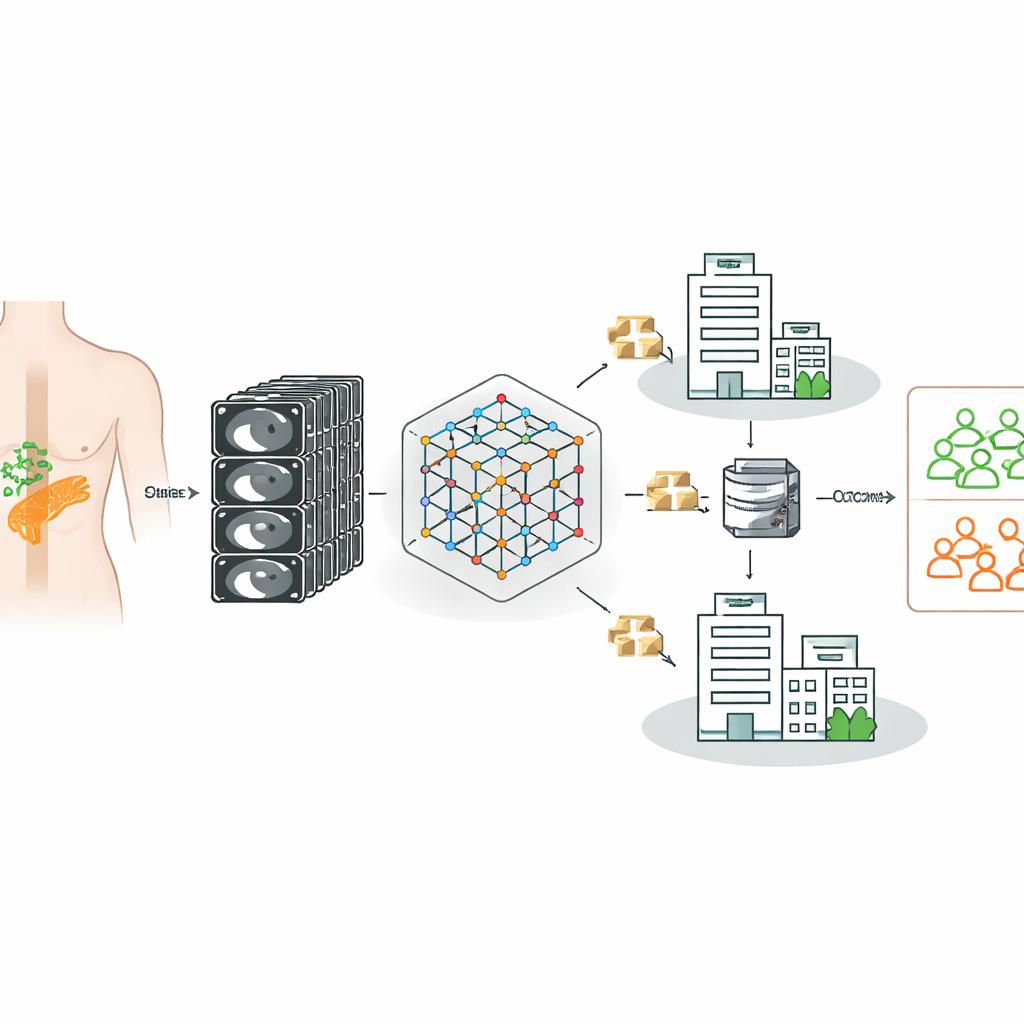
教会CT模型从多家医院学习
研究者基于一个强大的CT“基础模型”——该AI系统最初在148,000例CT扫描上训练,以识别三维解剖学中的通用模式。随后,他们对该模型进行了微调,使其能够对每位胰腺癌患者判断淋巴结是否真实转移,采用手术和病理确认结果作为真实标签。值得注意的是,数据来自三家使用不同扫描仪、成像协议和患者群体的德国医院,反映了临床实践中混杂多变的真实情况,而非单一精心筛选的数据集。
在不共享患者数据的情况下协作
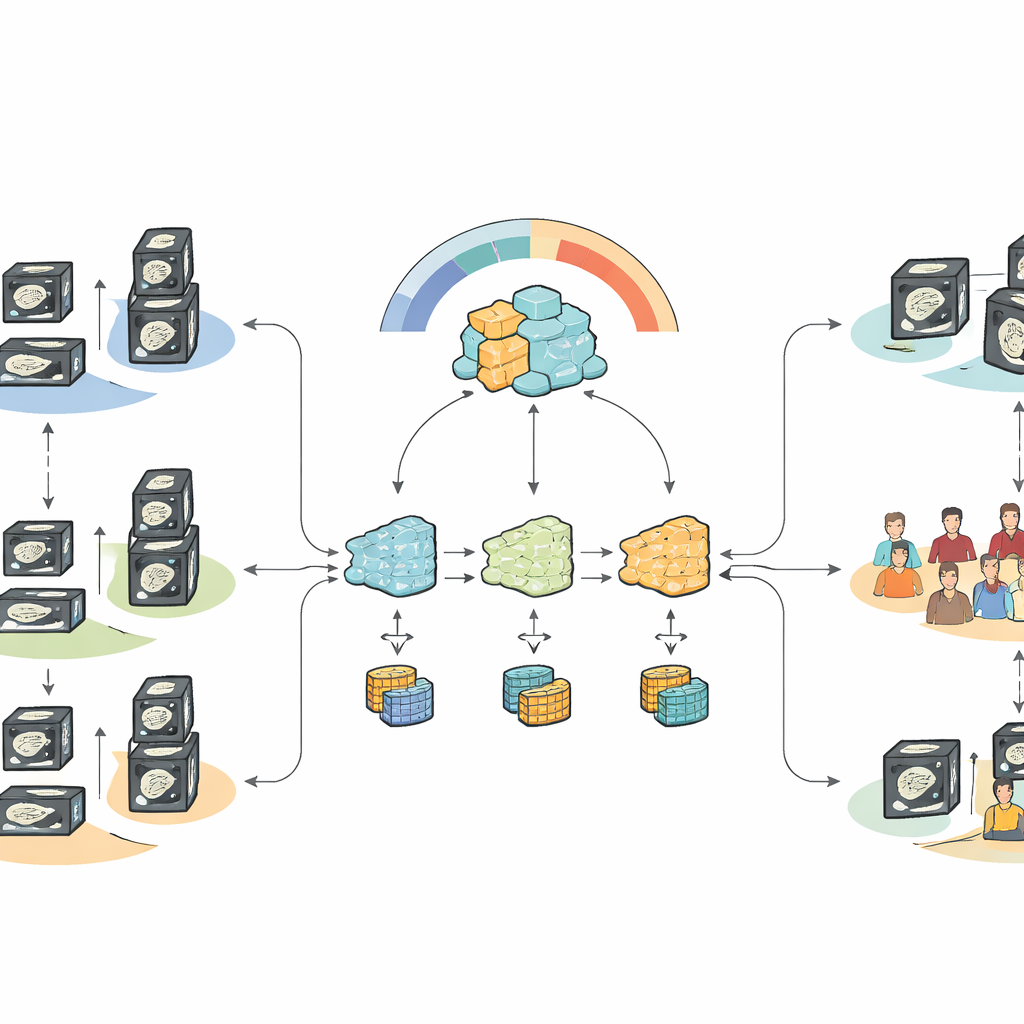
由于严格的隐私规定阻止医院自由集中患者影像,团队转向了联邦学习。在这种方法中,共同的模型被发送到每家医院,在当地数据上进行训练,然后仅使用模型学到的参数进行集中更新,影像本身从不被共享。然而,标准的联邦方法假定所有站点相似,而在医学中很少如此:设备、造影时机和患者构成的差异会使本地模型朝相互冲突的方向发展,当这些更新被简单平均时会降低性能。
一种更聪明的医院间知识融合方式
为了解决这一问题,作者设计了一种“异质性感知”的更新合并方式。他们的方法不仅考虑每个站点标签的失衡程度(有多少患者存在或不存在转移),还评估每家医院学到的决策边界与公共模型的差异。那些与共享模式偏离过大的客户端在合并更新时被降低权重。这个基于表征的策略在稳定训练的同时仍允许系统学习每家医院的独特经验,从而得到一个更能区分有无淋巴结扩散患者的全局模型。
对真实世界护理的启示
在所有数据被集中处理的情形下——通常会被隐私法规阻止——微调后的基础模型明显优于传统机器学习技术和早期的胰腺模型,在区分转移与非转移病例上表现更好。在保留隐私的联邦条件下,这种新的异质性感知方法恢复了大部分性能,并优于那些要么过度预测要么低估转移的标准联邦方法。该系统在敏感性方面尤为出色——能够捕捉到有淋巴结转移的患者——同时实现了适中但改进的特异性,这种权衡符合临床上优先避免漏诊的原则,即便这会带来一些误报。
对未来的意义
对普通读者来说,核心信息是:现在可以在不移动散落于多家医院的敏感影像数据的情况下训练强大的AI,仍然能改善医生判断胰腺癌是否已扩散至淋巴结的能力。这项工作表明,从广泛的CT基础模型出发,并采用一种更聪明的方式融合来自不同医院的知识,比旧方法能产生更可靠、更具临床意义的预测。尽管该工具尚未完美——尤其是在避免假阳性方面仍有改进空间——但它代表了朝向为直面这一最具挑战性的癌症之一的外科医生和肿瘤科医生提供更安全、更一致决策支持的有希望一步。
引用: Bhalla, P., Gaviria, D.D., Kupczyk, P. et al. Federated CT foundation models for multi-center detection of lymph node metastasis in pancreatic cancer. Sci Rep 16, 12051 (2026). https://doi.org/10.1038/s41598-026-47631-2
关键词: 胰腺癌, 淋巴结转移, CT成像, 医学人工智能, 联邦学习