Clear Sky Science · sv
Federerade CT-foundationmodeller för multicenterdetektion av lymfkörtelmetastaser vid bukspottkörtelcancer
Varför detta är viktigt för patienter
Bukspottkörtelcancer är en av de dödligaste cancerformerna, delvis eftersom den ofta upptäcks sent och redan har spridit sig till närliggande lymfkörtlar. Att veta om denna spridning har skett före operation är avgörande: det styr hur aggressivt ingreppet bör vara och om patienten bör få cytostatika först. Trots detta missar dagens CT‑undersökningar, även när de tolkas av experter, många av dessa dolda metastaser. Denna studie undersöker hur en ny generation av stora medicinska AI‑modeller, tränade gemensamt över sjukhus utan att dela råa patientdata, skulle kunna göra dessa livsavgörande beslut mer precisa och mer rättvisa.
En svår cancer och en blind fläck i bilddiagnostiken
De flesta bukspottkörtelcancerfall tillhör typen pankreascancer (pancreatic ductal adenocarcinoma), känd för sin dåliga överlevnad. Ett viktigt tecken på att sjukdomen är allvarlig är spridning till lymfkörtlar nära bukspottkörteln. Radiologer försöker upptäcka denna spridning på CT‑bilder, vanligtvis genom att bedöma lymfkörtlarnas storlek och form. Tyvärr är dessa visuella ledtrådar opålitliga: många patienter med mikroskopisk spridning ser “normala” ut på CT, och olika experter kan ofta vara oense. Som resultat kan tumörer underskattas och vissa patienter får inte den intensiva behandling de egentligen behöver.
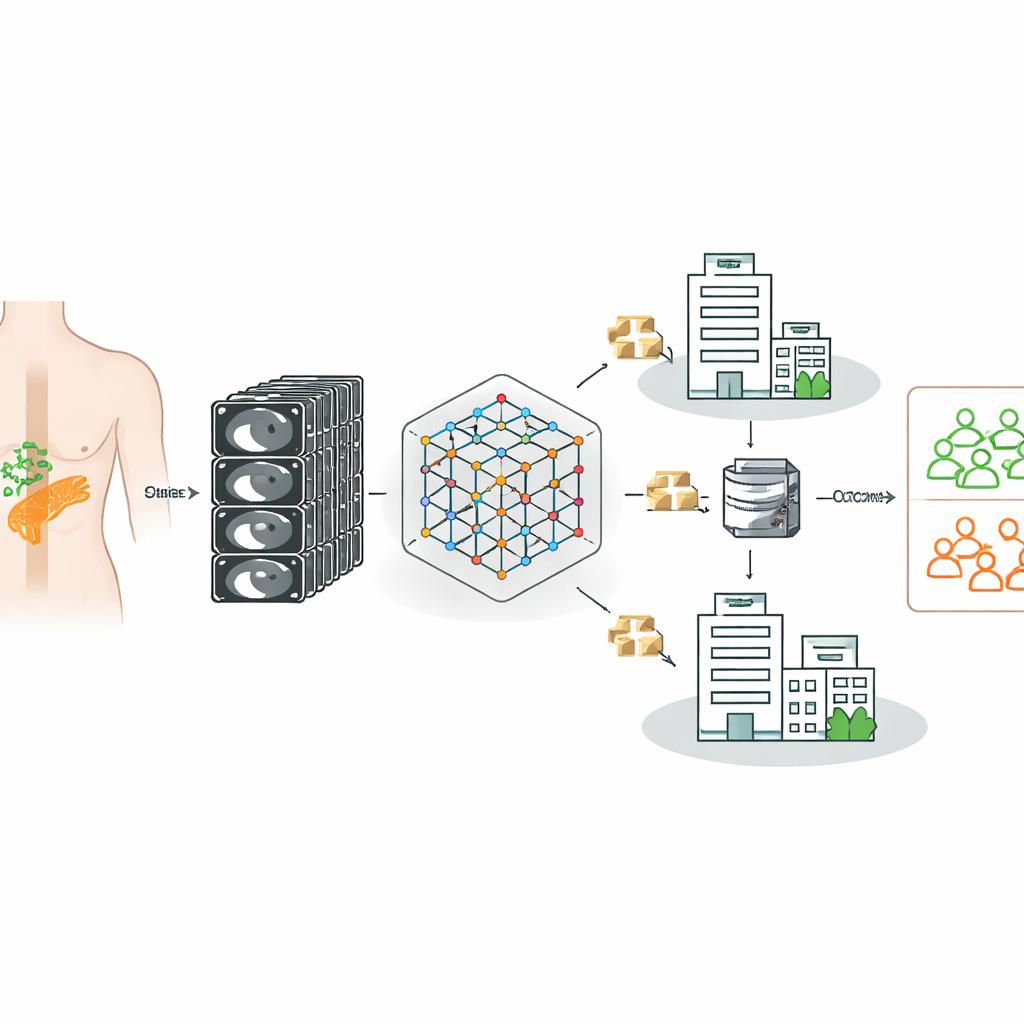
Att lära en CT‑modell från många sjukhus
Forskarna byggde vidare på en kraftfull “foundation‑modell” för CT‑avbildning—ett AI‑system som först tränades på 148 000 CT‑undersökningar för att känna igen generella mönster i tredimensionell anatomi. De finjusterade sedan modellen för att avgöra, för varje patient med bukspottkörtelcancer, om lymfkörtlar verkligen var metastatiska, med bekräftade kirurgiska och patologiska resultat som sanning. Viktigt är att data kom från tre tyska sjukhus med olika skannrar, avbildningsprotokoll och patientpopulationer, vilket speglar klinisk verklighet snarare än en enda, noggrant kurerad datamängd.
Samarbete utan att dela patientdata
Eftersom strikta sekretessregler hindrar sjukhus från att fritt slå samman patientskanningar använde teamet federerat lärande. I detta tillvägagångssätt skickas en gemensam modell till varje sjukhus, tränas lokalt på det sjukhusets data och uppdateras sedan centralt med endast modellens inlärda parametrar, aldrig bilderna själva. Standardmetoder för federerat lärande antar dock att alla platser är likartade. I medicin är detta sällan fallet: skillnader i maskiner, kontrasttiming och patientmix kan dra lokala modeller åt motsatta håll och försämra prestanda om uppdateringarna bara medelvärderas.
Ett smartare sätt att kombinera sjukhusens lärdomar
För att hantera detta utformade författarna en “heterogenitetsmedveten” metod för att kombinera uppdateringar från varje sjukhus. Deras metod beaktar inte bara hur obalanserade varje sites etiketter är (hur många patienter som har eller inte har metastaser) utan också hur olika varje sjukhus inlärda beslutgräns är från den gemensamma modellen. Klienter vars modeller avviker för mycket från det delade mönstret nedvägs när uppdateringarna slås samman. Denna representationmedvetna strategi stabiliserar träningen samtidigt som systemet får lära av varje sjukhus unika erfarenheter, vilket ger en global modell som bättre separerar patienter med respektive utan lymfkörtelspridning.
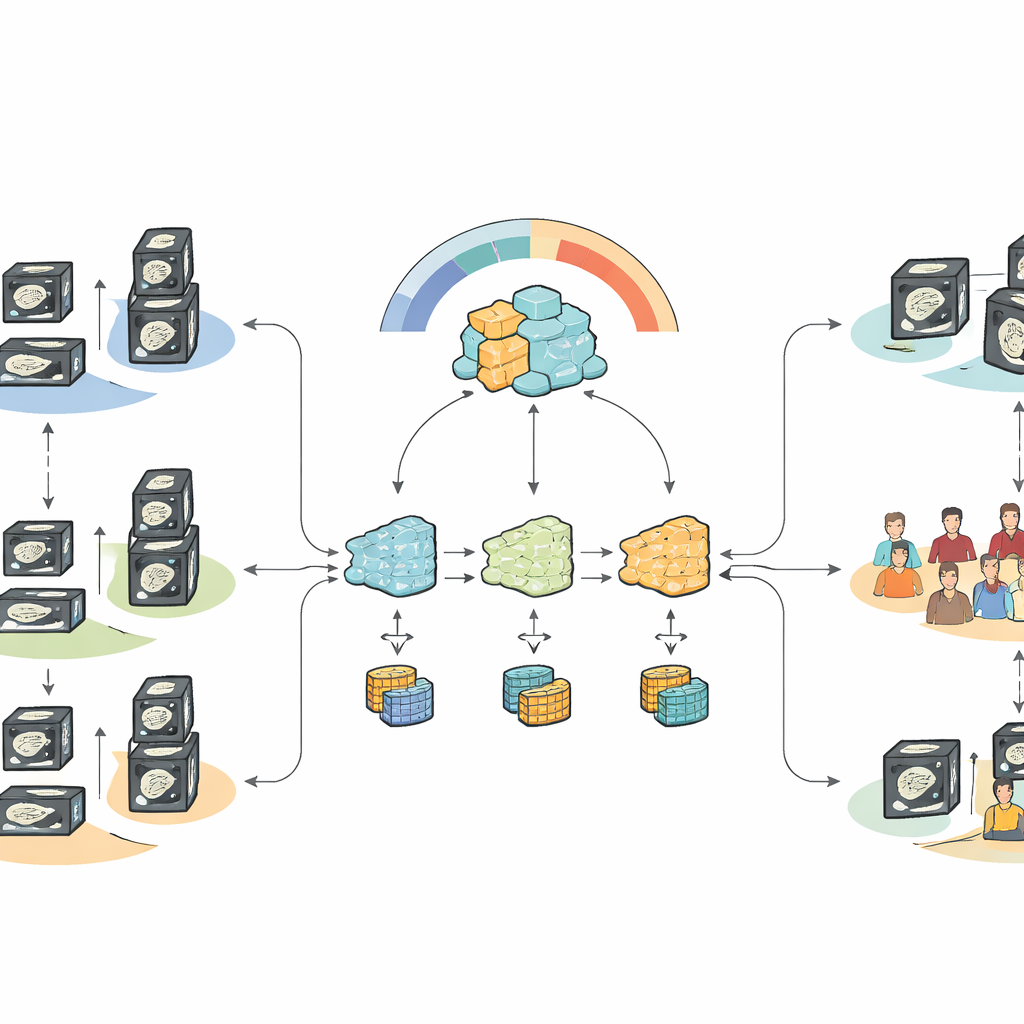
Vad resultaten visar för vård i verkligheten
När all data poolades centralt—ett scenario som normalt skulle blockeras av sekretessregler—överträffade den finjusterade foundation‑modellen tydligt traditionella maskininlärningstekniker och tidigare pankreasmodeller när det gällde att skilja metastatiska från icke‑metastatiska fall. Under federerade, sekretessbevarande förhållanden återvann den nya heterogenitetsmedvetna metoden det mesta av den prestandan och överträffade standardiserade federerade metoder som antingen överpredikterade eller underpredikterade metastas. Systemet var särskilt bra på känslighet—att hitta patienter med lymfkörtelspridning—samtidigt som det uppnådde måttlig men förbättrad specificitet, en avvägning som matchar det kliniska prioritetet att undvika missad sjukdom även på bekostnad av vissa falska larm.
Vad detta betyder framöver
För en lekmannaläsare är huvudbudskapet att kraftfull AI nu kan tränas på känsliga skanningar spridda över många sjukhus utan att flytta data, och ändå förbättra hur läkare bedömer om bukspottkörtelcancer har spridit sig till lymfkörtlar. Detta arbete visar att utgångspunkt i en bred CT‑foundationmodell och användning av ett smartare sätt att blanda kunskap från olika sjukhus ger mer tillförlitliga, kliniskt meningsfulla förutsägelser än äldre metoder. Även om verktyget ännu inte är perfekt—särskilt när det gäller att undvika falskt positiva resultat—är det ett lovande steg mot säkrare, mer konsekventa beslutsstöd för kirurger och onkologer som står inför en av de mest utmanande cancerformerna.
Citering: Bhalla, P., Gaviria, D.D., Kupczyk, P. et al. Federated CT foundation models for multi-center detection of lymph node metastasis in pancreatic cancer. Sci Rep 16, 12051 (2026). https://doi.org/10.1038/s41598-026-47631-2
Nyckelord: bukspottkörtelcancer, lymfkörtelmetastaser, CT-avbildning, medicinsk AI, federerat lärande