Clear Sky Science · he
דגמי יסוד לפיתוח מבוססי CT בפדרציה לזיהוי גרורות בבלוטות לימפה בסרטן הלבלב במספר מרכזים
מדוע זה חשוב עבור מטופלים
סרטן הלבלב הוא אחד הסרטנים הקטלניים ביותר, בין השאר כי הוא מתגלה לעתים קרובות בשלב מאוחר וכבר התפשט לבלוטות לימפה סמוכות. ידיעה האם התפשטות זו אירעה לפני הניתוח היא מכרעת: היא מנחה עד כמה הניתוח צריך להיות תוקפני והאם יש להעניק קודם כימותרפיה. עם זאת, סריקות CT כיום, שמפורשות על ידי מומחים, מפספסות רבות מהגרורות הבלתי נראות הללו. המחקר הזה בוחן כיצד דור חדש של דגמי בינה מלאכותית רפואיים רחבי גבולות, המאומנים בשיתוף בין בתי חולים מבלי לשתף נתוני מטופלים גולמיים, יכול לשפר את הדיוק וההוגנות בהחלטות שמשפיעות על החיים.
סרטן קשה ונקודת עיוורון בהדמיה
רוב מקרי סרטן הלבלב הם מסוג שנקרא אדנוקרצינומה של צינורות הלבלב, הידוע בתוצאת השרידות החלשה שלו. סימן מרכזי לכך שהמחלה חמורה הוא התפשטות לבלוטות לימפה בקרבת הלבלב. רדיולוגים מנסים לזהות תפשטות זו בסריקות CT, לרוב על‑ידי בדיקת גודל וצורה של הבלוטות. לצערנו, רמזים ויזואליים אלה אינם אמינים: רבים מהמטופלים עם התפשטות מיקרוסקופית נראים "נורמליים" ב‑CT, ומומחים שונים לעתים קרובות אינם מסכימים. כתוצאה מכך, הגידולים עלולים להיות מוערכים בחסר, וחלק מהמטופלים לא יקבלו את הטיפול האינטנסיבי שהם זקוקים לו בפועל.
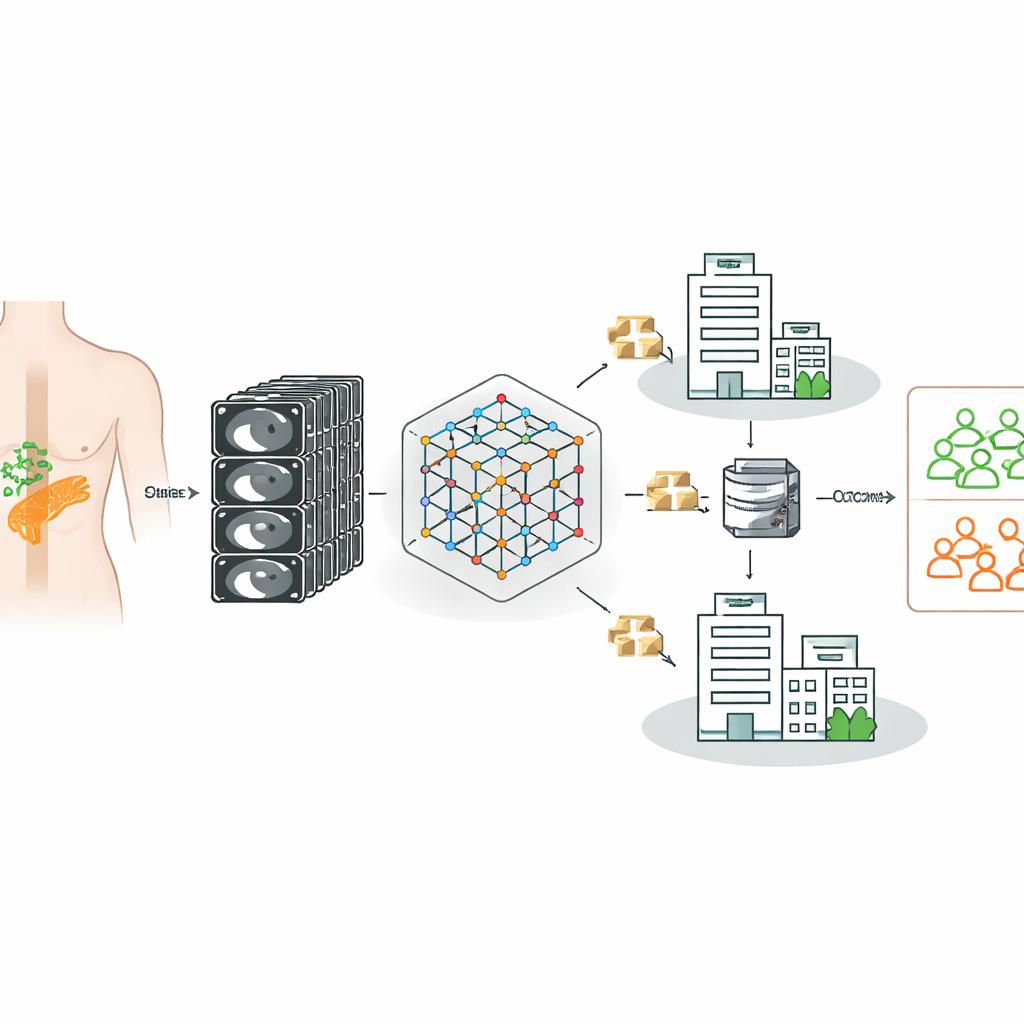
להדריך מודל CT ללמוד מבתי חולים רבים
החוקרים בנו על "מודל יסוד" עוצמתי להדמיית CT — מערכת בינה מלאכותית שאומנה תחילה על 148,000 סריקות CT כדי לזהות דפוסים כלליים באנטומיה תלת־ממדית. אחר כך הלבישו את המודל כדי להכריע, עבור כל מטופל עם סרטן הלבלב, האם הבלוטות הלימפתיות אכן גרומתיות, תוך שימוש בתוצאות כירורגיות ופאתולוגיות מאומתות כעובדת יסוד. באופן חשוב, הנתונים הגיעו משלושה בתי חולים בגרמניה עם סורקים, פרוטוקולי הדמיה ואוכלוסיות מטופלים שונים, מה שמשקף את המציאות המורכבת של הפרקטיקה הקלינית במקום מערך נתונים אחד ומסודר בקפידה.
שיתוף פעולה ללא שיתוף נתוני מטופלים
בגלל כללי פרטיות מחמירים שמונעים מבתי חולים לאגד בחופשיות סריקות של מטופלים, הצוות פנה ללמידה פדרטיבית. בגישה זו, מודל משותף נשלח לכל בית חולים, מאומן באופן מקומי על נתוני אותו בית חולים, ואז מעודכן באופן מרכזי תוך שימוש רק בפרמטרים של המודל שנלמדו, לעולם לא בתמונות עצמן. שיטות פדרטיביות סטנדרטיות מניחות עם זאת שכל האתרים דומים. ברפואה זה נדיר: הבדלים במכונות, בתזמון החומר הניגוד ובמאגרי המטופלים עלולים למשוך את המודלים המקומיים לכיוונים מנוגדים, מה שמחליש את הביצועים כאשר העדכונים מאוזנים פשוט על‑ידי ממוצע.
דרך חכמה יותר לשלב את מה שלמדו בתי החולים
כדי להתמודד עם זאת, המחברים תכננו דרך "מודעת הטרוגניות" לשילוב העדכונים מכל בית חולים. שיטתهم מתבוננת לא רק באיזון התוויות בכל אתר (כמה מטופלים יש או אין להם גרורות) אלא גם עד כמה גבול ההכרעה שנלמד בכל בית חולים שונה מהמודל המשותף. לקוחות שמודלים שלהם סוטים רחוק מדי מהתבנית המשותפת מוזלים במשקלם בעת מיזוג העדכונים. אסטרטגיה זו המודעת לייצוג מייצבת את האימון בעוד היא עדיין מאפשרת למערכת ללמוד מהניסיון הייחודי של כל בית חולים, ובכך מניבה מודל גלובלי שמפריד טוב יותר בין מטופלים עם ופחות התפשטות לבלוטות לימפה.
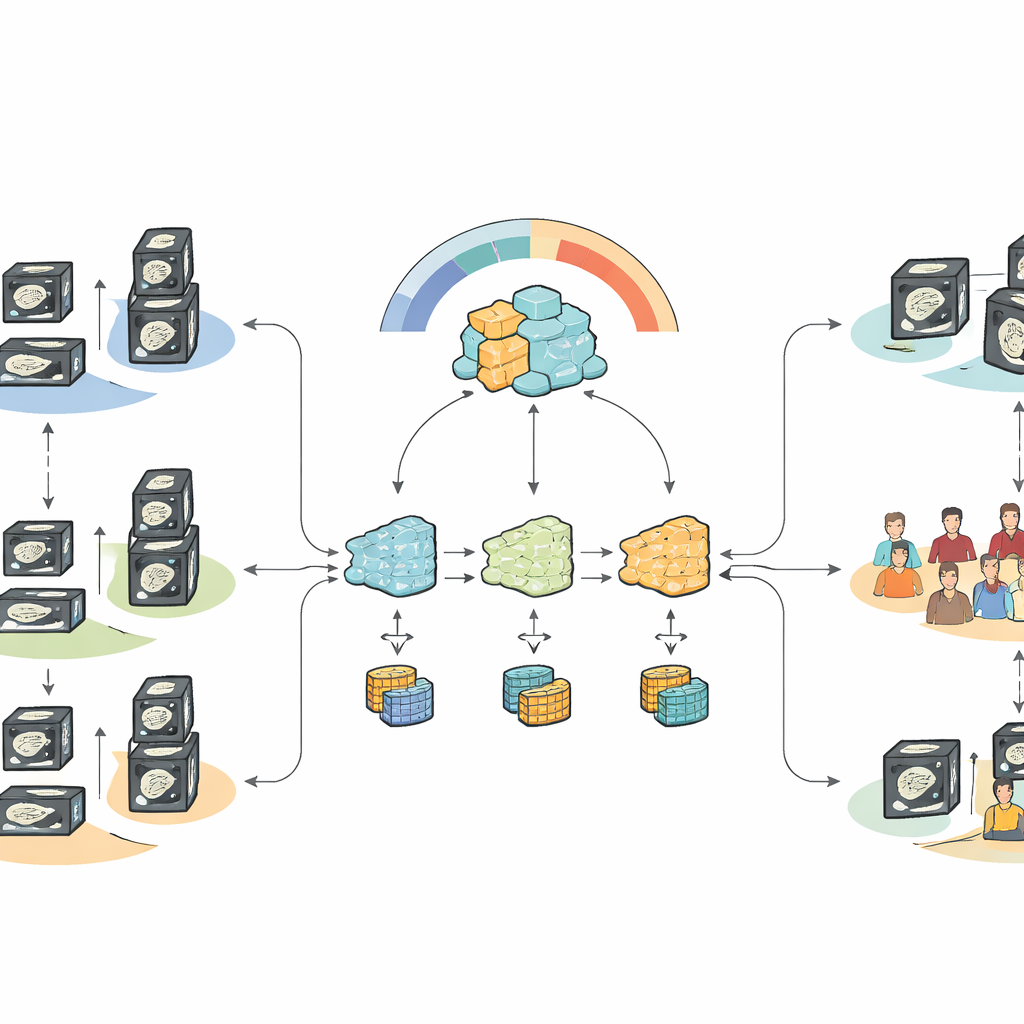
מה התוצאות מראות עבור טיפול בעולם האמיתי
כאשר כל הנתונים אוחדו מרכזית — תרחיש שלרוב היה נחסם על‑ידי תקנות פרטיות — המודל המותאם היטב מבוסס היסוד גבר בבירור על טכניקות למידת מכונה מסורתיות ודגמים מוקדמים לסרטן הלבלב בהבחנה בין מקרים גרומתיים ללא גרומתיים. בתנאי פדרציה ששומרים על פרטיות, הגישה החדשה המודעת להטרוגניות השיבה את רוב הביצועים הללו והצליחה מעבר לשיטות פדרטיביות סטנדרטיות שהטו את התחזיות כלפי עודף או חוסר זיהוי גרורות. המערכת הייתה טובה במיוחד ברגישות — זיהוי מטופלים עם התפשטות לבלוטות — תוך השגת ספיקות מתונים אך משופרים, חילוף שמתאים להעדפה הקלינית של הימנעות ממחלה שלא זוהתה, גם במחיר של מספר מסוים של אזעקות שווא.
מה המשמעות להמשך
לקריא כללי, המסר המרכזי הוא שניתן כעת לאמן בינה מלאכותית חזקה על סריקות רגישות פרוסות בבתי חולים רבים מבלי להזיז את הנתונים, ועדיין לשפר את אופן שיפוט הרופאים האם סרטן הלבלב התפשט לבלוטות לימפה. עבודה זו מראה שהתחלה ממודל יסוד רחב של CT ושימוש בדרך חכמה יותר של מיזוג ידע מבתי חולים מגוונים מניבה חיזויים אמינים יותר ובעלי משמעות קלינית מאשר שיטות ישנות. אף שהכלי עדיין לא מושלם — במיוחד בצמצום חיובים שווא — הוא מהווה צעד מבטיח לעבר תמיכה בהחלטות בטוחה ועקבית יותר עבור כירורגים ואונקולוגים העומדים מול אחד מהאתגרים הקשים ביותר בתחום הסרטן.
ציטוט: Bhalla, P., Gaviria, D.D., Kupczyk, P. et al. Federated CT foundation models for multi-center detection of lymph node metastasis in pancreatic cancer. Sci Rep 16, 12051 (2026). https://doi.org/10.1038/s41598-026-47631-2
מילות מפתח: סרטן הלבלב, גרורות בבלוטות לימפה, הדמיית CT, בינה מלאכותית רפואית, למידה פדרטיבית