Clear Sky Science · ru
Федеративные базовые модели КТ для многоцентрового выявления метастазов в лимфатические узлы при раке поджелудочной железы
Почему это важно для пациентов
Рак поджелудочной железы относится к числу наиболее смертельных злокачественных опухолей, отчасти потому, что часто выявляется на поздних стадиях и уже успевает распространиться в близлежащие лимфатические узлы. Знание того, произошло ли такое распространение до операции, критично: это определяет радикальность вмешательства и целесообразность первичной химиотерапии. Тем не менее современные КТ‑сканы, даже при интерпретации экспертами, пропускают многие скрытые метастазы. В этом исследовании изучается, как новое поколение крупных медицинских моделей ИИ, обучаемых совместно по больницам без обмена сырыми данными пациентов, может сделать эти решения, влияющие на жизнь, более точными и справедливыми.
Тяжёлый рак и «слепая зона» в визуализации
Большинство случаев рака поджелудочной железы приходится на панкреатическую протоковую аденокарциному, известную своей плохой выживаемостью. Важным признаком тяжести заболевания является распространение в лимфатические узлы рядом с поджелудочной железой. Радиологи пытаются обнаружить такое распространение на КТ, преимущественно оценивая размер и форму узлов. К сожалению, эти визуальные подсказки ненадёжны: у многих пациентов микроскопическое распространение выглядит «нормально» на КТ, а эксперты часто расходятся во мнениях. В результате опухоль может быть недооценена, и некоторые пациенты не получают интенсивного лечения, которое им действительно требуется.
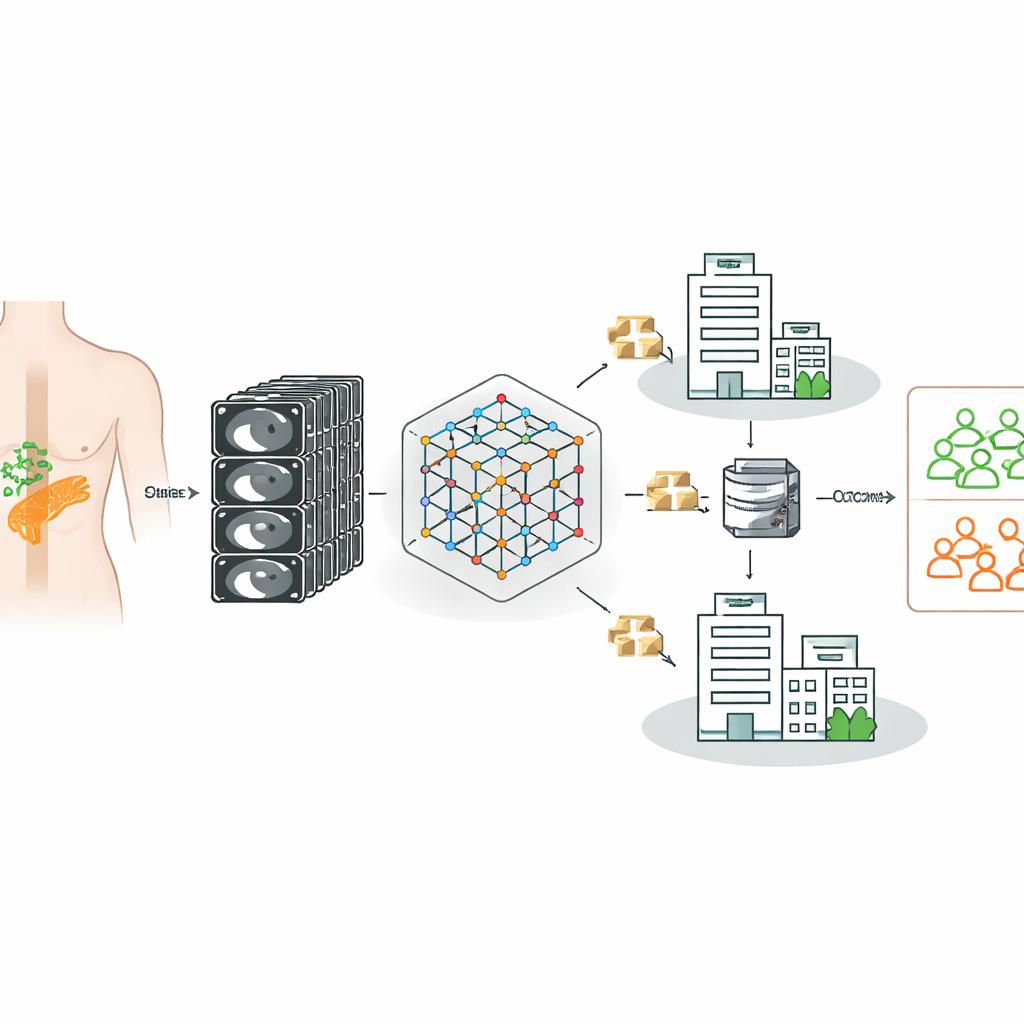
Обучение модели КТ на данных многих больниц
Исследователи опирались на мощную «фундаментальную модель» для КТ‑изображений — систему ИИ, изначально обученную на 148 000 КТ‑сканах для распознавания общих трёхмерных анатомических паттернов. Затем эту модель дообучили для задачи определения, имеются ли у каждого пациента с раком поджелудочной железы истинные метастазы в лимфатические узлы, используя подтверждённые хирургические и патологоанатомические данные в качестве эталона. Важно, что данные поступали из трёх немецких больниц с разными сканерами, протоколами визуализации и популяциями пациентов, отражая реальную клиническую разнородность, а не единый тщательно отобранный набор данных.
Сотрудничество без обмена данными пациентов
Поскольку строгие правила конфиденциальности препятствуют свободному объединению сканов пациентов, команда обратилась к федеративному обучению. В этом подходе общая модель отправляется в каждую больницу, обучается локально на данных этой больницы, а затем обновляется централизованно только с помощью параметров модели, но не самих изображений. Стандартные федеративные методы, однако, предполагают, что все участники похожи между собой. В медицине это редко так: различия в аппаратах, времени контрастирования и составе пациентов могут тянуть локальные модели в конфликтующие направления, ухудшая производительность при простом усреднении обновлений.
Более умный способ объединять знания больниц
Чтобы справиться с этим, авторы разработали «учитывающий гетерогенность» способ комбинирования обновлений от каждой больницы. Их метод учитывает не только то, насколько несбалансированы метки на каждом сайте (сколько пациентов с метастазами и без), но и насколько различается граница решений локальной модели по сравнению с общей моделью. Клиенты, чьи модели слишком сильно отклоняются от общей картины, получают меньший вес при объединении обновлений. Эта стратегия, основанная на представлениях модели, стабилизирует обучение, при этом позволяя системе извлекать опыт каждой больницы, в результате чего глобальная модель лучше разделяет пациентов с наличием и отсутствием лимфогенного распространения.
Что показывают результаты для реальной клиники
Когда все данные были бы собраны централизованно — сценарий, который обычно блокируется правилами конфиденциальности — дообученная фундаментальная модель заметно превзошла традиционные методы машинного обучения и ранние модели для поджелудочной железы в задаче различения метастатических и неметастатических случаев. В условиях федеративного, сохраняющего приватность обучения, новый подход, учитывающий гетерогенность, восстановил большую часть этой производительности и превзошёл стандартные федеративные методы, которые склонны были либо переоценивать, либо недооценивать наличие метастазов. Система показала особенно хорошую чувствительность — улавливала пациентов с поражением лимфатических узлов — при умеренно улучшенной специфичности, компромисс, соответствующий клиническому приоритету избегать пропуска заболевания, даже ценой некоторых ложных тревог.
Что это означает в перспективе
Для неспециалиста ключевое сообщение в том, что мощные модели ИИ теперь можно обучать на конфиденциальных сканах, распределённых по многим больницам, не перемещая сами данные, и при этом улучшать способность врачей оценивать, распространился ли рак поджелудочной железы в лимфатические узлы. Работа показывает, что старт с широкой фундаментальной КТ‑модели и более умный способ слияния знаний разных больниц дают более надёжные и клинически значимые прогнозы, чем старые методы. Хотя инструмент ещё не совершенен — особенно в части избежания ложноположительных результатов — он представляет собой многообещающий шаг к более безопасной и согласованной системе поддержки принятия решений для хирургов и онкологов, сталкивающихся с одним из самых сложных видов рака.
Цитирование: Bhalla, P., Gaviria, D.D., Kupczyk, P. et al. Federated CT foundation models for multi-center detection of lymph node metastasis in pancreatic cancer. Sci Rep 16, 12051 (2026). https://doi.org/10.1038/s41598-026-47631-2
Ключевые слова: рак поджелудочной железы, метастазы в лимфатические узлы, КТ-изображение, медицинский ИИ, федеративное обучение