Clear Sky Science · fr
Modèles fondamentaux fédérés pour la tomodensitométrie pour la détection multi‑centre des métastases ganglionnaires dans le cancer du pancréas
Pourquoi cela compte pour les patients
Le cancer du pancréas est l’un des plus mortels, en partie parce qu’il est souvent découvert tardivement et s’est déjà propagé aux ganglions lymphatiques voisins. Savoir si cette dissémination a eu lieu avant la chirurgie est crucial : cela oriente l’agressivité de l’intervention et détermine si les patients devraient recevoir une chimiothérapie en amont. Pourtant, les scanners CT actuels, même interprétés par des experts, manquent de nombreuses métastases occultes. Cette étude explore comment une nouvelle génération de grands modèles d’IA médicale, entraînés en collaboration entre hôpitaux sans partager les données brutes des patients, pourrait rendre ces décisions déterminantes plus précises et plus équitables.
Un cancer difficile et une zone d’ombre en imagerie
La plupart des cancers du pancréas sont des adénocarcinomes canalaires pancréatiques, connus pour leur mauvais pronostic. Un signe clé de gravité est la dissémination aux ganglions situés près du pancréas. Les radiologues cherchent à repérer cette propagation sur les scanners CT, en examinant généralement la taille et la forme des ganglions. Malheureusement, ces indices visuels sont peu fiables : de nombreux patients présentant une dissémination microscopique ont un aspect « normal » au CT, et les experts divergent souvent dans leurs interprétations. En conséquence, les tumeurs peuvent être sous‑estimées et certains patients ne reçoivent pas le traitement intensif dont ils auraient besoin.
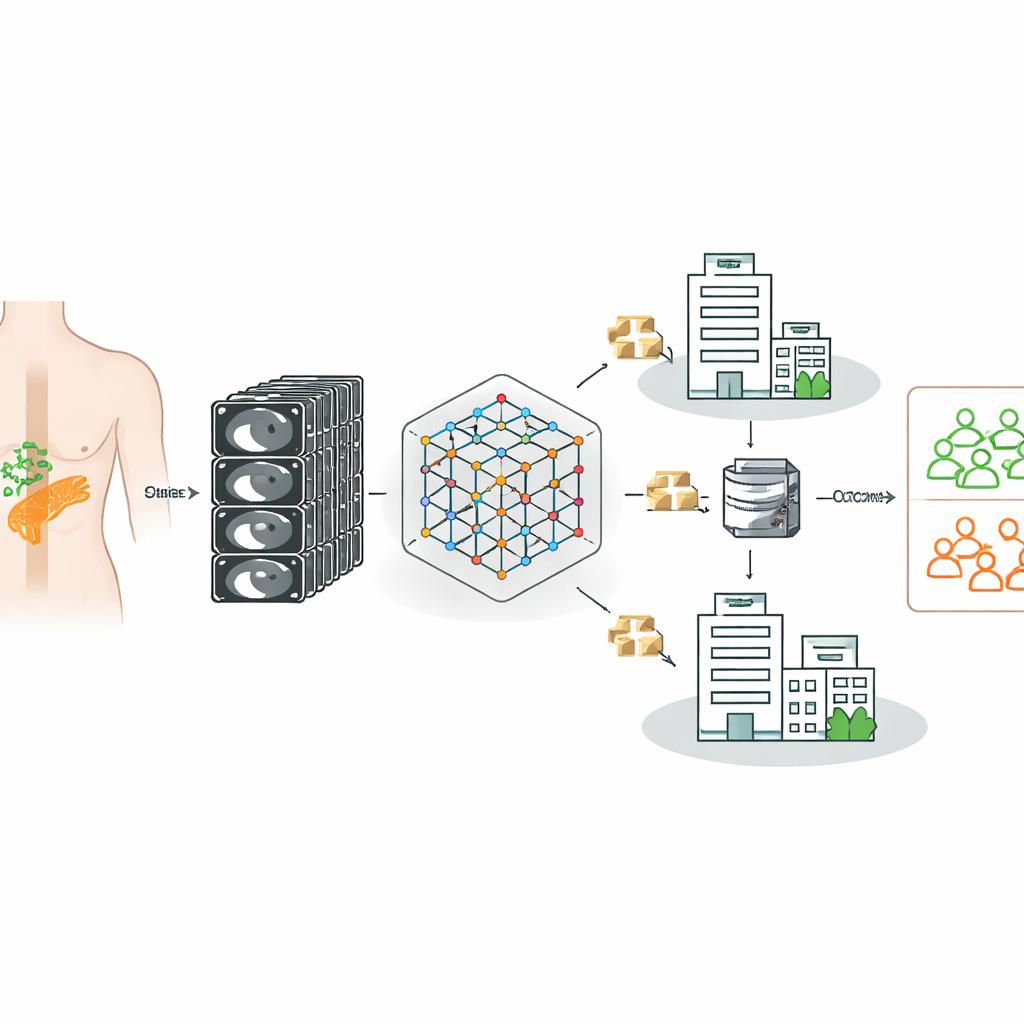
Apprendre à un modèle CT à tirer parti de nombreux hôpitaux
Les chercheurs se sont appuyés sur un puissant « modèle fondamental » pour l’imagerie CT — un système d’IA initialement entraîné sur 148 000 scanners CT pour reconnaître des motifs généraux dans l’anatomie tridimensionnelle. Ils ont ensuite affiné ce modèle pour décider, pour chaque patient atteint d’un cancer du pancréas, si les ganglions étaient réellement métastatiques, en utilisant comme vérité de terrain les résultats chirurgicaux et pathologiques confirmés. Fait important, les données provenaient de trois hôpitaux allemands disposant de scanners, de protocoles d’imagerie et de populations de patients différents, reflétant la réalité hétérogène de la pratique clinique plutôt qu’un jeu de données unique soigneusement sélectionné.
Collaborer sans partager les données des patients
Parce que des règles strictes de confidentialité empêchent les hôpitaux de fusionner librement les images des patients, l’équipe a eu recours à l’apprentissage fédéré. Dans cette approche, un modèle commun est envoyé à chaque hôpital, entraîné localement sur les données de cet hôpital, puis mis à jour de façon centralisée en n’utilisant que les paramètres appris du modèle, jamais les images elles‑mêmes. Les méthodes fédérées standard supposent toutefois que tous les sites se ressemblent. En médecine, cela est rarement le cas : des différences dans les appareils, le timing du produit de contraste et la composition des patients peuvent tirer les modèles locaux dans des directions contradictoires, dégradant les performances lorsque leurs mises à jour sont simplement moyennées.
Une manière plus intelligente de combiner les apprentissages des hôpitaux
Pour y remédier, les auteurs ont conçu une méthode « consciente de l’hétérogénéité » pour combiner les mises à jour de chaque hôpital. Leur approche prend en compte non seulement le déséquilibre des étiquettes de chaque site (combien de patients ont ou n’ont pas de métastases) mais aussi à quel point la frontière de décision apprise par chaque hôpital diffère du modèle commun. Les clients dont les modèles dévient trop du schéma partagé voient leur contribution pondérée à la baisse lors de la fusion des mises à jour. Cette stratégie, sensible à la représentation, stabilise l’entraînement tout en permettant au système d’apprendre de l’expérience unique de chaque hôpital, produisant un modèle global qui sépare mieux les patients avec et sans dissémination ganglionnaire.
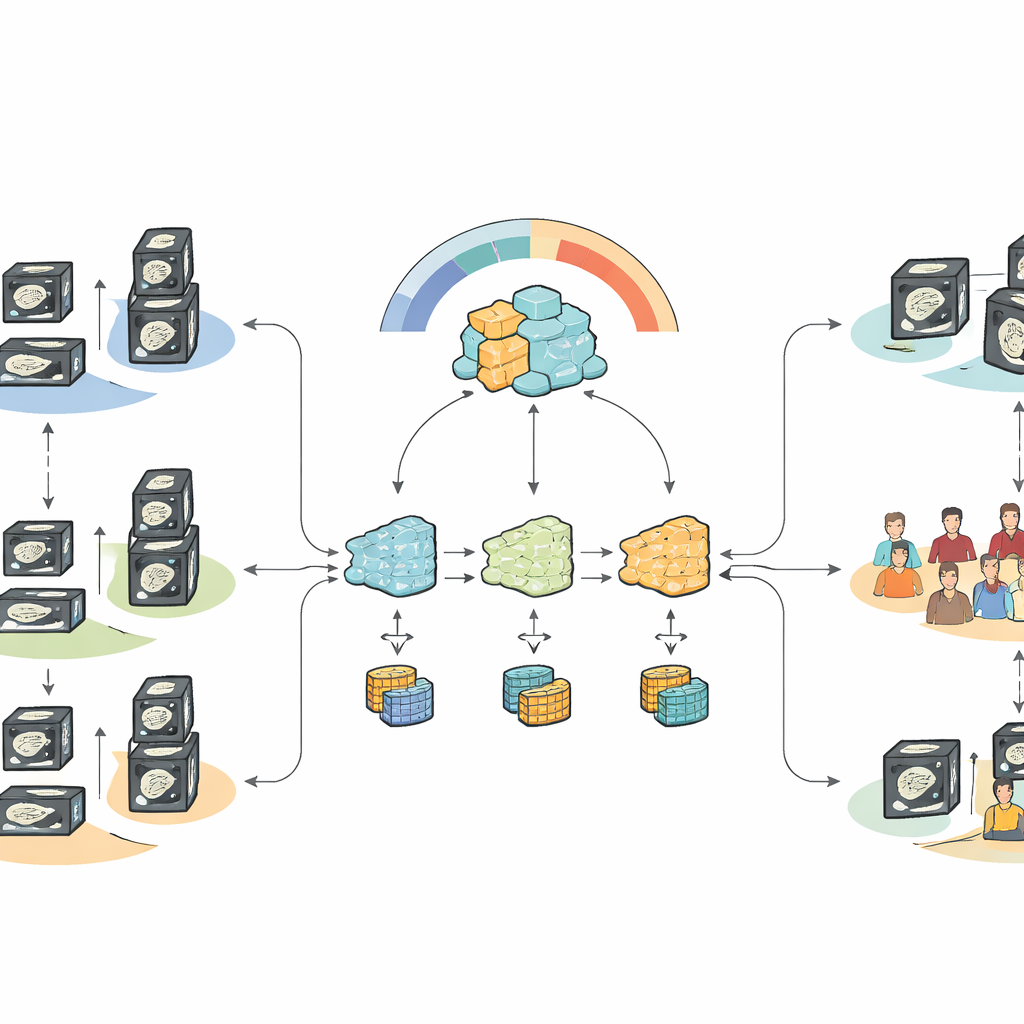
Ce que montrent les résultats pour la prise en charge réelle
Lorsque toutes les données ont été centralisées — un scénario généralement bloqué par les réglementations sur la vie privée — le modèle fondamental affiné a nettement surpassé les techniques d’apprentissage automatique traditionnelles et les modèles pancréatiques antérieurs pour distinguer les cas métastatiques des cas non métastatiques. Dans des conditions fédérées préservant la vie privée, la nouvelle approche consciente de l’hétérogénéité a récupéré la majeure partie de ces performances et a dépassé les méthodes fédérées standard qui avaient tendance à sur‑ ou sous‑estimer les métastases. Le système était particulièrement performant en sensibilité — détecter les patients avec dissémination ganglionnaire — tout en atteignant une spécificité modérée mais améliorée, un compromis qui correspond à la priorité clinique d’éviter les maladies manquées, quitte à accepter davantage de faux positifs.
Ce que cela signifie pour la suite
Pour un lecteur non spécialiste, le message principal est que des IA puissantes peuvent désormais être entraînées sur des scans sensibles répartis dans de nombreux hôpitaux sans déplacer les données, et améliorer malgré tout l’évaluation par les médecins de la dissémination ganglionnaire du cancer du pancréas. Ce travail montre qu’en partant d’un large modèle fondamental CT et en utilisant une manière plus intelligente de mélanger les connaissances issues d’hôpitaux divers, on obtient des prédictions plus fiables et cliniquement pertinentes que les méthodes antérieures. Bien que l’outil ne soit pas encore parfait — en particulier pour éviter les faux positifs — il représente une étape prometteuse vers un soutien à la décision plus sûr et plus cohérent pour les chirurgiens et les oncologues confrontés à l’un des cancers les plus difficiles.
Citation: Bhalla, P., Gaviria, D.D., Kupczyk, P. et al. Federated CT foundation models for multi-center detection of lymph node metastasis in pancreatic cancer. Sci Rep 16, 12051 (2026). https://doi.org/10.1038/s41598-026-47631-2
Mots-clés: cancer du pancréas, métastases ganglionnaires, imagerie CT, IA médicale, apprentissage fédéré