Clear Sky Science · de
Föderierte CT‑Foundation‑Modelle zur multizentrischen Erkennung von Lymphknotenmetastasen beim Pankreaskarzinom
Warum das für Patientinnen und Patienten wichtig ist
Das Pankreaskarzinom gehört zu den tödlichsten Krebsarten, unter anderem weil es oft spät entdeckt wird und zu diesem Zeitpunkt bereits in benachbarte Lymphknoten übergegangen ist. Zu wissen, ob diese Ausbreitung vor einer Operation stattgefunden hat, ist entscheidend: Es bestimmt, wie aggressiv der Eingriff sein sollte und ob Patientinnen und Patienten zuerst eine Chemotherapie erhalten sollten. Aktuelle CT‑Aufnahmen, von Expertinnen und Experten beurteilt, übersehen jedoch viele dieser verborgenen Metastasen. Diese Studie untersucht, wie eine neue Generation großer medizinischer KI‑Modelle, die kollaborativ über mehrere Krankenhäuser hinweg trainiert werden, ohne Rohpatientendaten auszutauschen, diese lebensverändernden Entscheidungen genauer und gerechter machen könnte.
Ein schwerer Krebs und eine Schwachstelle der Bildgebung
Die meisten Pankreaskarzinome sind sogenannte duktale Adenokarzinome der Bauchspeicheldrüse, die für ihre schlechte Überlebensrate bekannt sind. Ein zentrales Zeichen für eine schwere Erkrankung ist die Ausbreitung in Lymphknoten in der Nähe der Bauchspeicheldrüse. Radiologinnen und Radiologen versuchen, diese Ausbreitung in CT‑Bildern zu erkennen, meist anhand von Größe und Form der Lymphknoten. Leider sind diese visuellen Hinweise unzuverlässig: Viele Patientinnen und Patienten mit mikroskopischer Streuung erscheinen im CT „normal“, und Expertinnen und Experten sind sich häufig uneinig. Infolgedessen können Tumoren unterschätzt werden und einige Patientinnen und Patienten erhalten nicht die intensive Behandlung, die sie tatsächlich bräuchten.
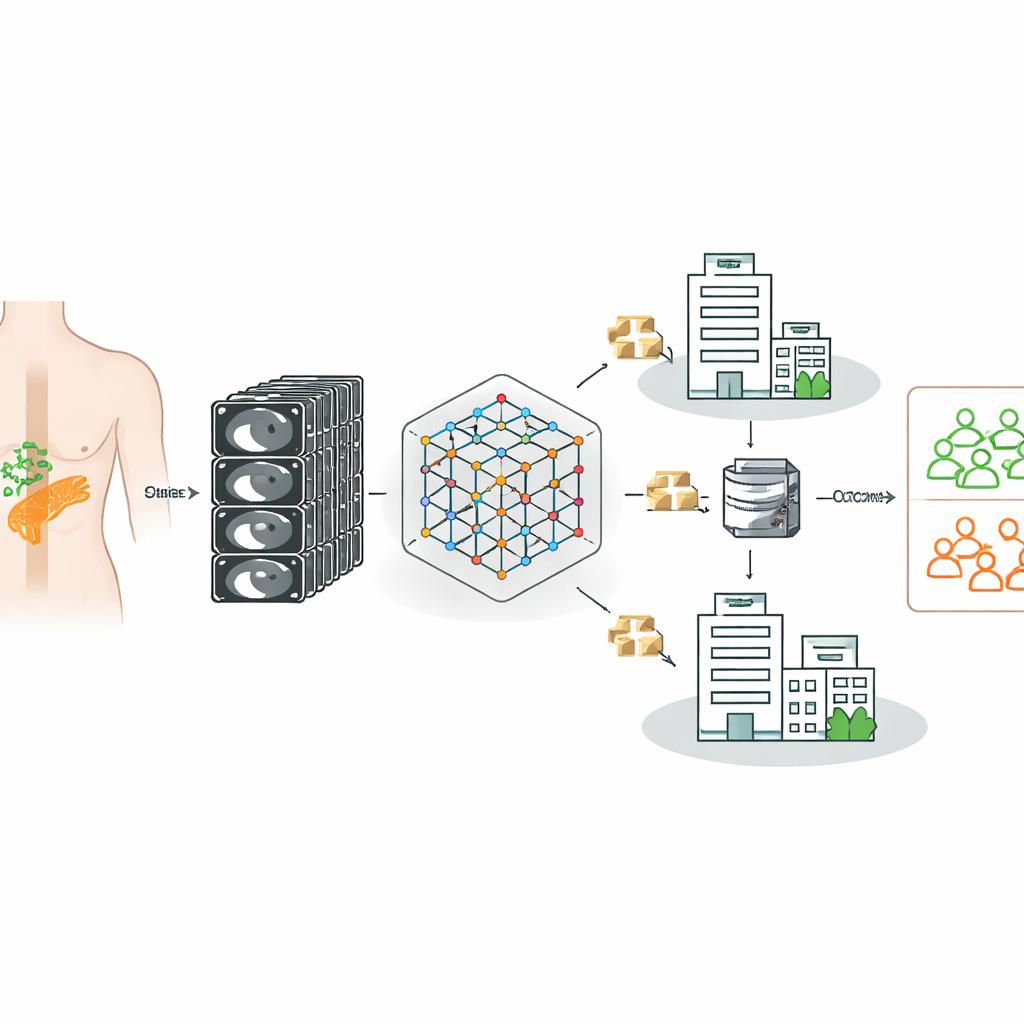
Ein CT‑Modell so trainieren, dass es von vielen Krankenhäusern lernt
Die Forschenden bauten auf einem leistungsfähigen „Foundation‑Modell“ für CT‑Bildgebung auf – einem KI‑System, das zunächst an 148.000 CT‑Aufnahmen trainiert wurde, um allgemeine Muster in der dreidimensionalen Anatomie zu erkennen. Anschließend passten sie dieses Modell gezielt an, damit es für jede Patientin bzw. jeden Patienten mit Pankreaskarzinom entscheiden kann, ob Lymphknoten tatsächlich metastatisch sind, wobei bestätigte chirurgische und pathologische Befunde als Goldstandard dienten. Wichtig ist, dass die Daten aus drei deutschen Krankenhäusern stammten, die unterschiedliche Scanner, Bildgebungsprotokolle und Patientenpopulationen nutzen – ein Abbild der unordentlichen Realität der klinischen Praxis statt eines einzelnen, sorgfältig kuratierten Datensatzes.
Kollaboration ohne Austausch von Patientendaten
Da strenge Datenschutzvorschriften Krankenhäusern häufig verbieten, Patientenscans frei zusammenzuführen, wandte sich das Team dem föderierten Lernen zu. Bei diesem Ansatz wird ein gemeinsames Modell an jedes Krankenhaus gesendet, lokal mit den dortigen Daten trainiert und anschließend zentral nur anhand der gelernten Modellparameter aktualisiert – niemals anhand der Bilder selbst. Standardmäßige föderierte Methoden gehen jedoch davon aus, dass alle Standorte ähnlich sind. In der Medizin trifft das selten zu: Unterschiede bei Geräten, Kontrasttiming und Patientenmix können lokale Modelle in widersprüchliche Richtungen ziehen und die Leistung verschlechtern, wenn ihre Updates einfach gemittelt werden.
Eine klügere Methode, das Gelernte der Krankenhäuser zu kombinieren
Um dem zu begegnen, entwickelten die Autorinnen und Autoren eine „heterogenitäts‑bewusste“ Methode zur Kombination der Updates aus den einzelnen Krankenhäusern. Ihre Methode berücksichtigt nicht nur, wie unausgeglichen die Label an jedem Standort sind (wie viele Patienten Metastasen haben oder nicht), sondern auch, wie stark die von jedem Krankenhaus gelernte Entscheidungsgrenze vom gemeinsamen Modell abweicht. Clients, deren Modelle zu weit vom geteilten Muster abdriften, werden bei der Zusammenführung der Updates niedriger gewichtet. Diese representations‑bewusste Strategie stabilisiert das Training, ohne das Lernen aus den einzigartigen Erfahrungen jedes Krankenhauses zu verhindern, und ergibt ein globales Modell, das Patientinnen und Patienten mit und ohne Lymphknotenbefall besser trennt.
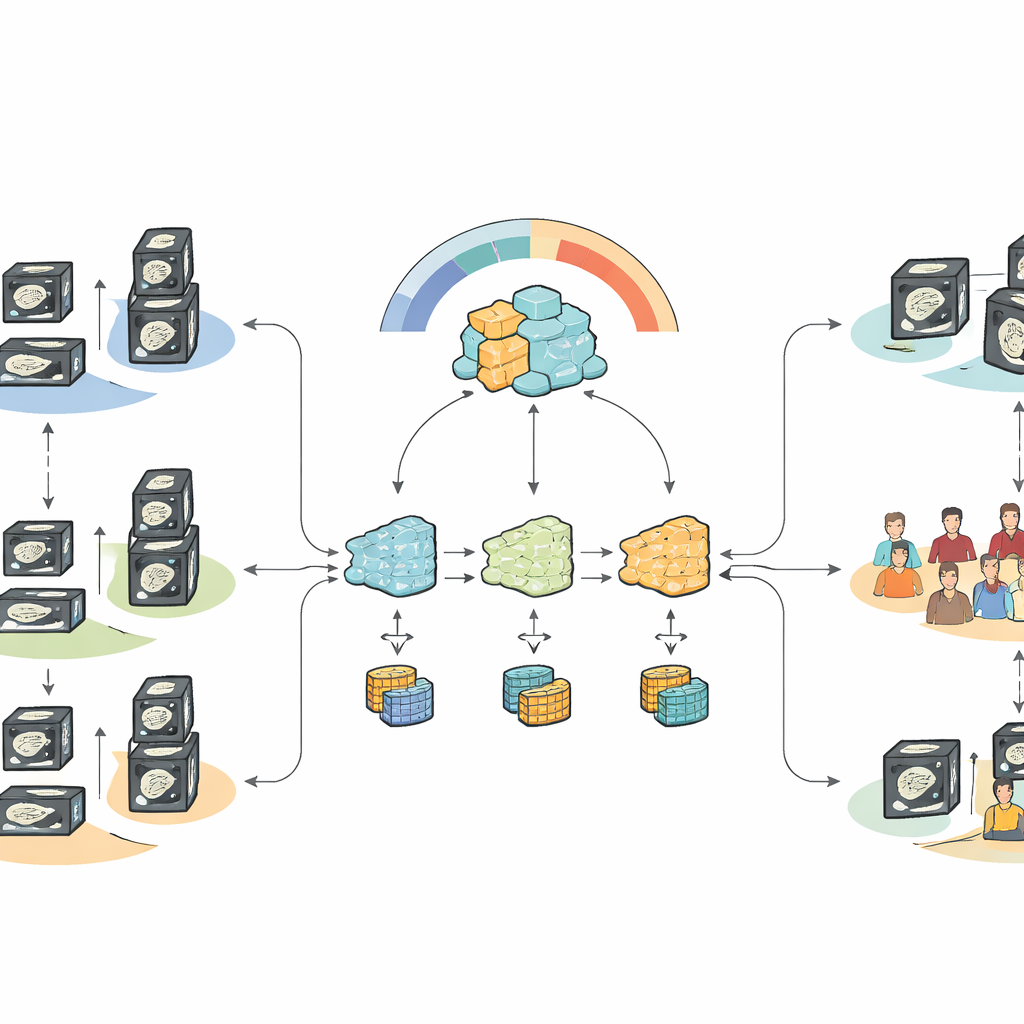
Was die Ergebnisse für die Versorgung in der Praxis zeigen
Wenn alle Daten zentral zusammengeführt wurden – ein Szenario, das in der Regel durch Datenschutzbestimmungen blockiert wäre – übertraf das feinabgestimmte Foundation‑Modell deutlich traditionelle maschinelle Lernverfahren und frühere Pankreasmodelle bei der Unterscheidung von metastatischen und nicht‑metastatischen Fällen. Unter föderierten, datenschutzwahrenden Bedingungen stellte der neue heterogenitäts‑bewusste Ansatz einen Großteil dieser Leistung wieder her und übertraf standardmäßige föderierte Methoden, die entweder zu viele oder zu wenige Metastasen voraussagten. Das System war besonders gut in der Sensitivität – es erwischte Patientinnen und Patienten mit Lymphknotenbefall – und erreichte zugleich eine moderate, aber verbesserte Spezifität, ein Kompromiss, der der klinischen Priorität entspricht, kein Vorliegen der Krankheit zu übersehen, selbst wenn das einige Fehlalarme zur Folge hat.
Was das für die Zukunft bedeutet
Für eine fachlich interessierte Leserschaft lautet die Kernbotschaft: Leistungsfähige KI lässt sich heute an sensiblen Aufnahmen trainieren, die über viele Krankenhäuser verteilt sind, ohne die Daten zu bewegen, und kann dennoch die Einschätzung verbessern, ob sich Pankreaskrebs in Lymphknoten ausgebreitet hat. Diese Arbeit zeigt, dass der Start von einem breiten CT‑Foundation‑Modell und die Nutzung einer klügeren Methode zum Verschmelzen des Wissens aus verschiedenen Krankenhäusern verlässlichere, klinisch relevante Vorhersagen liefern als ältere Methoden. Obwohl das Werkzeug noch nicht perfekt ist – insbesondere bei der Vermeidung falsch positiver Befunde – stellt es einen vielversprechenden Schritt in Richtung sichererer und konsistenterer Entscheidungsunterstützung für Chirurginnen und Chirurgen sowie Onkologinnen und Onkologen dar, die mit einer der herausforderndsten Krebsarten konfrontiert sind.
Zitation: Bhalla, P., Gaviria, D.D., Kupczyk, P. et al. Federated CT foundation models for multi-center detection of lymph node metastasis in pancreatic cancer. Sci Rep 16, 12051 (2026). https://doi.org/10.1038/s41598-026-47631-2
Schlüsselwörter: Pankreaskrebs, Lymphknotenmetastasen, CT‑Bildgebung, medizinische KI, föderiertes Lernen