Clear Sky Science · nl
Federated CT‑foundationmodellen voor multicenterdetectie van lymfeknooppmetastasen bij alvleesklierkanker
Waarom dit belangrijk is voor patiënten
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, deels omdat hij vaak laat wordt ontdekt en dan al is uitgezaaid naar nabije lymfeklieren. Weten of die verspreiding vóór de operatie heeft plaatsgevonden is cruciaal: het bepaalt hoe ingrijpend de operatie moet zijn en of patiënten eerst chemotherapie dienen te krijgen. Toch missen huidige CT‑scans, zelfs wanneer door experts beoordeeld, veel van deze verborgen metastasen. Deze studie onderzoekt hoe een nieuwe generatie grote medische AI‑modellen, gezamenlijk getraind over ziekenhuizen heen zonder ruwe patiëntgegevens te delen, dergelijke levensbepalende beslissingen nauwkeuriger en rechtvaardiger zou kunnen maken.
Een agressieve kanker en een blind vak in beeldvorming
De meeste alvleesklierkankers behoren tot het type pancreatisch ductaal adenocarcinoom, dat berucht is vanwege de slechte overleving. Een belangrijke aanwijzing dat de ziekte ernstig is, is uitzaaiing naar lymfeklieren nabij de alvleesklier. Radiologen proberen deze uitzaaiing op CT‑scans te herkennen, meestal door naar de grootte en vorm van lymfeklieren te kijken. Helaas zijn deze visuele aanwijzingen onbetrouwbaar: veel patiënten met microscopische uitzaaiingen lijken op CT “normaal”, en experts lopen vaak uiteen in hun beoordeling. Daardoor kan de tumor worden onderschat en krijgen sommige patiënten niet de intensieve behandeling die ze eigenlijk nodig hebben.
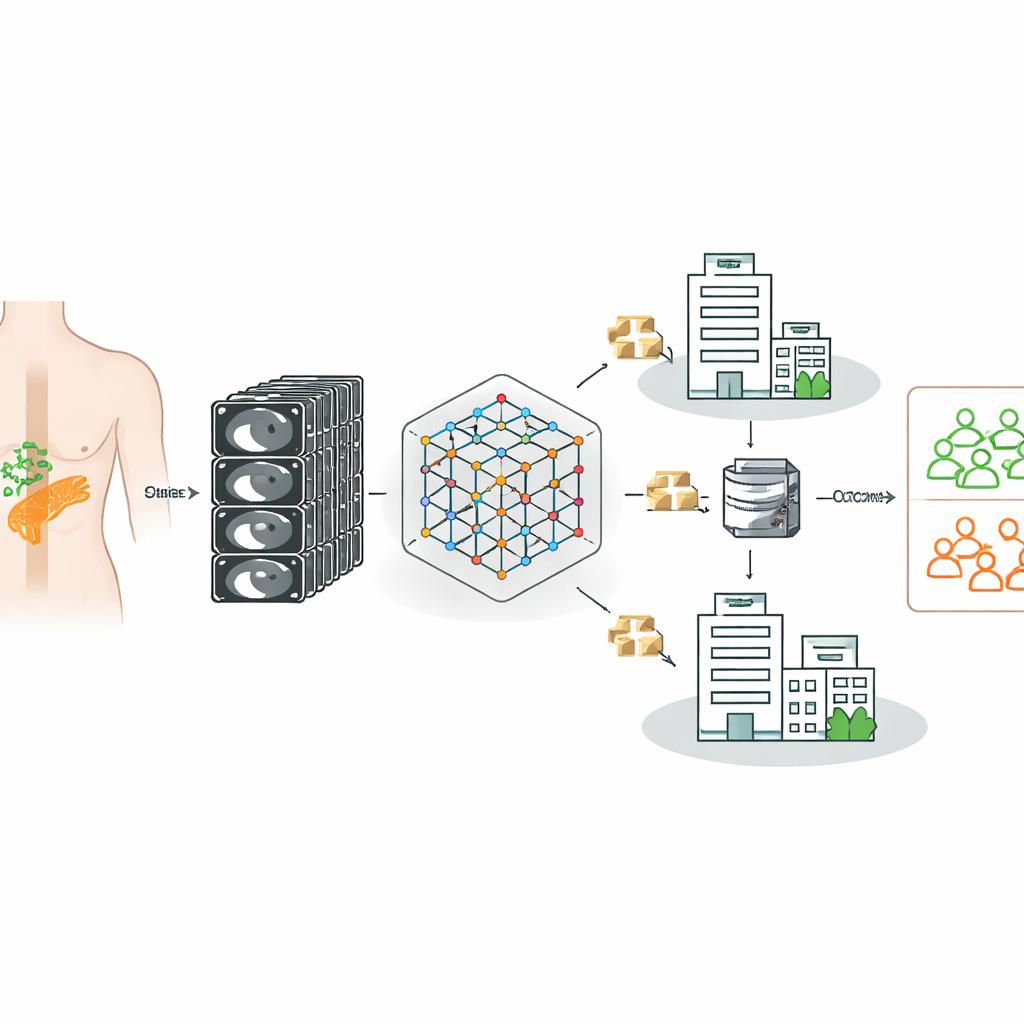
Een CT‑model leren van veel ziekenhuizen
De onderzoekers bouwden voort op een krachtig “foundationmodel” voor CT‑beeldvorming — een AI‑systeem dat aanvankelijk getraind is op 148.000 CT‑scans om algemene patronen in driedimensionale anatomie te herkennen. Zij verfijnden dit model vervolgens om per patiënt met alvleesklierkanker te beslissen of lymfeklieren daadwerkelijk gemetastaseerd waren, waarbij bevestigde chirurgische en pathologierapporten als grondwaarheid werden gebruikt. Belangrijk is dat de data afkomstig waren uit drie Duitse ziekenhuizen met verschillende scanners, beeldvormingsprotocollen en patiëntpopulaties, wat de rommelige realiteit van de klinische praktijk weerspiegelt in plaats van een enkele, zorgvuldig samengestelde dataset.
Samenwerken zonder patiëntgegevens te delen
Omdat strikte privacyregels ziekenhuizen verhinderen patiëntscans vrijelijk te centraliseren, wendde het team zich tot federated learning. Bij deze aanpak wordt een gemeenschappelijk model naar elk ziekenhuis gestuurd, lokaal getraind op die ziekenhuisdata, en daarna centraal bijgewerkt met alleen de geleerde modelparameters, nooit met de beelden zelf. Standaard federated‑methoden gaan er echter van uit dat alle locaties op elkaar lijken. In de geneeskunde is dat zelden het geval: verschillen in apparatuur, timing van contrastmiddelen en patiëntenbestand kunnen lokale modellen in tegenstrijdige richtingen trekken, wat de prestatie verslechtert wanneer hun updates simpelweg worden gemiddeld.
Een slimmer manier om te combineren wat ziekenhuizen leren
Om dit aan te pakken ontwierpen de auteurs een “heterogeniteits‑bewuste” manier om updates van elk ziekenhuis te combineren. Hun methode kijkt niet alleen naar hoe onevenwichtig de labels per locatie zijn (hoeveel patiënten wel of geen metastasen hebben), maar ook naar hoe verschillend de door elk ziekenhuis geleerde beslissingsgrens is ten opzichte van het gemeenschappelijke model. Clients waarvan de modellen te ver afdrijven van het gedeelde patroon worden bij het samenvoegen van de updates minder zwaar gewogen. Deze representatie‑bewuste strategie stabiliseert de training en laat het systeem toch profiteren van elke locatie’s unieke ervaring, wat leidt tot een globaal model dat patiënten met en zonder lymfeknoopuitzaaiing beter scheidt.
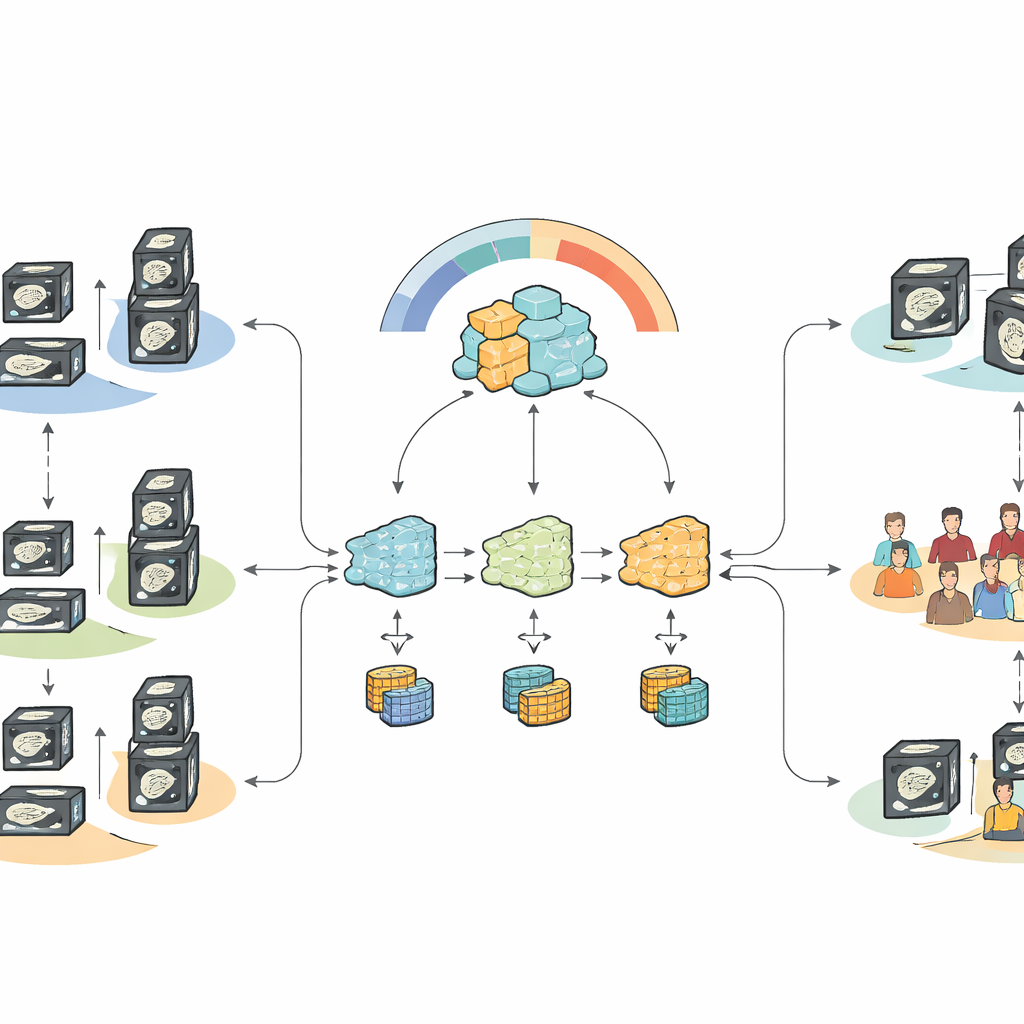
Wat de resultaten laten zien voor de zorg in de praktijk
Wanneer alle data centraal werden samengevoegd — een scenario dat doorgaans door privacyregelgeving zou worden geblokkeerd — versloeg het fijn afgestelde foundationmodel duidelijk traditionele machine‑learningtechnieken en eerdere alvleeskliermodellen bij het onderscheiden van gemetastaseerde en niet‑gemetastaseerde gevallen. Onder federated, privacy‑behoudende voorwaarden wist de nieuwe heterogeniteits‑bewuste aanpak het grootste deel van die prestatie te herstellen en presteerde beter dan standaard federated‑methoden die metastasen ofwel te veel ofwel te weinig voorspelden. Het systeem was bijzonder goed in sensitiviteit — het opsporen van patiënten met lymfeknoopuitzaaiing — terwijl het een matige maar verbeterde specificiteit behaalde, een afweging die past bij de klinische prioriteit om gemiste ziekte te vermijden, zelfs ten koste van enkele false alarms.
Wat dit vooruit betekent
Voor een niet‑specialistische lezer is de kernboodschap dat krachtige AI nu kan worden getraind op gevoelige scans die verspreid staan over veel ziekenhuizen zonder de data te verplaatsen, en toch kan verbeteren hoe artsen inschatten of alvleesklierkanker naar lymfeklieren is uitgezaaid. Dit werk toont dat starten vanuit een breed CT‑foundationmodel en een slimmere manier van samenvoegen van kennis uit diverse ziekenhuizen leidt tot betrouwbaardere, klinisch relevante voorspellingen dan oudere methoden. Hoewel het hulpmiddel nog niet perfect is — met name in het vermijden van foutpositieve uitslagen — vormt het een veelbelovende stap richting veiliger, consistenter beslissingsondersteuning voor chirurgen en oncologen die een van de meest uitdagende kankersoorten behandelen.
Bronvermelding: Bhalla, P., Gaviria, D.D., Kupczyk, P. et al. Federated CT foundation models for multi-center detection of lymph node metastasis in pancreatic cancer. Sci Rep 16, 12051 (2026). https://doi.org/10.1038/s41598-026-47631-2
Trefwoorden: alvleesklierkanker, lymfeknoopmetastase, CT‑beeldvorming, medische AI, federated learning