Clear Sky Science · zh
基于放射组学的机器学习模型在酰胺质子转移加权影像上用于脑胶质瘤分级的可解释性
这项研究为何重要
被称为胶质瘤的脑肿瘤可从生长相对缓慢到高度侵袭性不等。传统上,医生通过手术或活检取出肿瘤组织片并在显微镜下检查来确定胶质瘤的危险程度。这种方法具有侵入性、伴随医疗风险,并且可能错过在高度不均匀肿瘤中最具侵袭性的区域。本研究探讨了先进的磁共振成像结合人工智能是否能实现对胶质瘤的非侵入性分级——更重要的是,解释计算模型如何做出决策,以便医生能够信任并解读结果。
无需手术也能窥见大脑内部
研究者聚焦于一种特殊的磁共振方法:酰胺质子转移加权(APTw)成像,它对脑组织的化学环境敏感。早期研究表明APTw图像能够区分高分级和低分级胶质瘤,但其成功背后的原因尚未完全明了。在本研究中,102例未经治疗的脑胶质瘤患者在肿瘤手术切除并由病理学家分级前接受了包括APTw在内的磁共振扫描。研究小组随后利用这些扫描训练计算模型,以仅凭影像数据区分最具侵袭性的肿瘤(4级)与其他所有肿瘤,试图模拟病理学家的判断。
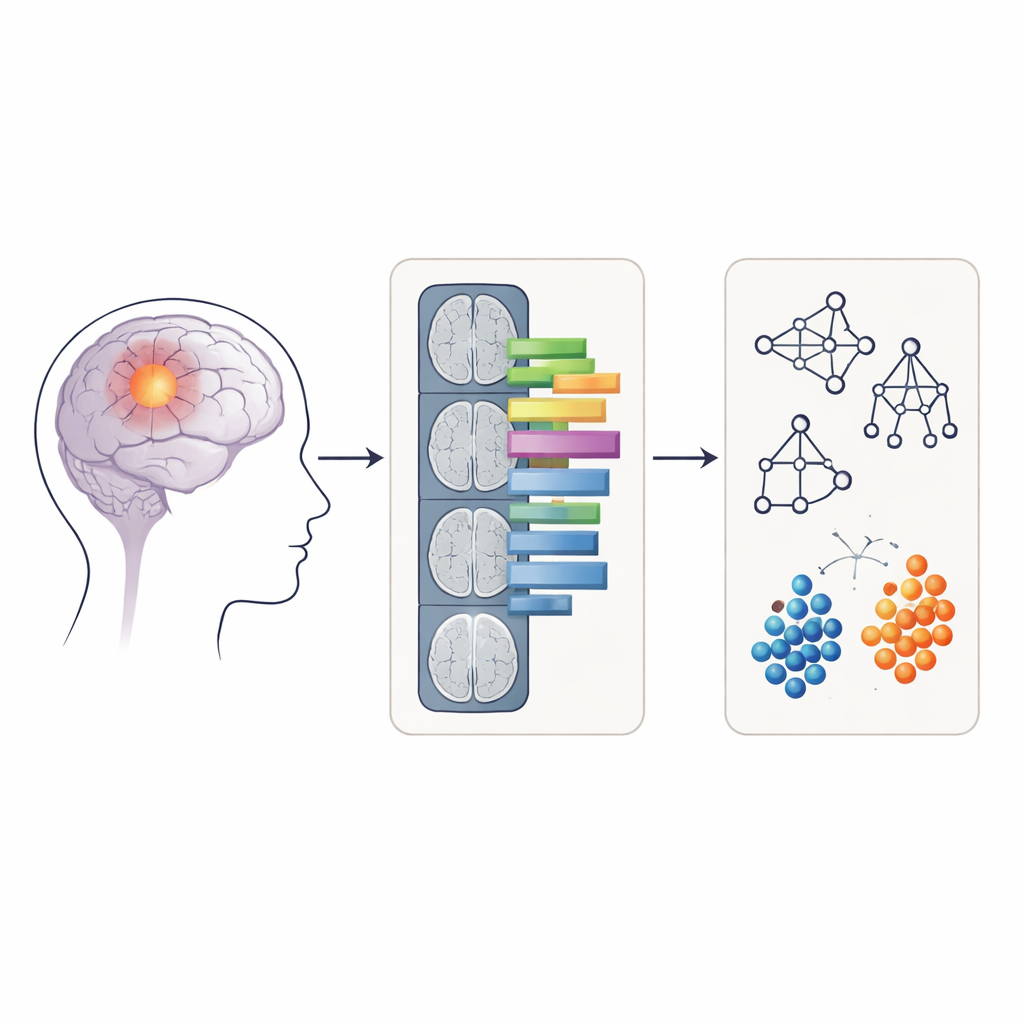
将图像转换为可测量的模式
研究者并非直接将原始MRI图像输入计算机,而是采用一种称为放射组学的技术,将医学影像转换为数百个数值特征。这些特征描述诸如肿瘤形状的圆润或不规则程度,以及信号强度在肿瘤内分布的均匀或不均匀程度等信息。对于每名患者,研究者从APTw图像上两类区域提取放射组学特征:仅肿瘤的强化核心,以及包含强化核心和周围肿胀组织(脑水肿)的较大区域。四种常见的机器学习方法——随机森林、支持向量机、朴素贝叶斯和逻辑回归——在这些特征上进行训练和测试,以评估它们将肿瘤分类为4级或非4级的准确性。
打开人工智能的黑箱
许多强大的机器学习模型像“黑箱”一样,能够做出正确预测却不揭示其推理过程。为了解决这一问题,作者应用了三种可解释性工具。Shapley值估算每个特征对单次预测的贡献;置换重要性通过打乱特征后性能下降的幅度来衡量该特征的重要性;而一种称为anchors的方法寻找简单的、类规则的特征组合,这些组合足以支撑模型的决策。三者结合使研究团队能够识别模型在对胶质瘤分级时最依赖的APTw图像外观方面。
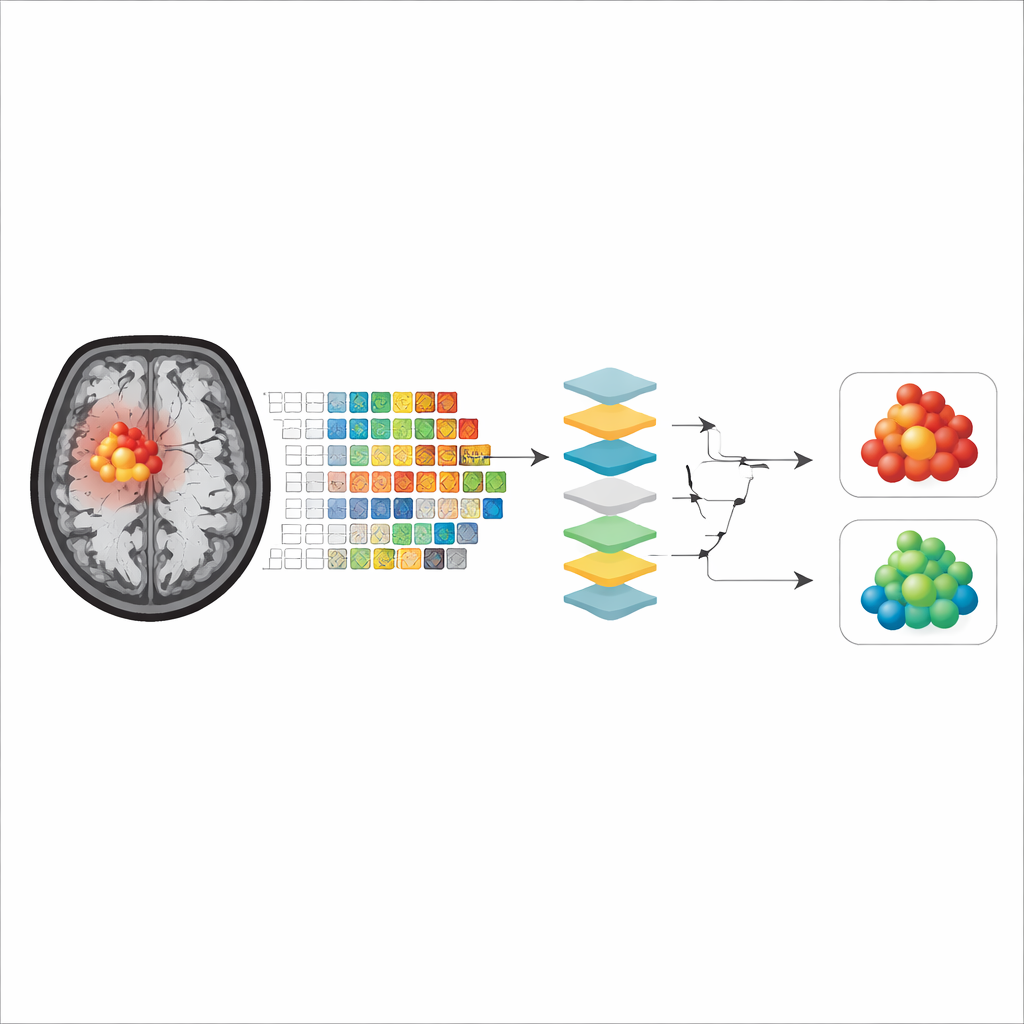
模型实际上关注什么
在所有模型与可解释性方法中,两类主要特征被一致识别为最重要。第一类描述肿瘤形状,尤其是肿瘤轮廓接近平滑、规则形态还是呈不规则、参差不齐。第二类反映肿瘤内部APTw信号的斑驳或均匀程度,指示内部组织类型的混合情况。有趣的是,当模型仅以强化核心为训练对象时,某些算法往往以形状特征为主;而当包含周围水肿组织时,内部信号不均匀度的度量有时会变得更具影响力,或根据具体模型情况相反。总体而言,关注强化肿瘤核心的模型表现略优,这表明该区域更好地代表真实肿瘤组织,较少受到坏死或水肿的混淆影响。
局限与未来方向
本研究存在若干实际限制。患者群中低分级肿瘤相对较少,因此模型被设计为将4级肿瘤与其他所有肿瘤合并区分,而不是逐级精确区分。数据也来自单一医院,且APTw图像的层厚相对较大,这可能限制某些形状特征测量的精度。尽管有这些限制,研究结果在不同的可解释性方法间保持一致,支持不规则肿瘤边界和内部信号不均匀性是模型识别高度侵袭性胶质瘤的关键影像线索这一观点。
对患者和医生意味着什么
简言之,这项工作表明,计算模型可以利用高级MRI扫描中隐藏的细微模式来区分侵袭性较强的脑肿瘤与相对不那么危险的肿瘤,并且阐明了图像中哪些视觉线索驱动这些决策。通过强调APTw扫描上肿瘤形状与内部斑驳性的关键性,并证明这些线索可以被透明地解释,该研究使非侵入性肿瘤分级更接近临床应用。如果在更大规模、多中心的研究中得到验证,这类可解释的人工智能工具可能帮助医生更安全、更迅速地制定治疗方案,有时减少高风险活检的需要,并仅凭影像为患者提供更清晰的信息。
引用: Gao, X., Wang, J. The explainability of radiomic-based machine learning models for brain glioma grading on amide proton transfer-weighted images. Sci Rep 16, 14539 (2026). https://doi.org/10.1038/s41598-026-44963-x
关键词: 脑胶质瘤影像, 放射组学, 可解释的人工智能, 磁共振生物标志物, 肿瘤分级