Clear Sky Science · sv
Tydliggörande av radiomik‑baserade maskininlärningsmodeller för gradbestämning av hjärngliom på amideprotonövergångsviktade bilder
Varför denna forskning är viktig
Hjärntumörer som kallas gliom kan variera från relativt långsamt växande till mycket aggressiva. Traditionellt avgörs ett glioms farlighet genom att kirurgen tar en bit av tumören vid operation eller biopsi och undersöker den i mikroskop. Det förfarandet är invasivt, medför medicinska risker och kan missa de mest aggressiva delarna av en ojämn tumör. Denna studie undersöker om avancerade MR‑undersökningar i kombination med artificiell intelligens kan gradbestämma gliom icke‑invasivt — och, avgörande, förklarar hur datoralgoritmerna fattar sina beslut så att läkare kan lita på och tolka resultaten.
Se in i hjärnan utan operation
Forskarna fokuserade på en speciell MR‑metod kallad amide proton transfer‑viktad (APTw) avbildning, som är känslig för vävnadens kemiska miljö. Tidigare studier visade att APTw‑bilder kan skilja mellan hög‑ och låggradiga gliom, men skälen till detta var inte helt klarlagda. I denna studie genomgick 102 patienter med obehandlade hjärngliom MR‑undersökningar, inklusive APTw‑bilder, innan tumörerna opererades bort och graderades av patologer. Teamet använde sedan dessa bilder för att träna datormodeller att särskilja de mest aggressiva tumörerna (grad 4) från övriga, i syfte att efterlikna patologens bedömning enbart med bilddata.
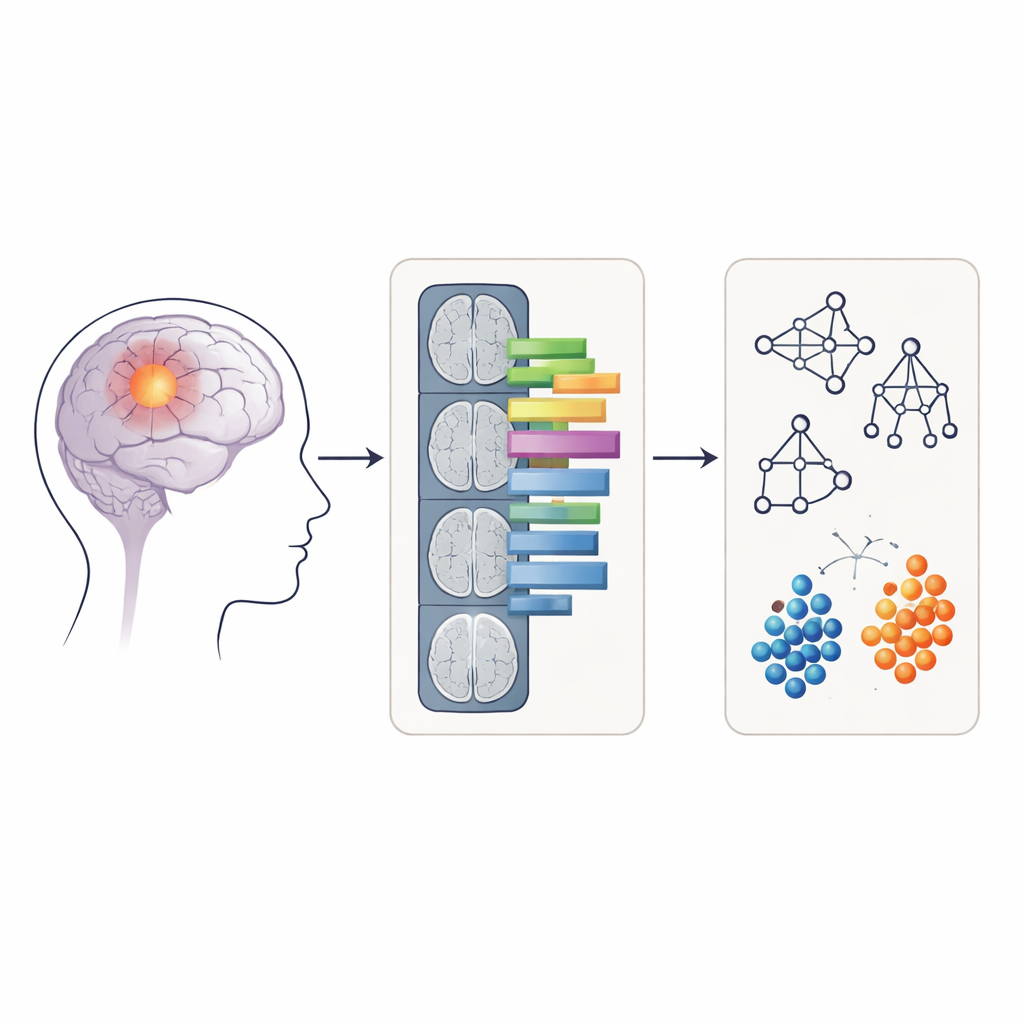
Att omvandla bilder till mätbara mönster
I stället för att mata råa MR‑bilder direkt till modellerna använde forskarna en teknik kallad radiomik, som omvandlar medicinska bilder till hundratals numeriska egenskaper. Dessa egenskaper beskriver till exempel hur rund eller oregelbunden tumören ser ut och hur jämnt eller ojämnt signalintensiteten är fördelad inom den. För varje patient extraherades radiomiska egenskaper från två typer av regioner på APTw‑bilderna: endast den kontrast‑förstärkande tumörkärnan, och ett större område som inkluderade både den förstärkande kärnan och den omgivande svullnaden (ödem). Fyra vanliga maskininlärningsmetoder — random forest, support vector machine, naïv Bayes och logistisk regression — tränades och testades på dessa egenskaper för att se hur noggrant de kunde klassificera tumörer som grad 4 eller ej.
Att öppna artificiell intelligens svarta låda
Många kraftfulla maskininlärningsmodeller fungerar som "svarta lådor": de gör korrekta prediktioner utan att avslöja hur de kom fram till dem. För att tackla detta använde författarna tre förklarbarhetsverktyg. Shapley‑värden uppskattar hur mycket varje egenskap bidrar till en given prediktion, permutation importance mäter hur mycket prestandan sjunker när en egenskap slumpas om, och en metod kallad anchors hittar enkla, regel‑lika kombinationer av egenskaper som är tillräckliga för att stödja ett modellsbeslut. Tillsammans gjorde dessa verktyg det möjligt för teamet att identifiera vilka aspekter av tumörutseendet på APTw‑bilderna modellerna förlitade sig mest på vid gradbestämning.
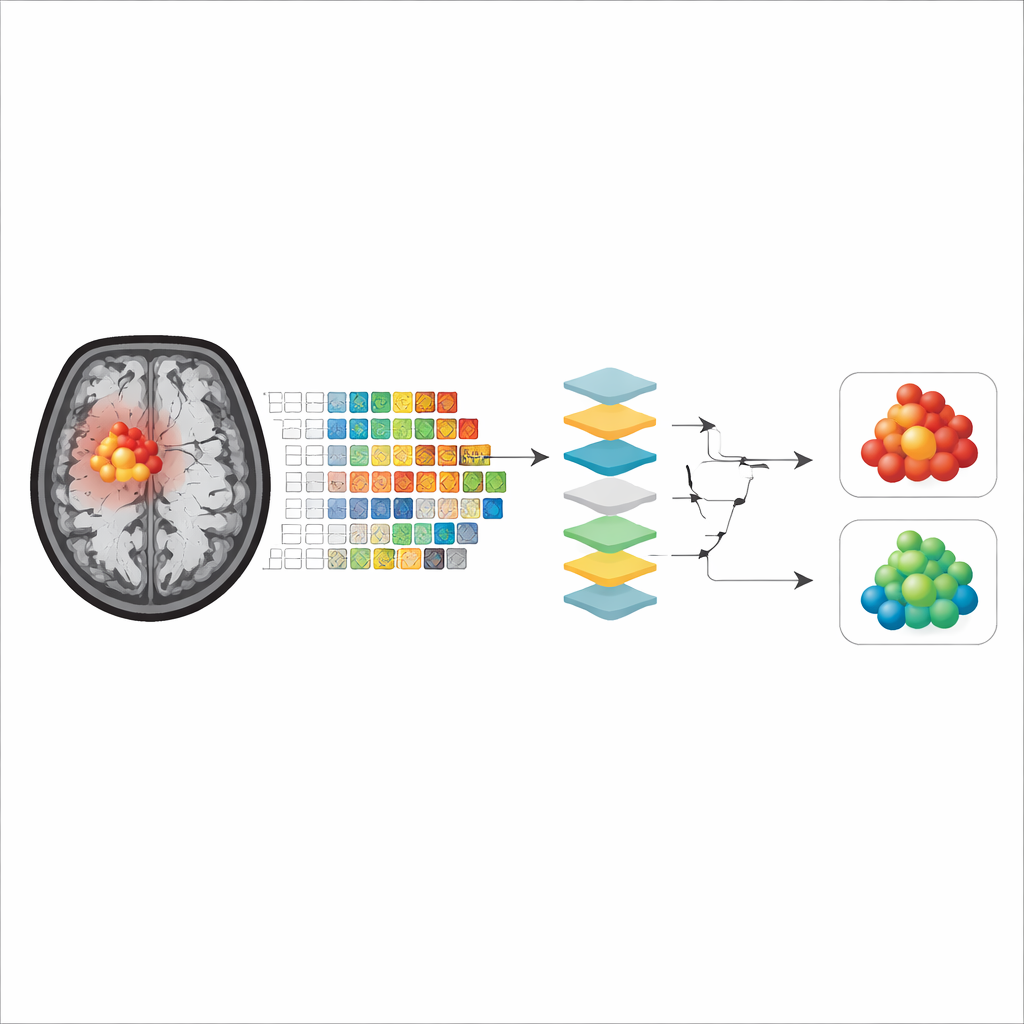
Vad modellerna faktiskt tittar på
Över alla modeller och förklarbarhetsmetoder framträdde två huvudgrupper av egenskaper som viktigast. Den första beskrev tumörens form, särskilt hur väl tumörkonturen motsvarade en slät, regelbunden form kontra att vara oregelbunden och ojämn. Den andra fångade hur fläckigt eller enhetligt APTw‑signalen var inuti tumören, vilket speglar den interna blandningen av vävnadstyper. Intressant nog, när modeller tränades enbart på den kontrast‑förstärkande kärnan dominerade formegenskaper ofta för vissa algoritmer, medan när den omgivande svullnaden inkluderades blev mått på intern signalojämnhet mer inflytelserika, eller vice versa beroende på modell. Sammantaget visade modeller som fokuserade på den förstärkande tumörkärnan något bättre noggrannhet, vilket tyder på att denna region bättre representerar den verkliga tumörvävnaden med färre förväxlingsfaktorer från nekros eller ödem.
Begränsningar och framtida riktningar
Studien har flera praktiska begränsningar. Patientgruppen innehöll relativt få låggradiga tumörer, så modellerna utformades för att skilja grad 4‑tumörer från alla andra sammanslagna i stället för att separera varje enskild grad. Data kom också från ett enda sjukhus, och APTw‑bilderna hade relativt tjocka skivor, vilket kan begränsa hur exakt vissa formegenskaper kan mätas. Trots dessa begränsningar var fynden konsekventa över olika förklarbarhetsmetoder, vilket stöder idén att oregelbundna tumörgränser och ojämna interna signalmönster är centrala bildsignaler som modellerna använder för att känna igen mycket aggressiva gliom.
Vad detta innebär för patienter och läkare
Förenklat visar arbetet att datormodeller kan använda detaljerade mönster dolda i avancerade MR‑skanningar för att skilja aggressiva hjärntumörer från mindre farliga, och det klargör vilka visuella tecken i bilderna som ligger bakom dessa beslut. Genom att lyfta fram betydelsen av tumörform och intern fläckighet på APTw‑skanningar, och genom att visa att dessa ledtrådar kan förklaras transparent, förflyttar studien icke‑invasiv gradbestämning närmare klinisk tillämpning. Om resultaten valideras i större, multicenterstudier kan sådana förklarbara AI‑verktyg hjälpa läkare att planera behandling säkrare och snabbare, ibland minska behovet av riskfyllda biopsier och ge patienter tydligare information baserad endast på skanningar.
Citering: Gao, X., Wang, J. The explainability of radiomic-based machine learning models for brain glioma grading on amide proton transfer-weighted images. Sci Rep 16, 14539 (2026). https://doi.org/10.1038/s41598-026-44963-x
Nyckelord: bilddiagnostik av hjärngliom, radiomik, förklarbar AI, MRI‑biomarkörer, tumörgradbestämning