Clear Sky Science · ja
アミドプロトン移動強調画像に基づく放射線オミクス機械学習モデルの脳神経膠腫グレーディングにおける説明可能性
この研究が重要な理由
膠腫と呼ばれる脳腫瘍は、比較的ゆっくり増大するものから非常に攻撃的なものまで幅があります。従来、医師は手術や生検で腫瘍の一部を採取し顕微鏡で調べることで危険性を判断してきました。その方法は侵襲的で医学的リスクを伴い、不均一な腫瘍の最も攻撃的な部分を見逃す可能性があります。本研究は、高度なMRI検査と人工知能を組み合わせることで膠腫を非侵襲的にグレード付けできるかを検証し、さらに重要なことに、コンピュータモデルがどのように判断しているかを説明可能にすることで医師が結果を信頼し解釈できるようにすることを目指しています。
手術をせずに脳内部をのぞく
研究者らは、組織の化学的環境に敏感な特殊なMRI法であるアミドプロトン移動強調(APTw)イメージングに着目しました。以前の研究でAPTw画像は高悪性度と低悪性度の膠腫を区別できることが示されていましたが、その成功の理由は完全には解明されていませんでした。本研究では、未治療の脳膠腫を有する102人の患者が手術で腫瘍が摘出され病理医によってグレード付けされる前に、APTwを含むMRI検査を受けました。研究チームはこれらのスキャンを用いて、病理医の判断を画像データだけで模倣することを目標に、最も攻撃的な腫瘍(グレード4)をそれ以外の腫瘍から分離するコンピュータモデルを訓練しました。
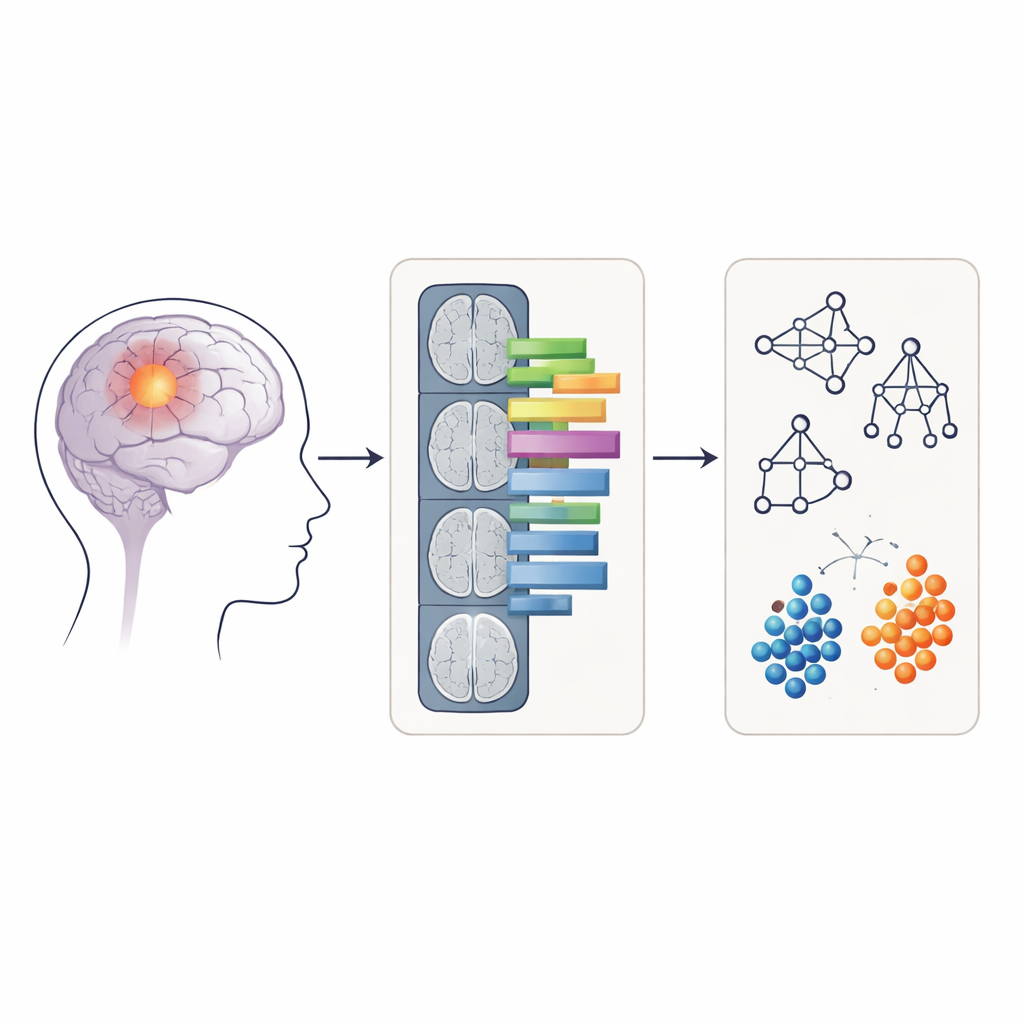
画像を測定可能なパターンに変換する
生のMRI画像を直接モデルに入力する代わりに、研究者らはラジオミクスという手法を用いて医療画像を数百の数値特徴に変換しました。これらの特徴は、腫瘍の輪郭が丸いか不規則か、あるいは信号強度が腫瘍内で均一か斑状かといった性質を記述します。各患者について、APTw画像上の2種類の領域からラジオミクス特徴が抽出されました:造影効果を示す腫瘍核のみと、腫瘍核と周囲の浮腫組織を含むより広い領域です。ランダムフォレスト、サポートベクターマシン、ナイーブベイズ、ロジスティック回帰という4つの一般的な機械学習法がこれらの特徴で訓練および検証され、腫瘍をグレード4か否かに分類する精度が評価されました。
人工知能のブラックボックスを開く
多くの強力な機械学習モデルは「ブラックボックス」のように動作し、正しい予測を行ってもその根拠を示しません。これに対処するため、著者らは3つの説明可能性ツールを適用しました。シャープレイ値は各特徴が特定の予測にどれだけ寄与したかを推定し、置換重要度はある特徴をシャッフルしたときに性能がどれだけ低下するかを測定し、アンカーと呼ばれる手法はモデルの決定を支持する単純なルール状の特徴組み合わせを見つけます。これらを併用することで、チームは膠腫のグレーディング時にモデルがAPTw画像上のどの外見的側面を最も頼りにしているかを特定できました。
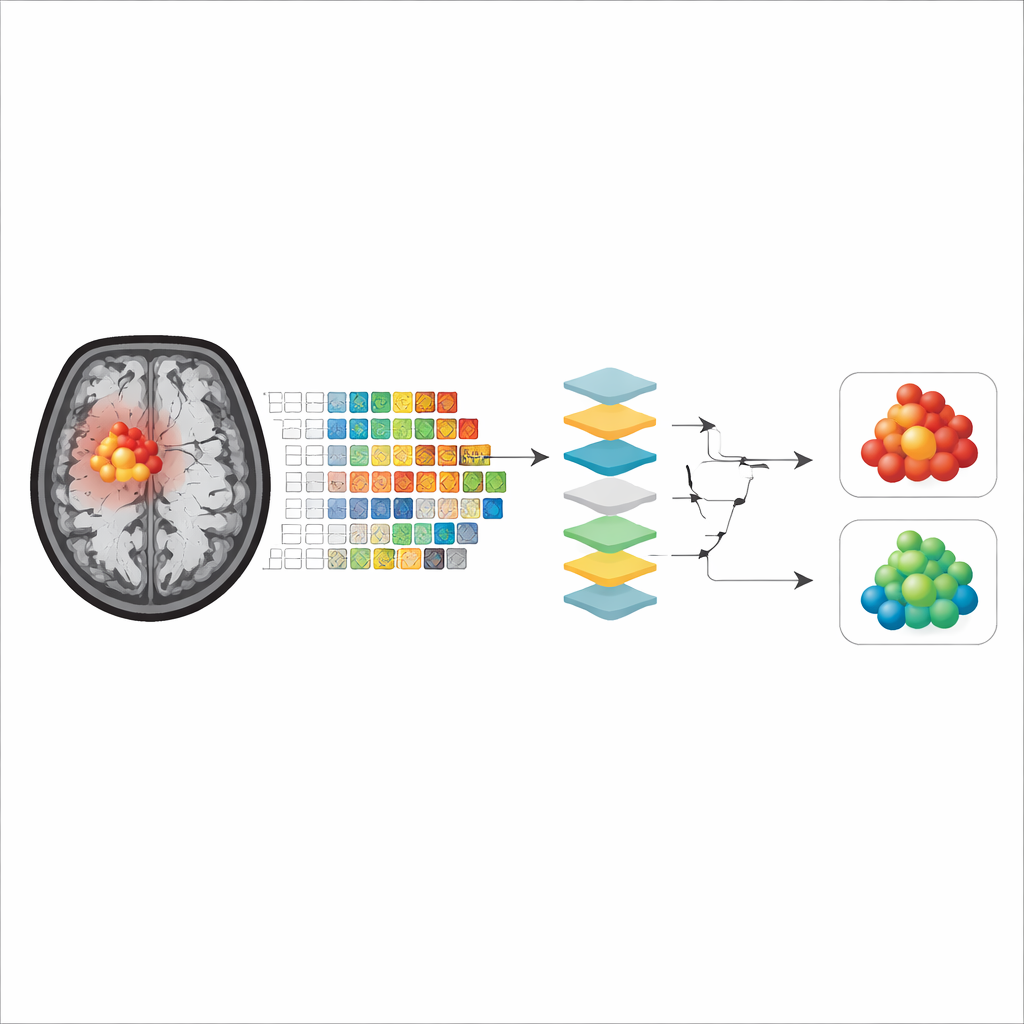
モデルが実際に注目しているもの
全モデルと説明可能性手法を通じて、重要な特徴は主に2つのグループに分かれて浮かび上がりました。1つは腫瘍の形状を記述するもので、輪郭が滑らかで規則的に近いか、不規則で凸凹しているかを示します。もう1つは腫瘍内部のAPTw信号が斑状か均一かをとらえるもので、組織タイプの内部混在を反映します。興味深いことに、モデルを造影効果を示す核だけで訓練した場合は形状特徴があるアルゴリズムで優勢になることが多く、周囲の浮腫を含めた場合は内部信号の不均一性を示す指標がより影響力を持つようになることがあり、モデルによってその傾向は変わりました。全体として、造影腫瘍核に焦点を当てたモデルのほうがやや高い精度を示し、壊死や浮腫の影響が少ないためこの領域がより真の腫瘍組織を反映していることが示唆されます。
限界と今後の方向性
本研究にはいくつかの実用的制約があります。患者群には低悪性度腫瘍が比較的少なかったため、モデルは全てのグレードを個別に分離するのではなく、グレード4を他の全てと区別するよう設計されました。またデータは単一病院由来であり、APTw画像のスライス厚が比較的厚かったため、いくつかの形状特徴の精度が制約を受ける可能性があります。これらの制約にもかかわらず、結果は異なる説明可能性手法間で一貫しており、不規則な腫瘍境界と内部信号の不均一性が高悪性度膠腫を認識する主要な画像手がかりであるという考えを支持しています。
患者と医師にとっての意味
簡潔に言えば、本研究はコンピュータモデルが高度なMRI検査に潜む詳細なパターンを用いて攻撃的な脳腫瘍をより低危険度の腫瘍と識別できること、そして画像内のどの視覚的手がかりがその判断を導くかを明らかにしたことを示しています。APTwスキャンでの腫瘍形状と内部斑状性の重要性を強調し、これらの手がかりが透明に説明可能であることを示したことで、非侵襲的な腫瘍グレーディングは臨床応用に一歩近づきました。より大規模で多施設の検証が行われれば、このような説明可能なAIツールは医師の治療計画をより安全かつ迅速に支援し、場合によっては危険を伴う生検の必要性を減らし、患者にスキャンのみを基にしたより明確な情報を提供できる可能性があります。
引用: Gao, X., Wang, J. The explainability of radiomic-based machine learning models for brain glioma grading on amide proton transfer-weighted images. Sci Rep 16, 14539 (2026). https://doi.org/10.1038/s41598-026-44963-x
キーワード: 脳膠腫イメージング, ラジオミクス, 説明可能なAI, MRIバイオマーカー, 腫瘍グレーディング