Clear Sky Science · de
Die Erklärbarkeit radiomikbasierter Machine‑Learning‑Modelle zur Klassifizierung von Hirngliomen in amide‑Proton‑Transfer‑gewichteten Bildern
Warum diese Forschung wichtig ist
Hirntumoren vom Typ Gliom können von relativ langsam wachsend bis hochgradig aggressiv reichen. Traditionell bestimmen Ärzte die Gefährlichkeit eines Glioms, indem sie während einer Operation oder Biopsie ein Stück des Tumors entnehmen und es mikroskopisch untersuchen. Dieser Ansatz ist invasiv, mit medizinischen Risiken verbunden und kann die aggressivsten Bereiche eines sehr heterogenen Tumors übersehen. Diese Studie untersucht, ob fortgeschrittene MRT‑Aufnahmen in Kombination mit künstlicher Intelligenz Gliome nichtinvasiv einstufen können — und, was entscheidend ist, wie die Computermodelle ihre Entscheidungen treffen, damit Ärzte den Ergebnissen vertrauen und sie interpretieren können.
Blick ins Gehirn ohne Operation
Die Forschenden konzentrierten sich auf eine spezielle MRT‑Methode namens amide‑Proton‑Transfer‑gewichtete (APTw) Bildgebung, die empfindlich gegenüber dem chemischen Umfeld des Hirngewebes ist. Frühere Arbeiten hatten gezeigt, dass APTw‑Bilder zwischen hoch‑ und niedriggradigen Gliomen unterscheiden können, die Gründe für diesen Erfolg waren jedoch nicht vollständig geklärt. In dieser Studie wurden 102 Patientinnen und Patienten mit unbehandelten Hirngliomen vor der chirurgischen Entfernung der Tumoren MRT‑Untersuchungen einschließlich APTw‑Aufnahmen unterzogen. Die Tumoren wurden anschließend von Pathologen klassifiziert. Das Team nutzte diese Aufnahmen, um Computer‑Modelle zu trainieren, die die aggressivsten Tumoren (Grad 4) von allen anderen unterscheiden sollten, mit dem Ziel, das Urteil des Pathologen allein auf Basis der Bilddaten zu nachzuahmen.
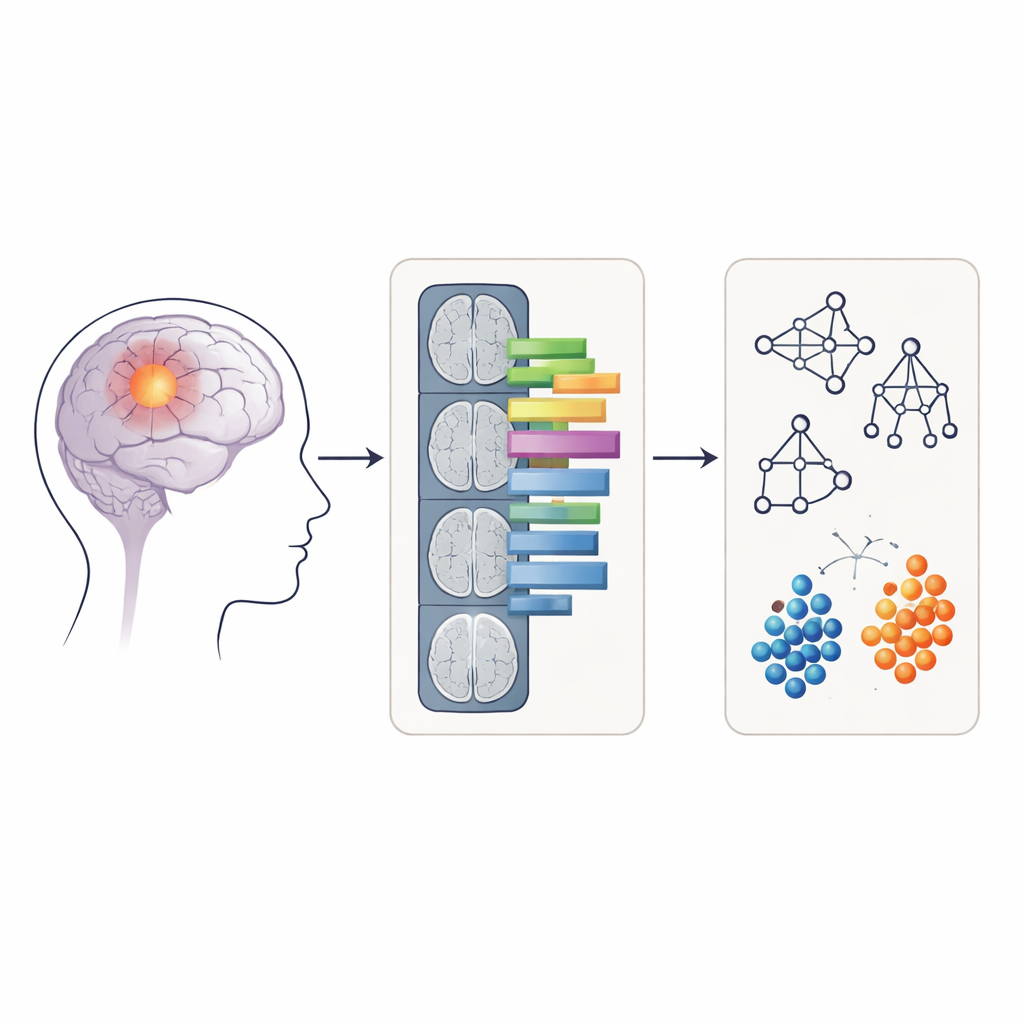
Bilder in messbare Muster verwandeln
Anstatt rohe MRT‑Bilder direkt in die Modelle zu füttern, verwendeten die Forschenden eine Technik namens Radiomik, die medizinische Bilder in hunderte numerische Merkmale umwandelt. Diese Merkmale beschreiben etwa, wie rund oder unregelmäßig der Tumor erscheint und wie gleichmäßig oder ungleichmäßig die Signalintensität innerhalb des Tumors verteilt ist. Für jeden Patienten wurden radiomische Merkmale aus zwei Arten von Regionen auf den APTw‑Bildern extrahiert: nur dem kontrastmittelaufnehmenden Tumorkern und einer größeren Region, die sowohl den kontrastaufnehmenden Kern als auch das umgebende geschwollene Gewebe (Ödem) einschloss. Vier gängige Machine‑Learning‑Methoden — Random Forest, Support Vector Machine, Naive Bayes und logistische Regression — wurden mit diesen Merkmalen trainiert und getestet, um zu prüfen, wie genau sie Tumoren als Grad‑4 oder nicht‑Grad‑4 klassifizieren konnten.
Die Blackbox der künstlichen Intelligenz öffnen
Viele leistungsstarke Machine‑Learning‑Modelle agieren wie „Blackboxen“: Sie liefern korrekte Vorhersagen, ohne offenzulegen, wie sie dazu gelangt sind. Um dem zu begegnen, wendeten die Autorinnen und Autoren drei Erklärbarkeitswerkzeuge an. Shapley‑Werte schätzen, wie viel jedes Merkmal zu einer einzelnen Vorhersage beiträgt, Permutations‑Importance misst, wie stark die Leistung abnimmt, wenn ein Merkmal zufällig vertauscht wird, und eine Methode namens Anchors findet einfache, regelähnliche Kombinationen von Merkmalen, die ausreichen, um eine Modellentscheidung zu stützen. Zusammengenommen ermöglichten diese Werkzeuge dem Team, zu identifizieren, auf welche Aspekte des Tumorbildes in APTw‑Aufnahmen die Modelle bei der Einstufung von Gliomen am stärksten vertrauen.
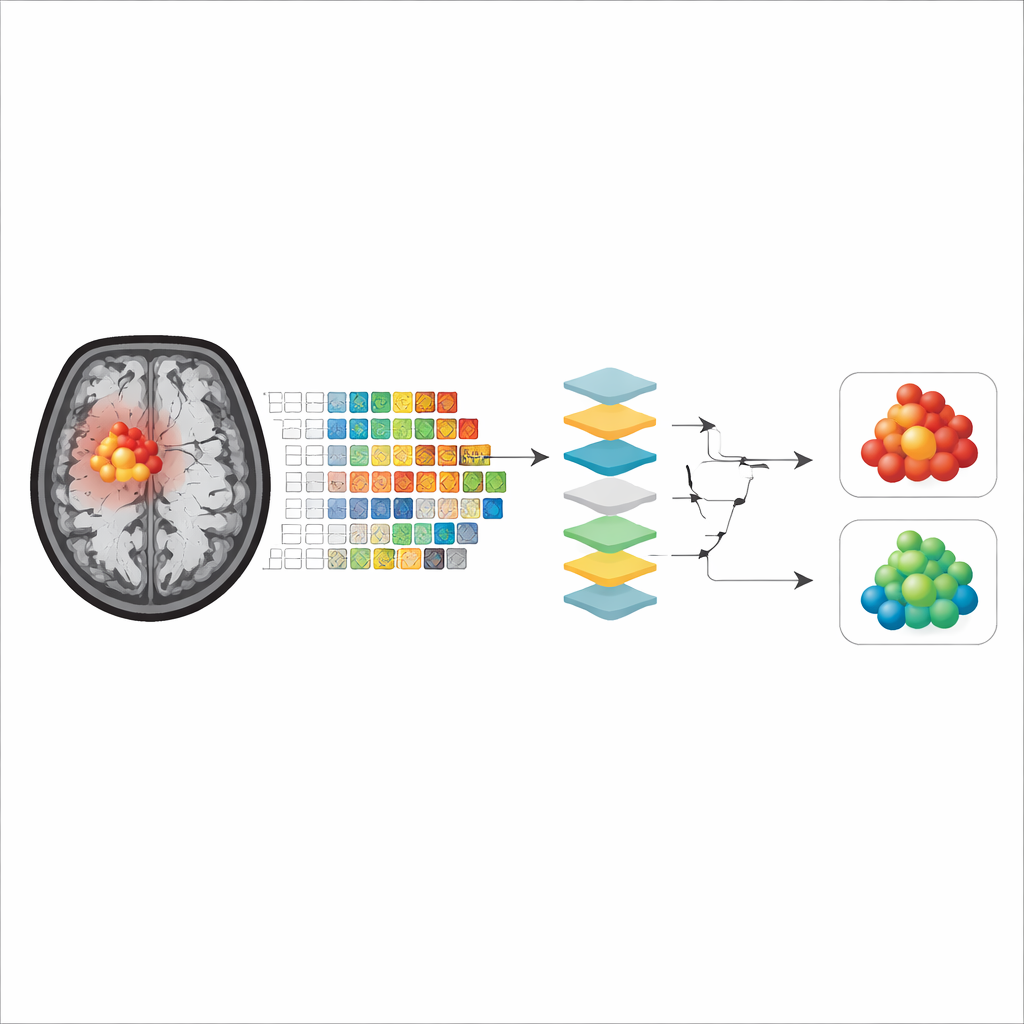
Worauf die Modelle tatsächlich achten
Über alle Modelle und Erklärbarkeitsmethoden hinweg kristallisierten sich zwei Hauptgruppen von Merkmalen als am wichtigsten heraus. Die erste beschrieb die Tumorform, insbesondere wie nahe die Tumorbegrenzung einer glatten, regelmäßigen Form entsprach versus unregelmäßig und uneben zu sein. Die zweite fasste zusammen, wie fleckig oder homogen das APTw‑Signal innerhalb des Tumors war, was die innere Mischung von Gewebetypen widerspiegelt. Interessanterweise dominierten bei Modellen, die nur auf dem kontrastaufnehmenden Kern trainiert wurden, häufig Formmerkmale bei einigen Algorithmen, während bei Einbeziehung des umgebenden Ödems Messgrößen der internen Signalungleichmäßigkeit einflussreicher wurden — oder umgekehrt, je nach Modell. Insgesamt zeigten Modelle, die sich auf den kontrastaufnehmenden Tumorkern konzentrierten, eine geringfügig bessere Genauigkeit, was darauf hindeutet, dass diese Region das tatsächliche Tumorgewebe besser darstellt und weniger durch Nekrose oder Ödem verfälscht wird.
Beschränkungen und zukünftige Richtungen
Die Studie hat mehrere praktische Einschränkungen. Die Patientengruppe enthielt relativ wenige niedriggradige Tumoren, sodass die Modelle darauf ausgelegt waren, Grad‑4‑Tumoren von allen anderen zusammen zu unterscheiden, anstatt jeden Grad einzeln zu trennen. Die Daten stammten zudem aus einem einzigen Krankenhaus und die APTw‑Bilder hatten relativ dicke Schichten, was die genaue Messung mancher Formmerkmale einschränken kann. Trotz dieser Beschränkungen waren die Ergebnisse über verschiedene Erklärbarkeitsmethoden hinweg konsistent, was die Annahme stützt, dass unregelmäßige Tumorgrenzen und ungleichmäßige interne Signalmuster zentrale Bildhinweise sind, die Modelle zur Erkennung hochgradiger Gliome nutzen.
Was das für Patientinnen, Patienten und Ärzte bedeutet
Kurz gesagt zeigt diese Arbeit, dass Computer‑Modelle detaillierte, in fortgeschrittenen MRT‑Aufnahmen verborgene Muster nutzen können, um aggressive Hirntumoren von weniger gefährlichen zu unterscheiden, und sie erklärt, welche visuellen Hinweise in den Bildern diese Entscheidungen antreiben. Indem die Studie die Bedeutung von Tumorform und innerer Fleckigkeit auf APTw‑Aufnahmen hervorhebt und demonstriert, dass sich diese Hinweise transparent erklären lassen, rückt sie die nichtinvasive Tumorbeurteilung näher an die klinische Realität. Werden solche erklärbaren KI‑Werkzeuge in größeren, multizentrischen Studien validiert, könnten sie Ärztinnen und Ärzten helfen, die Behandlung sicherer und schneller zu planen, mitunter das Risiko von Biopsien zu reduzieren und Patientinnen und Patienten klarere Informationen allein auf Basis von Aufnahmen zu geben.
Zitation: Gao, X., Wang, J. The explainability of radiomic-based machine learning models for brain glioma grading on amide proton transfer-weighted images. Sci Rep 16, 14539 (2026). https://doi.org/10.1038/s41598-026-44963-x
Schlüsselwörter: Bildgebung von Hirngliomen, Radiomik, erklärbare KI, MRT‑Biomarker, Tumor‑Grading