Clear Sky Science · ru
Объяснимость моделей машинного обучения на основе радиомики для градации глиом головного мозга на APTw‑изображениях
Почему это исследование важно
Глиомы головного мозга могут варьироваться от относительно медленно растущих до крайне агрессивных. Традиционно врачи оценивают опасность глиомы, беря кусочек опухоли во время операции или биопсии и исследуя его под микроскопом. Этот подход инвазивен, связан с медицинскими рисками и может пропустить наиболее агрессивные участки неоднородной опухоли. В этом исследовании изучают, можно ли с помощью продвинутых МР‑сканов в сочетании с искусственным интеллектом проводить неинвазивную градацию глиом — и что важно, поясняют, как компьютерные модели принимают решения, чтобы врачи могли доверять и интерпретировать результаты.
Заглянуть в мозг без операции
Исследователи сосредоточились на специальном методе МРТ — амид‑протон‑переносно‑взвешенной (APTw) визуализации, чувствительной к химической среде мозговой ткани. Ранние работы показали, что APTw‑изображения способны различать высоко‑ и низкодифференцированные глиомы, но причины такого успеха были поняты не полностью. В этом исследовании 102 пациента с нелечеными глиомами прошли МРТ, включая APTw‑сканы, до хирургического удаления опухолей и их градации патологами. Затем команда использовала эти сканы для обучения компьютерных моделей, которые должны были отделять наиболее агрессивные опухоли (4‑й уровень) от всех остальных, пытаясь имитировать суждение патолога, опираясь только на данные визуализации.
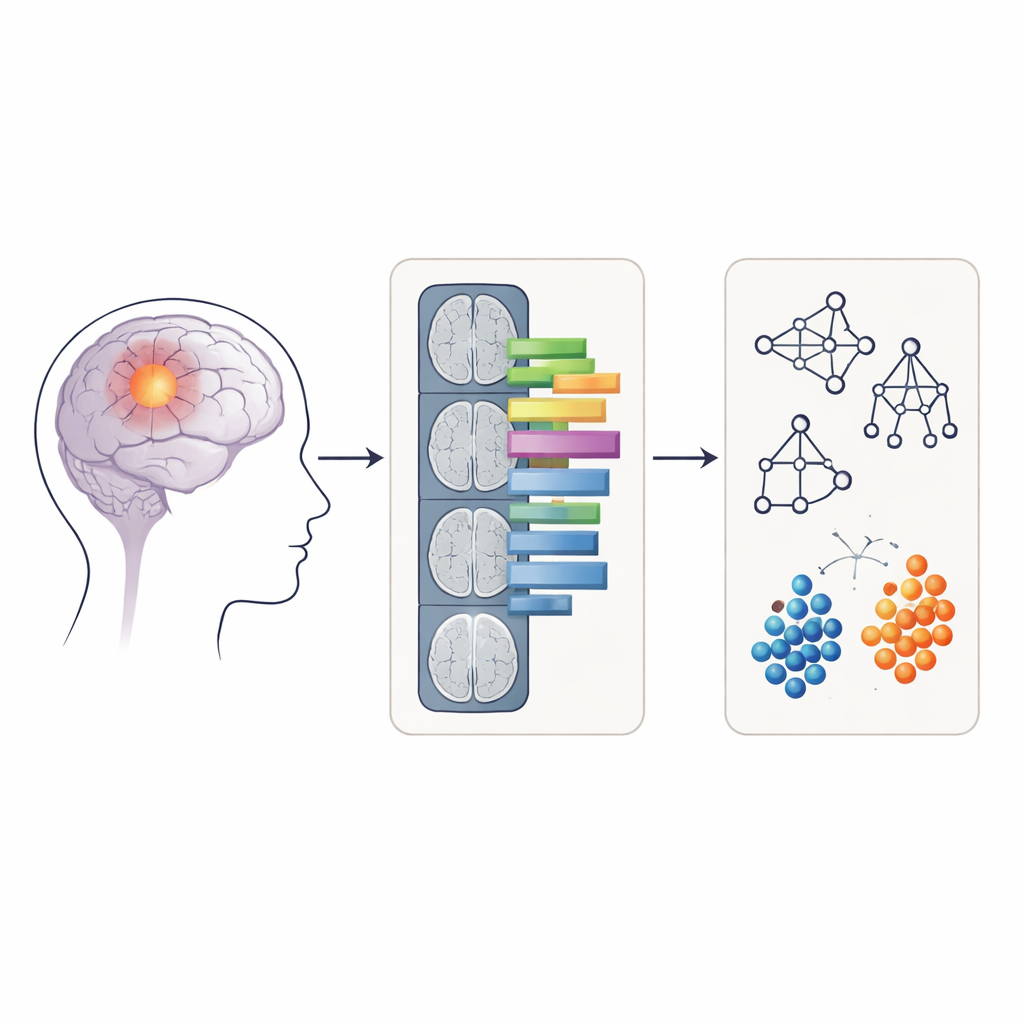
Преобразование изображений в измеримые шаблоны
Вместо того чтобы напрямую подавать сырые МР‑изображения в модель, исследователи использовали метод радиомики, который преобразует медицинские изображения в сотни числовых признаков. Эти признаки описывают, например, насколько округлой или неправильной выглядит опухоль и насколько равномерно распределена интенсивность сигнала внутри неё. Для каждого пациента радиомические признаки извлекали из двух типов областей на APTw‑изображениях: только контрастно‑насыщенного ядра опухоли и более широкой зоны, включающей ядро и окружающий отёк. Четыре распространённых метода машинного обучения — случайный лес, метод опорных векторов, наивный байесовский классификатор и логистическая регрессия — были обучены и протестированы на этих признаках, чтобы оценить, насколько точно они классифицируют опухоли как 4‑й степени или нет.
Открывая «чёрный ящик» искусственного интеллекта
Многие мощные модели машинного обучения функционируют как «чёрные ящики», делая верные предсказания, не раскрывая, как они к ним пришли. Чтобы решить эту проблему, авторы применили три инструмента объяснимости. Значения Шэпли оценивают вклад каждого признака в конкретное предсказание, permutation importance измеряет, насколько ухудшается качество при перемешивании признака, а метод anchors находит простые, похожие на правила комбинации признаков, достаточные для поддержки решения модели. В совокупности эти инструменты позволили команде определить, на какие аспекты вида опухоли на APTw‑сканах модели опирались в первую очередь при градации глиом.
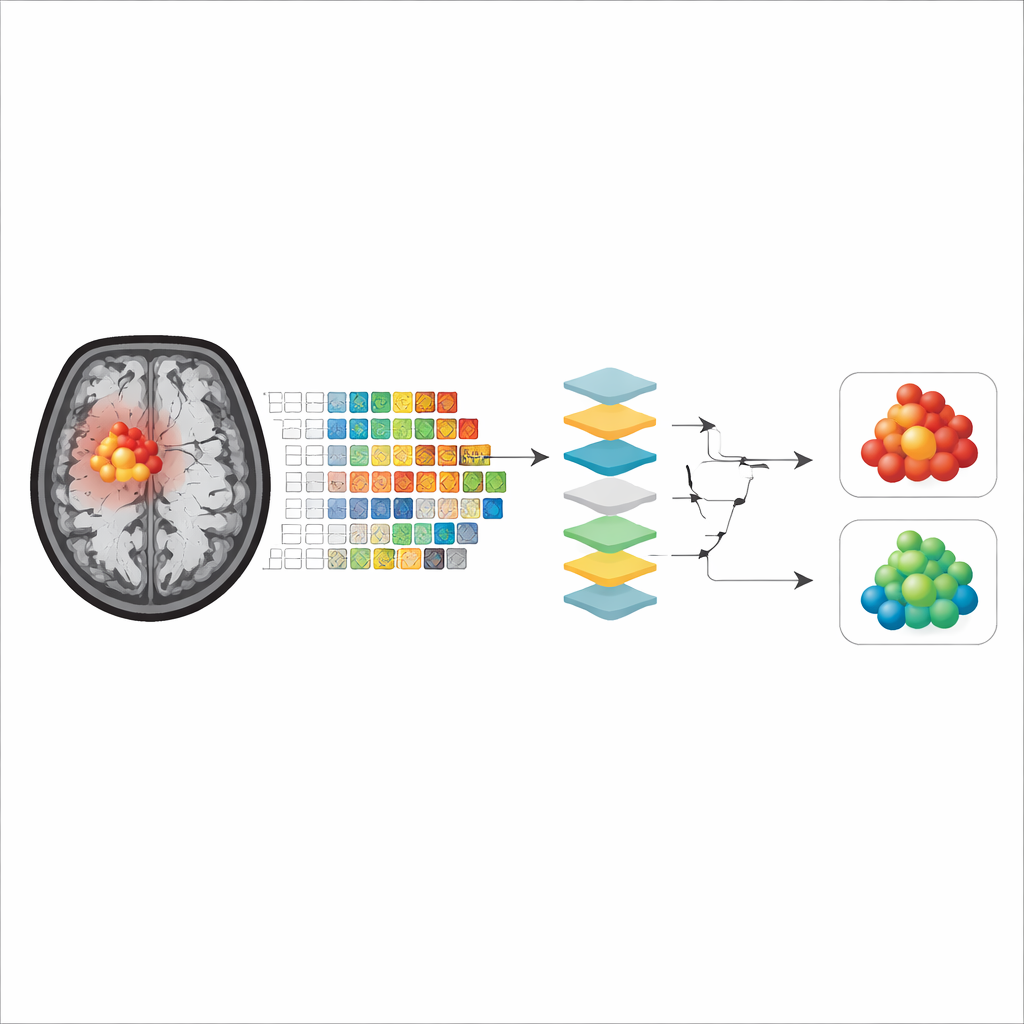
На что модели действительно обращают внимание
Во всех моделях и при использовании разных методов объяснимости выявились две основные группы признаков, оказавшиеся наиболее важными. Первая описывает форму опухоли, в частности, насколько контур опухоли близок к гладкой, правильной форме или, наоборот, является неправильным и неровным. Вторая отражает, насколько пятнистым или однородным является APTw‑сигнал внутри опухоли, что показывает внутреннее сочетание типов ткани. Интересно, что при обучении моделей только на контрастно‑насыщенном ядре для некоторых алгоритмов доминировали признаки формы, тогда как при включении окружающей отёчной ткани меры внутренней неоднородности сигнала становились более влиятельными, или наоборот в зависимости от модели. В целом модели, фокусировавшиеся на ядре усиливающейся части опухоли, показали слегка лучшую точность, что указывает на то, что эта зона лучше представляет истинную опухолевую ткань с меньшим влиянием некроза или отёка.
Ограничения и направления дальнейших исследований
У исследования есть несколько практических ограничений. В группе пациентов было относительно мало низкодифференцированных опухолей, поэтому модели разрабатывали для различения 4‑й степени от всех остальных, а не для отдельного различения каждой степени. Данные также поступали из одной клиники, а APTw‑изображения имели относительно толстые срезы, что может ограничивать точность измерения некоторых признаков формы. Несмотря на эти ограничения, результаты были последовательны при использовании разных методов объяснимости, что подтверждает идею о том, что неправильные границы опухоли и внутренние неоднородные сигналы являются ключевыми визуальными подсказками, которые модели используют для распознавания высокоагрессивных глиом.
Что это значит для пациентов и врачей
Проще говоря, эта работа показывает, что компьютерные модели могут использовать детальные закономерности, скрытые в продвинутых МР‑сканах, чтобы отличать агрессивные опухоли мозга от менее опасных, и при этом раскрывает, какие визуальные признаки в изображениях обуславливают такие решения. Подчёркивая важность формы опухоли и внутренней пятнистости на APTw‑сканах и демонстрируя, что эти подсказки можно прозрачно объяснить, исследование приближает неинвазивную градацию опухолей к клинической практике. При валидации на больших многоцентровых выборках такие объяснимые инструменты ИИ могут помочь врачам планировать лечение более безопасно и оперативно, иногда снижая необходимость рискованных биопсий и давая пациентам более ясную информацию, основанную только на снимках.
Цитирование: Gao, X., Wang, J. The explainability of radiomic-based machine learning models for brain glioma grading on amide proton transfer-weighted images. Sci Rep 16, 14539 (2026). https://doi.org/10.1038/s41598-026-44963-x
Ключевые слова: визуализация глиом головного мозга, радиомика, объяснимая ИИ, МРТ‑биомаркеры, градация опухоли