Clear Sky Science · zh
使用经验证的稳定性指示HPLC方法对阿西替尼降解产物的结构与计算机安全评估以确定致突变性杂质
为何抗癌药片的安全性会随时间变化
许多现代抗癌药需连续服用数月甚至数年,这意味着药片必须在较长时间内保持安全与有效。但药物会逐步降解,产生原始配方中不存在的新分子。本研究考察了白血病药物阿西替尼在严苛条件下的分解途径、如何检测这些微量降解产物,以及计算工具是否提示其中任何一种可能具有危害性。
追踪抗癌药物的分解过程
阿西替尼是一种用于慢性髓性白血病的靶向口服药物。与所有药物一样,它在生产、贮存或体内可能与酸、碱、光、热或氧发生反应。这些反应会产生降解产物,其中少数可能具有“致突变性”,即可能损伤DNA。监管机构现在要求公司查找此类副产物、鉴定其结构并将其含量严格控制。研究团队旨在绘制阿西替尼的降解图谱,识别出现的新分子,并开发一种实用的实验室方法来分离与测定药物及其杂质。
构建能够检测极低痕量的实验方法
研究组设计并优化了一种液相色谱方法,这是一种制药实验室中广泛使用的分离技术。他们测试了多种色谱柱和溶剂体系,最终选择出能将阿西替尼与三种已知致突变性杂质及多种未知降解产物清晰分离的条件。该方法按照国际指南进行了准确性、灵敏度和稳健性验证,能够检测非常低的杂质水平,并在条件略有变化时仍表现出一致性。这使其适用于日常质量控制,确保每批药片满足严格的纯度限值。
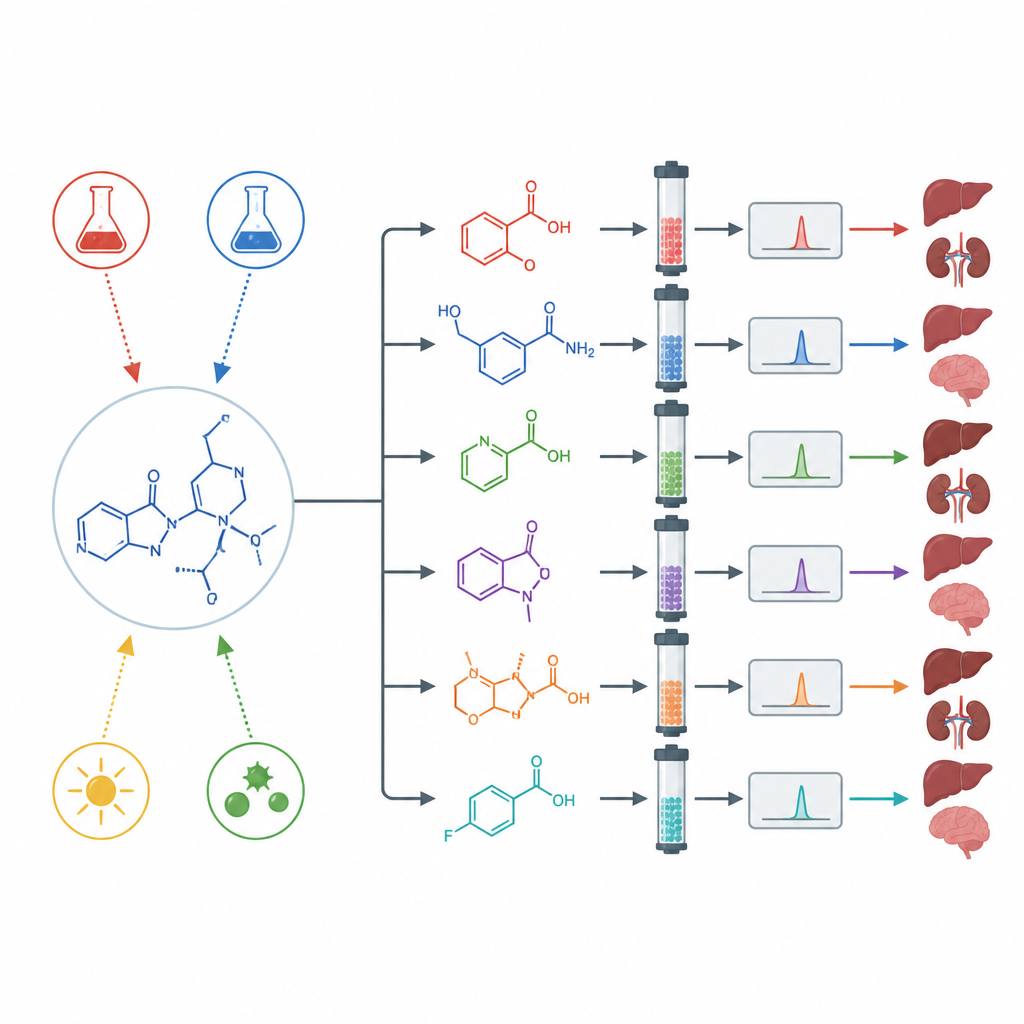
对药物施加应力以暴露隐匿的副产物
为了观察阿西替尼在极端条件下的表现,科学家们进行了“加速降解”试验。他们将药物暴露于强酸、强碱、氧化剂、热、水和包括紫外在内的强光下。在中性水、热和普通光照条件下,药物几乎没有变化。但在酸碱、氧化剂和紫外光作用下,它明显发生分解并形成若干不同的新分子。研究团队利用制备性分离、高分辨质谱和核磁共振技术分离并解析了各类应力下形成的多种降解产物的结构。
利用计算模型窥探安全性与行为
鉴于对每个降解产物进行动物或人体测试既耗时又昂贵,研究人员转而使用基于化学结构估算毒性和类药性行为的计算(in silico)工具。这些程序表明,所有已鉴定的降解产物总体落在中等毒性区间,但预测风险存在差异。有些产物显示出可能影响肝、肾或神经系统的信号,而另一些看起来更为温和。若干产物被标记为具有潜在致癌或致基因损伤的活性,它们在体内分布和进入大脑的能力差异很大。虽然这些预测并不能作为危害的确证,但它们突出了哪些杂质更值得进行深入的实验检测。
对患者和制药商的意义
对于服用阿西替尼的患者来说,本研究并不改变药物的用法,但它加强了围绕该药的安全保障。作者表明阿西替尼在常规贮存条件下相对稳定,但在更严苛的条件下可形成若干具有特征性的降解产物。他们提供了用于监测这些分子的详细实验方法以及关于哪些产物可能更令人担忧的初步计算线索。总体而言,这项工作有助于生产商和监管机构追踪阿西替尼的长期安全性,并为评估其他随时间变化的抗癌药物提供了范式。
引用: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
关键词: 阿西替尼, 药物降解, 致突变性杂质, HPLC 分析, 计算机毒性预测