Clear Sky Science · de
Strukturelle und In-silico-Sicherheitsbewertung der Abbauprodukte von Asciminib mit einer validierten, stabilitätsanzeigenden HPLC-Methode zur Bestimmung genotoxischer Verunreinigungen
Warum die Sicherheit einer Krebs-Tablette sich mit der Zeit verändert
Viele moderne Krebsmedikamente werden über Monate oder Jahre eingenommen, was bedeutet, dass die Tabletten über lange Zeiträume sicher und wirksam bleiben müssen. Arzneimittel bauen sich jedoch langsam ab und erzeugen dabei neue Moleküle, die ursprünglich nicht zur Rezeptur gehörten. Diese Studie untersucht, wie das Leukämie-Medikament Asciminib unter belastenden Bedingungen zerfällt, wie die winzigen Abbauprodukte nachgewiesen werden können und ob Computermodelle darauf hindeuten, dass eines davon schädlich sein könnte.
Ein Krebsmedikament verfolgen, während es zerfällt
Asciminib ist eine zielgerichtete orale Therapie gegen eine Blutkrebserkrankung namens chronische myeloische Leukämie. Wie alle Arzneistoffe kann es während der Herstellung, Lagerung oder im Körper mit Säuren, Basen, Licht, Hitze oder Sauerstoff reagieren. Diese Reaktionen erzeugen Abbauprodukte, von denen einige „genotoxisch“ sein können, also DNA-Schäden verursachen könnten. Regulierungsbehörden verlangen inzwischen, dass Hersteller solche Nebenprodukte suchen, identifizieren und ihre Gehalte streng kontrollieren. Die Forschenden wollten kartieren, wie Asciminib zerfällt, die neu entstehenden Moleküle identifizieren und einen praxisnahen Labortest entwickeln, der den Wirkstoff und seine Verunreinigungen trennt und misst.
Eine Labormethode bauen, die selbst kleinste Spuren erkennt
Das Team entwarf und optimierte eine Flüssigchromatographie-Methode, eine Arbeitspferd-Trenntechnik in pharmazeutischen Laboren. Sie testeten mehrere Säulen und Lösungsmittelgemische, bevor sie Bedingungen auswählten, die Asciminib sauber von drei bekannten genotoxischen Verunreinigungen und einer Reihe unbekannter Abbauprodukte trennen. Die Methode wurde hinsichtlich Genauigkeit, Sensitivität und Robustheit gemäß internationalen Richtlinien geprüft. Sie konnte sehr niedrige Verunreinigungsniveaus erkennen und zeigte konsistente Leistung, selbst wenn die Bedingungen leicht variierten. Damit eignet sie sich für die routinemäßige Qualitätskontrolle, um sicherzustellen, dass jede Tablettencharge strenge Reinheitsgrenzen einhält.
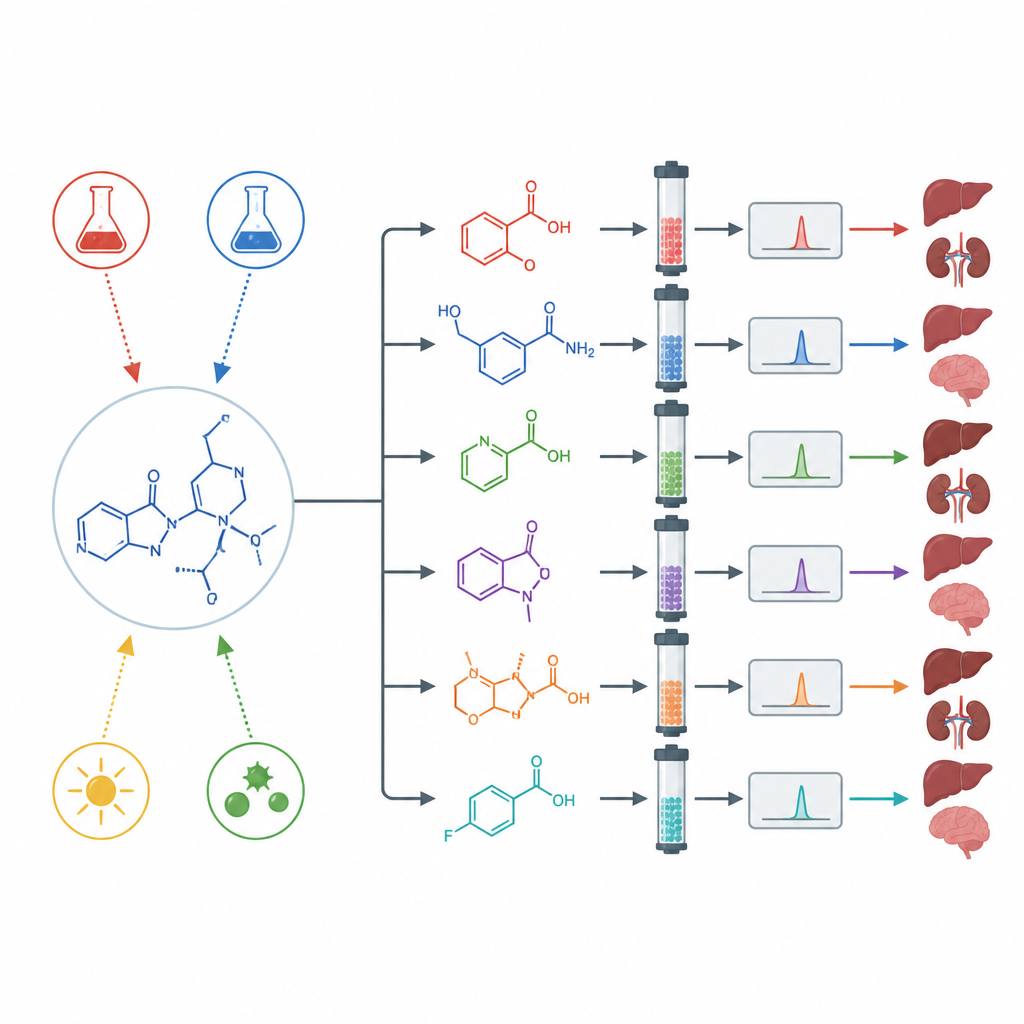
Das Medikament belasten, um verborgene Nebenprodukte sichtbar zu machen
Um zu sehen, wie Asciminib unter extremen Bedingungen reagiert, führten die Wissenschaftler sogenannte Forced-Degradation-Tests durch. Sie setzten den Wirkstoff starker Säure, starker Base, oxidierenden Chemikalien, Hitze, Wasser und hellem Licht einschließlich Ultraviolett aus. Unter neutralem Wasser, Hitze und normalem Licht veränderte sich das Medikament kaum. Unter Säure-, Base-, Oxidationsmitteln und UV-Licht zerfiel es jedoch deutlich und bildete mehrere unterschiedliche neue Moleküle. Mithilfe präparativer Trennverfahren, hochauflösender Massenspektrometrie und Kernspinresonanz isolierte das Team mehrere Abbauprodukte und bestimmte ihre Strukturen für die verschiedenen Stressbedingungen.
Sicherheit und Verhalten mit Computermodellen abschätzen
Da die Untersuchung jedes Abbauprodukts in Tieren oder Menschen langsam und teuer ist, nutzten die Forschenden in-silico-Werkzeuge, die Toxizität und arzneistoffähnliches Verhalten aus der chemischen Struktur abschätzen. Diese Programme deuteten an, dass alle identifizierten Abbauprodukte in einen Bereich moderater Toxizität fallen, ihre prognostizierten Risiken jedoch unterschiedlich sind. Einige zeigten Hinweise auf mögliche Leber-, Nieren- oder Nervensystemeffekte, andere wirkten milder. Mehrere wurden wegen potenzieller karzinogener oder genotoxischer Aktivität markiert, und ihre Fähigkeit, sich im Körper zu verteilen und in das Gehirn einzudringen, variierte stark. Obwohl diese Vorhersagen keinen Schadensnachweis darstellen, heben sie hervor, welche Verunreinigungen einer besonders genauen experimentellen Prüfung bedürfen.
Was das für Patientinnen, Patienten und Hersteller bedeutet
Für Personen, die Asciminib einnehmen, ändert die Studie nichts an der Anwendung des Medikaments, stärkt aber das Sicherheitsnetz um das Präparat. Die Autorinnen und Autoren zeigen, dass Asciminib unter normalen Lagerbedingungen relativ stabil ist, unter raueren Bedingungen jedoch eine Handvoll charakteristischer Abbauprodukte bilden kann. Sie liefern eine detaillierte Labormethode, um diese Moleküle zu überwachen, sowie erste computerbasierte Hinweise darauf, welche davon besorgniserregender sein könnten. Zusammen hilft diese Arbeit Herstellern und Aufsichtsbehörden, die Langzeitsicherheit von Asciminib zu überwachen, und bietet eine Vorlage zur Bewertung anderer Krebsmedikamente im Alterungsprozess.
Zitation: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
Schlüsselwörter: asciminib, Arzneimittelabbau, genotoxische Verunreinigungen, HPLC-Analyse, in-silico Toxizität