Clear Sky Science · es
Evaluación estructural y en silico de los productos de degradación de asciminib con un método HPLC indicativo de estabilidad validado para la determinación de impurezas genotóxicas
Por qué la seguridad de una pastilla contra el cáncer cambia con el tiempo
Muchos fármacos modernos contra el cáncer se toman durante meses o años, por lo que las píldoras deben mantenerse seguras y eficaces a lo largo del tiempo. Pero los medicamentos se degradan lentamente, generando nuevas moléculas que no formaban parte de la formulación original. Este estudio examina cómo el fármaco contra la leucemia asciminib se descompone bajo condiciones agresivas, cómo detectar los diminutos productos de degradación y si las herramientas informáticas sugieren que alguno de ellos podría ser perjudicial.
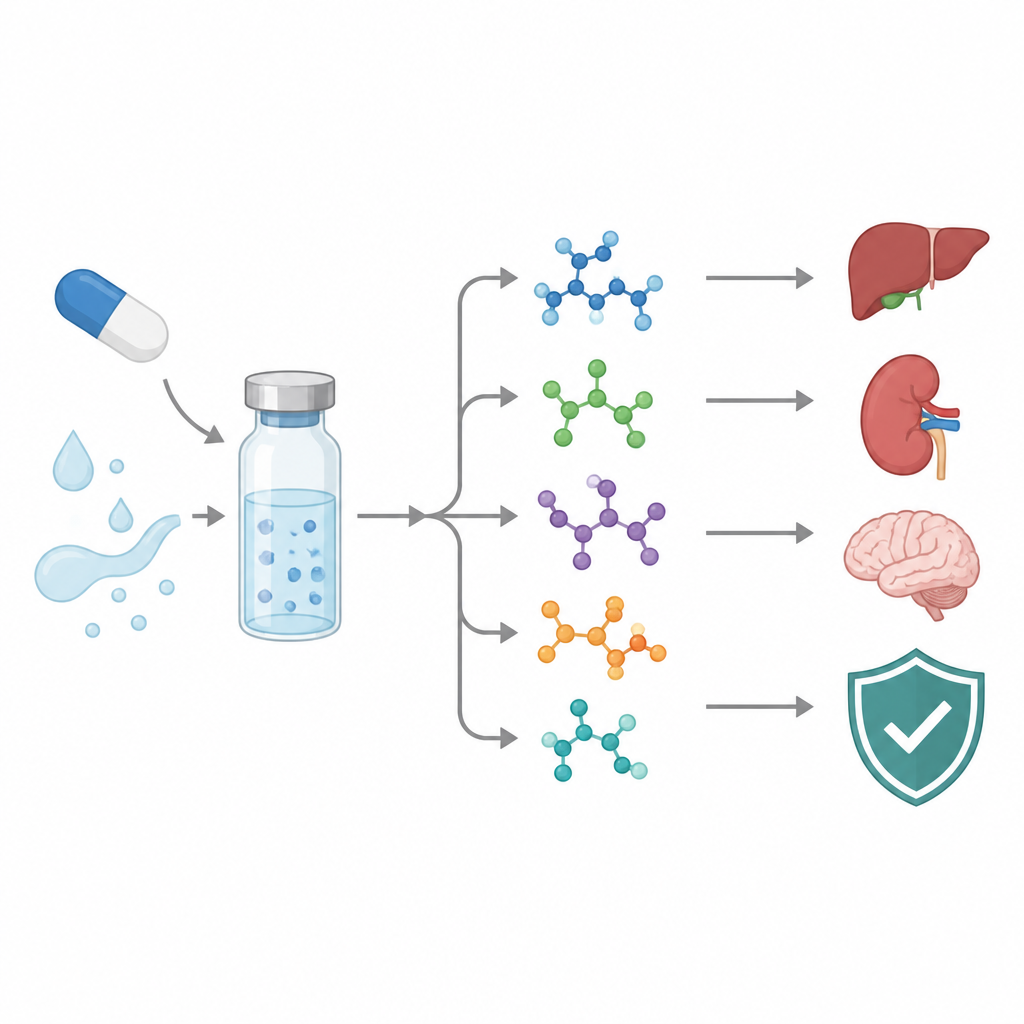
Siguiendo a un fármaco oncológico mientras se descompone
Asciminib es una pastilla dirigida usada para una leucemia llamada leucemia mieloide crónica. Como todos los fármacos, puede reaccionar con ácidos, bases, luz, calor u oxígeno durante la fabricación, el almacenamiento o dentro del organismo. Estas reacciones generan productos de degradación, y algunos pueden ser “genotóxicos”, es decir, capaces de dañar el ADN. Las agencias reguladoras exigen ahora que las empresas busquen esos subproductos, los identifiquen y mantengan sus niveles bajo control estricto. Los investigadores se propusieron mapear cómo se degrada asciminib, identificar las nuevas moléculas que aparecen y desarrollar una prueba de laboratorio práctica que separe y cuantifique el fármaco y sus impurezas.
Desarrollar una prueba de laboratorio capaz de detectar las trazas más pequeñas
El equipo diseñó y afinó un método de cromatografía líquida, una técnica de separación fundamental en laboratorios farmacéuticos. Probaron varias columnas y mezclas de disolventes antes de elegir condiciones que separaron claramente asciminib de tres impurezas genotóxicas conocidas y de una serie de productos de degradación desconocidos. El método se verificó en cuanto a exactitud, sensibilidad y robustez, siguiendo directrices internacionales. Pudo detectar niveles de impurezas muy bajos y mostró un rendimiento consistente incluso cuando las condiciones se variaron ligeramente. Esto lo hace adecuado para el control de calidad rutinario y para asegurar que cada lote de comprimidos cumpla con estrictos límites de pureza.
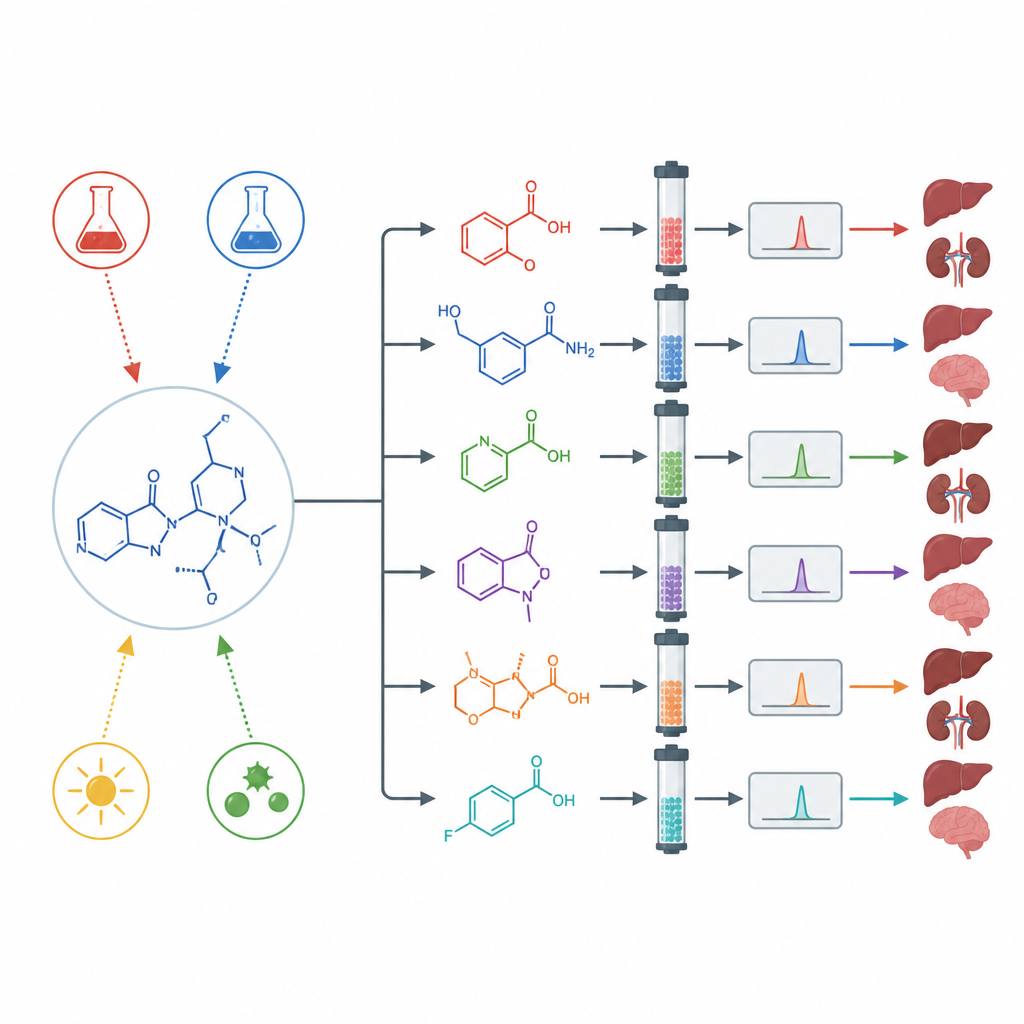
Someter el fármaco a estrés para revelar subproductos ocultos
Para ver cómo se comporta asciminib en condiciones extremas, los científicos realizaron pruebas de “degradación forzada”. Expusieron el fármaco a ácido fuerte, base fuerte, agentes oxidantes, calor, agua y luz intensa, incluida la ultravioleta. En agua neutra, calor y luz normal, el fármaco apenas cambió. Pero bajo ácido, base, agentes oxidantes y luz ultravioleta se degradó de forma notable y formó varias moléculas nuevas y diferenciadas. Mediante separación preparativa, espectrometría de masas de alta resolución y resonancia magnética nuclear, el equipo aisló y determinó las estructuras de múltiples productos de degradación formados en cada tipo de estrés.
Examinar la seguridad y el comportamiento con modelos informáticos
Dado que ensayar cada producto de degradación en animales o personas es lento y costoso, los investigadores recurrieron a herramientas in silico que estiman la toxicidad y el comportamiento tipo fármaco a partir de la estructura química. Estos programas sugirieron que todos los productos de degradación identificados se sitúan en una franja de toxicidad moderada, aunque sus riesgos previstos difieren. Algunos mostraron señales de posibles efectos hepáticos, renales o sobre el sistema nervioso, mientras que otros parecieron más leves. Varios fueron señalados por potencial cancerígeno o dañino para los genes, y su capacidad para moverse por el cuerpo y atravesar la barrera hematoencefálica varió considerablemente. Aunque estas predicciones no prueban daño, señalan qué impurezas merecen el escrutinio experimental más cercano.
Qué significa esto para pacientes y fabricantes
Para las personas que toman asciminib, el estudio no cambia el uso del fármaco, pero sí refuerza la red de seguridad a su alrededor. Los autores muestran que asciminib es bastante estable en condiciones normales de almacenamiento, pero puede formar un puñado de productos de degradación distintivos bajo condiciones más duras. Proporcionan un método de laboratorio detallado para vigilar estas moléculas y pistas iniciales basadas en ordenador sobre cuáles podrían ser más preocupantes. En conjunto, este trabajo ayuda a fabricantes y reguladores a seguir la seguridad a largo plazo de asciminib y ofrece un modelo para evaluar otros fármacos oncológicos conforme envejecen.
Cita: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
Palabras clave: asciminib, degradación de fármacos, impurezas genotóxicas, análisis HPLC, toxicidad in silico