Clear Sky Science · pt
Avaliação estrutural e in silico da segurança dos produtos de degradação do asciminibe com um método HPLC validado indicativo de estabilidade para determinação de impurezas genotóxicas
Por que a segurança de um comprimido contra o câncer muda ao longo do tempo
Muitos medicamentos oncológicos modernos são tomados por meses ou anos, o que significa que os comprimidos precisam permanecer seguros e eficazes por longos períodos. Mas os medicamentos se degradam lentamente, produzindo novas moléculas que não faziam parte da fórmula original. Este estudo investiga como o fármaco para leucemia asciminibe se desfaz sob condições agressivas, como detectar os mínimos produtos de degradação e se ferramentas computacionais indicam que algum deles pode ser prejudicial.
Acompanhando um fármaco oncológico enquanto ele se desfaz
O asciminibe é um comprimido direcionado usado no tratamento de uma neoplasia sanguínea chamada leucemia mieloide crônica. Como todos os fármacos, ele pode reagir com ácidos, bases, luz, calor ou oxigênio durante a fabricação, armazenamento ou no interior do corpo. Essas reações geram produtos de degradação, e alguns podem ser “genotóxicos”, ou seja, capazes de danificar o DNA. As agências reguladoras hoje exigem que as empresas identifiquem esses subprodutos, determinem o que são e mantenham seus níveis sob controle rigoroso. Os pesquisadores propuseram-se a mapear como o asciminibe se degrada, identificar as novas moléculas que surgem e desenvolver um teste de laboratório prático que separe e meça o fármaco e suas impurezas.
Construindo um teste de laboratório capaz de detectar os menores vestígios
A equipe concebeu e ajustou um método de cromatografia líquida, uma técnica de separação amplamente usada em laboratórios farmacêuticos. Testaram várias colunas e misturas de solventes antes de escolher condições que separassem claramente o asciminibe de três impurezas genotóxicas conhecidas e de uma série de produtos de degradação desconhecidos. O método foi verificado quanto à exatidão, sensibilidade e robustez, seguindo diretrizes internacionais. Ele foi capaz de detectar níveis muito baixos de impurezas e apresentou desempenho consistente mesmo quando as condições foram ligeiramente alteradas. Isso o torna adequado para controle de qualidade rotineiro, garantindo que cada lote de comprimidos atenda a limites rigorosos de pureza.
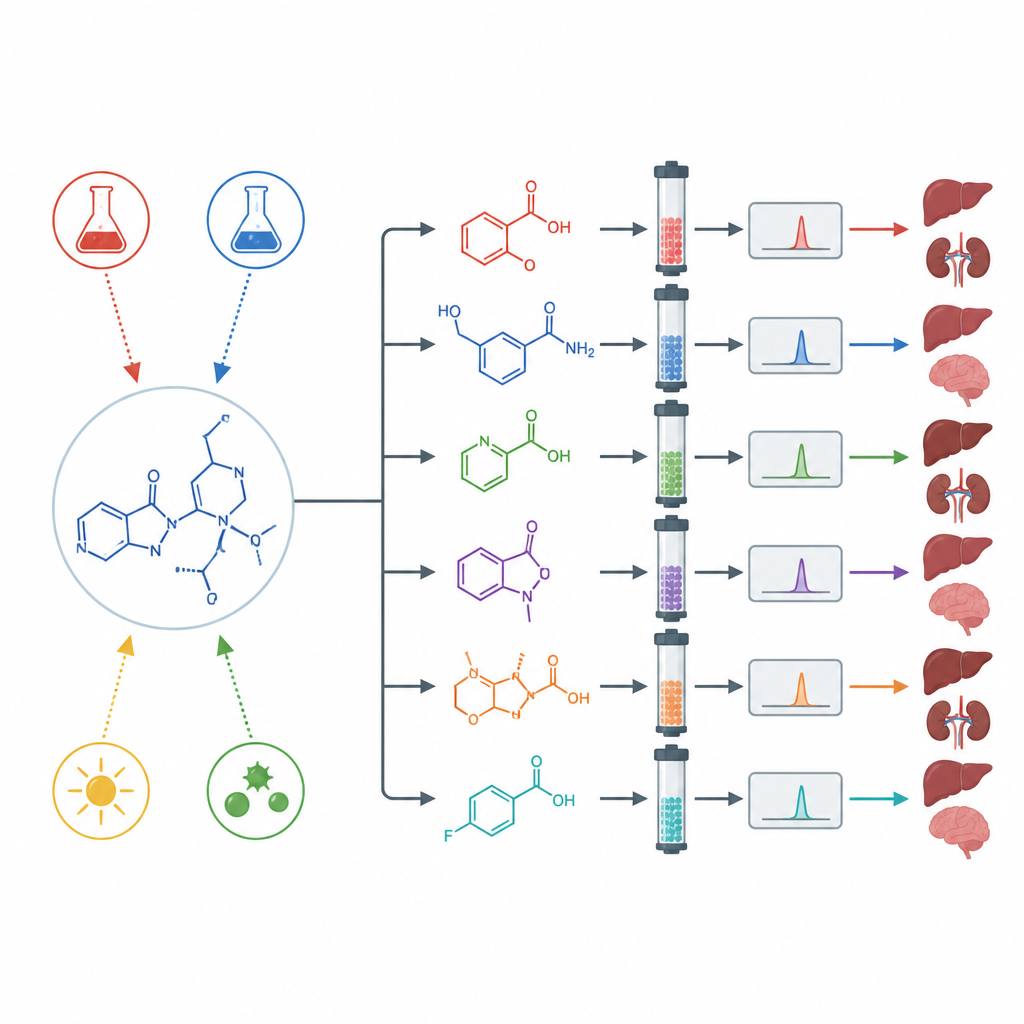
Submetendo o fármaco a estresse para revelar subprodutos ocultos
Para avaliar o comportamento do asciminibe sob condições extremas, os cientistas realizaram testes de “degradação forçada”. Eles expuseram o fármaco a ácido forte, base forte, agentes oxidantes, calor, água e luz intensa, incluindo ultravioleta. Em água neutra, calor e luz normal, o fármaco pouco se alterou. Mas sob ácido, base, agentes oxidantes e luz ultravioleta, ele se degradou de forma marcante e formou várias novas moléculas distintas. Usando separação preparativa, espectrometria de massa de alta resolução e ressonância magnética nuclear, a equipe isolou e elucidou as estruturas de múltiplos produtos de degradação formados em cada tipo de estresse.
Conferindo segurança e comportamento com modelos computacionais
Como testar experimentalmente cada produto de degradação em animais ou em humanos é demorado e caro, os pesquisadores recorreram a ferramentas in silico que estimam toxicidade e propriedades farmacocinéticas a partir da estrutura química. Esses programas sugeriram que todos os produtos de degradação identificados se enquadram em uma faixa de toxicidade moderada, embora seus riscos previstos variem. Alguns exibiram sinais de possíveis efeitos no fígado, nos rins ou no sistema nervoso, enquanto outros pareceram mais brandos. Vários foram sinalizados por potencial carcinogênico ou genotóxico, e sua capacidade de se distribuir pelo corpo e atravessar a barreira hematoencefálica variou amplamente. Embora essas predições não constituam prova de dano, elas destacam quais impurezas merecem escrutínio experimental mais aprofundado.
O que isso significa para pacientes e fabricantes
Para pessoas que tomam asciminibe, o estudo não altera o modo de uso do medicamento, mas reforça a rede de segurança ao seu redor. Os autores mostram que o asciminibe é bastante estável em condições normais de armazenamento, mas pode formar um punhado de produtos de degradação característicos sob condições mais severas. Eles apresentam um método laboratorial detalhado para monitorar essas moléculas e pistas iniciais, baseadas em simulações computacionais, sobre quais delas podem ser mais preocupantes. Em conjunto, esse trabalho ajuda fabricantes e reguladores a acompanhar a segurança a longo prazo do asciminibe e oferece um modelo para avaliar outros medicamentos oncológicos à medida que envelhecem.
Citação: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
Palavras-chave: asciminibe, degradação de fármacos, impurezas genotóxicas, análise por HPLC, toxicidade in silico