Clear Sky Science · fr
Évaluation structurale et in silico de la sécurité des produits de dégradation de l’asciminib avec une méthode HPLC validée indiquant la stabilité pour la détermination des impuretés génotoxiques
Pourquoi la sécurité d’un comprimé anticancéreux évolue avec le temps
De nombreux médicaments anticancéreux modernes sont pris pendant des mois voire des années, ce qui implique que les comprimés doivent rester sûrs et efficaces sur de longues périodes. Mais les médicaments se décomposent lentement, produisant de nouvelles molécules qui ne faisaient pas partie de la formulation initiale. Cette étude examine comment l’asciminib, médicament contre la leucémie, se dégrade sous des conditions agressives, comment détecter les très faibles produits de dégradation, et si des outils informatiques suggèrent que l’un d’eux pourrait être nocif.
Suivre un médicament anticancéreux qui se désagrège
L’asciminib est un comprimé ciblé utilisé contre une hémopathie appelée leucémie myéloïde chronique. Comme tous les médicaments, il peut réagir avec des acides, des bases, la lumière, la chaleur ou l’oxygène lors de la fabrication, du stockage ou à l’intérieur du corps. Ces réactions créent des produits de dégradation, dont quelques-uns peuvent être « génotoxiques », c’est‑à‑dire susceptibles d’endommager l’ADN. Les autorités exigent désormais que les industriels recherchent ces sous-produits, identifient leur nature et maintiennent leurs niveaux sous contrôle strict. Les chercheurs se sont donc attachés à cartographier la dégradation de l’asciminib, identifier les nouvelles molécules apparues et développer un test de laboratoire pratique qui sépare et quantifie le médicament et ses impuretés.
Mettre au point un test de laboratoire capable de détecter les traces les plus faibles
L’équipe a conçu et optimisé une méthode de chromatographie liquide, technique de séparation largement utilisée dans les laboratoires pharmaceutiques. Ils ont testé plusieurs colonnes et mélanges de solvants avant de retenir des conditions qui séparent nettement l’asciminib de trois impuretés génotoxiques connues et d’une gamme de produits de dégradation inconnus. La méthode a été vérifiée pour son exactitude, sa sensibilité et sa robustesse, conformément aux lignes directrices internationales. Elle permet de détecter des niveaux d’impuretés très faibles et a montré des performances constantes même lorsque les conditions étaient légèrement modifiées. Cela la rend adaptée au contrôle qualité de routine pour garantir que chaque lot de comprimés respecte des limites de pureté strictes.
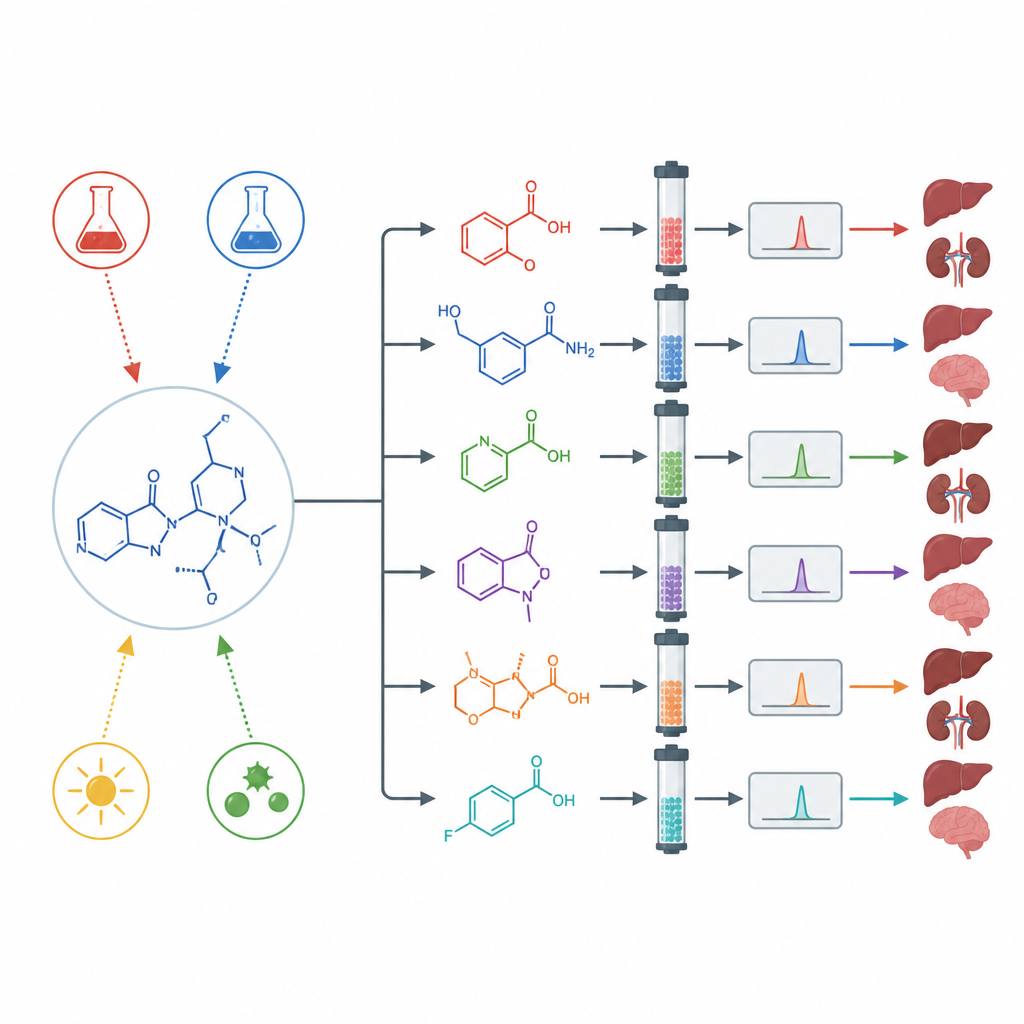
Soumettre le médicament à des contraintes pour révéler des sous-produits cachés
Pour observer le comportement de l’asciminib en conditions extrêmes, les scientifiques ont réalisé des essais de « dégradation forcée ». Ils ont exposé le médicament à des acides forts, des bases fortes, des agents oxydants, à la chaleur, à l’eau et à une lumière intense incluant les ultraviolets. En milieu aqueux neutre, à la chaleur et sous lumière normale, le composé a peu changé. Mais sous l’action d’acide, de base, d’agents oxydants et de lumière ultraviolette, il s’est décomposé de manière notable et a formé plusieurs nouvelles molécules distinctes. À l’aide de séparations préparatives, de spectrométrie de masse haute résolution et de résonance magnétique nucléaire, l’équipe a isolé et élucidé les structures de multiples produits de dégradation formés pour chaque type de contrainte.
Regarder la sécurité et le comportement avec des modèles informatiques
Parce que tester chaque produit de dégradation chez l’animal ou chez l’humain est long et coûteux, les chercheurs ont eu recours à des outils in silico qui estiment la toxicité et le comportement pharmacologique à partir de la structure chimique. Ces programmes ont suggéré que tous les produits de dégradation identifiés se situent dans une gamme de toxicité modérée, mais que leurs risques prédits diffèrent. Certains ont montré des signaux possibles d’effets sur le foie, les reins ou le système nerveux, tandis que d’autres paraissaient plus bénins. Plusieurs ont été signalés pour un potentiel cancérogène ou génotoxique, et leur capacité à se distribuer dans l’organisme et à traverser la barrière hémato‑encéphalique variait largement. Bien que ces prédictions ne constituent pas une preuve de nocivité, elles mettent en lumière les impuretés qui méritent la vigilance expérimentale la plus poussée.
Ce que cela signifie pour les patients et les fabricants
Pour les personnes prenant de l’asciminib, l’étude ne modifie pas l’usage du médicament, mais renforce le filet de sécurité autour de celui‑ci. Les auteurs montrent que l’asciminib est assez stable en conditions de stockage normales mais peut former une poignée de produits de dégradation caractéristiques sous conditions plus sévères. Ils fournissent une méthode de laboratoire détaillée pour surveiller ces molécules et des indications initiales issues de calculs sur celles qui pourraient être les plus préoccupantes. Ensemble, ces travaux aident les fabricants et les autorités à suivre la sécurité à long terme de l’asciminib et offrent un modèle pour évaluer d’autres médicaments anticancéreux au fil du vieillissement.
Citation: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
Mots-clés: asciminib, dégradation des médicaments, impuretés génotoxiques, analyse HPLC, toxicité in silico