Clear Sky Science · it
Valutazione strutturale e in silico della sicurezza dei prodotti di degradazione di asciminib con un metodo HPLC convalidato indicativo di stabilità per la determinazione di impurità genotossiche
Perché la sicurezza di una pillola oncologica cambia nel tempo
Molti farmaci oncologici moderni si assumono per mesi o anni, il che implica che le compresse devono rimanere sicure ed efficaci per lunghi periodi. Tuttavia i medicinali si degradano lentamente, generando nuove molecole che non facevano parte della formulazione originale. Questo studio analizza come il farmaco per la leucemia asciminib si scompone in condizioni severe, come rilevare i minuscoli prodotti di degradazione e se strumenti computazionali suggeriscono che alcuni di essi possano essere dannosi.
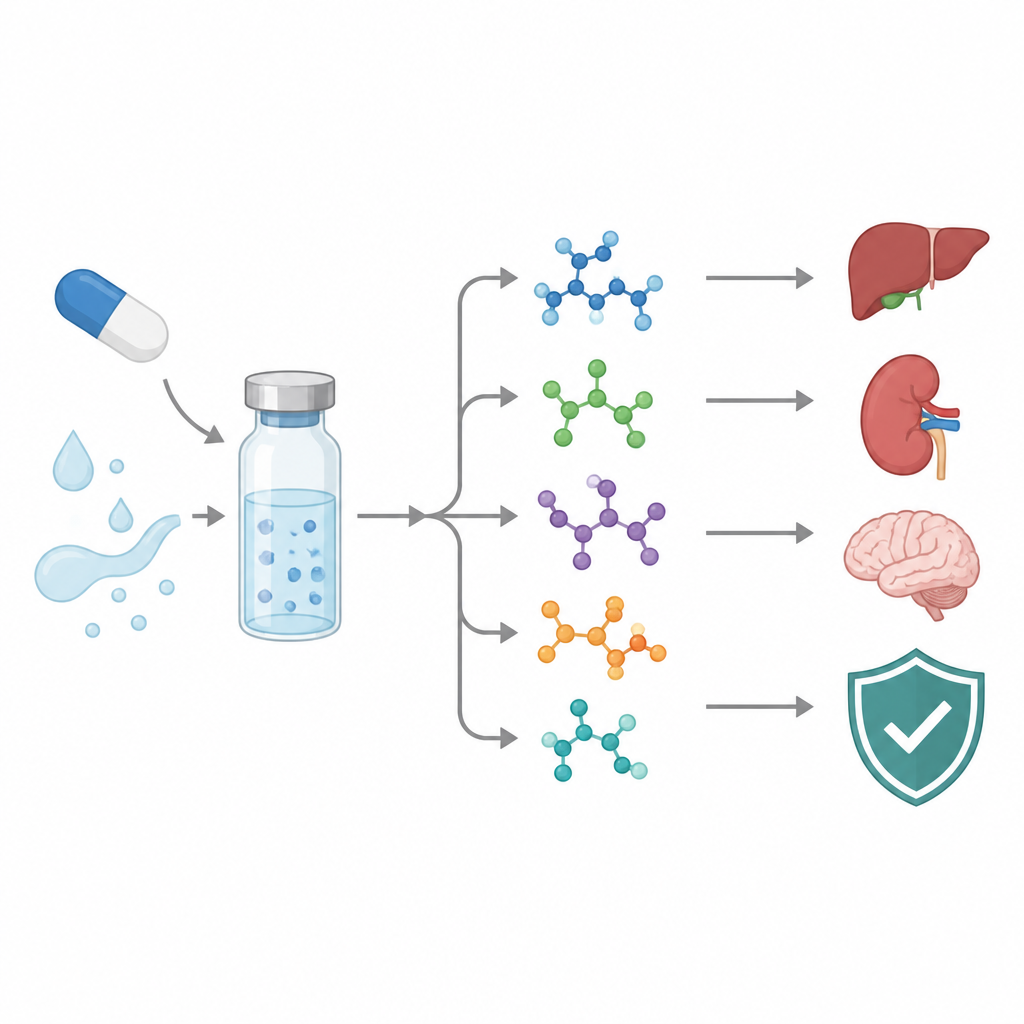
Seguo un farmaco antitumorale mentre si sgretola
Asciminib è una compressa mirata utilizzata per una forma di tumore del sangue chiamata leucemia mieloide cronica. Come tutti i farmaci, può reagire con acidi, basi, luce, calore o ossigeno durante la produzione, lo stoccaggio o all’interno dell’organismo. Queste reazioni generano prodotti di degradazione e alcuni potrebbero essere «genotossici», cioè in grado di danneggiare il DNA. Le autorità regolatorie ora richiedono alle aziende di cercare tali sottoprodotti, identificarli e mantenere i loro livelli sotto stretto controllo. I ricercatori si sono impegnati a mappare come asciminib si degrada, identificare le nuove molecole che compaiono e sviluppare un test di laboratorio pratico che separi e misuri il farmaco e le sue impurità.
Creare un test di laboratorio in grado di rilevare le tracce più minute
Il gruppo ha progettato e affinato un metodo di cromatografia liquida, una tecnica di separazione largamente utilizzata nei laboratori farmaceutici. Hanno provato diverse colonne e miscele di solventi prima di scegliere condizioni che separassero nettamente asciminib da tre note impurità genotossiche e da una serie di prodotti di degradazione non identificati. Il metodo è stato verificato per accuratezza, sensibilità e robustezza, seguendo linee guida internazionali. È in grado di rilevare livelli di impurità molto bassi e ha mostrato prestazioni coerenti anche quando le condizioni erano leggermente variate. Ciò lo rende adatto al controllo qualità di routine per garantire che ogni lotto di compresse rispetti limiti di purezza rigorosi.
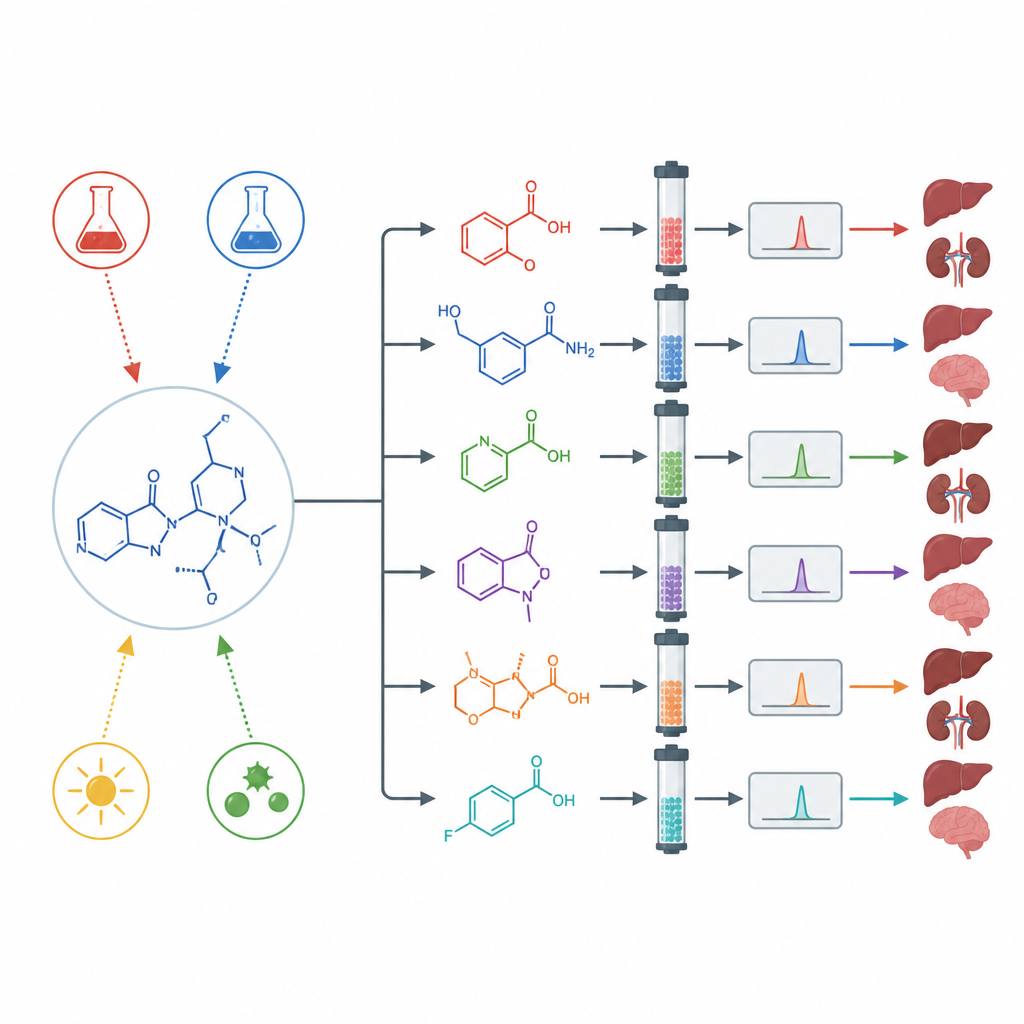
Sottoporre il farmaco a stress per rivelare sottoprodotti nascosti
Per osservare il comportamento di asciminib in condizioni estreme, gli scienziati hanno eseguito test di «degradazione forzata». Hanno esposto il farmaco a acido forte, base forte, agenti ossidanti, calore, acqua e luce intensa, inclusa l’ultravioletto. In condizioni neutre (acqua), al calore e alla luce normale, il farmaco cambiava pochissimo. Ma in presenza di acidi, basi, ossidanti e luce UV si è degradato in modo significativo formando diverse molecole nuove e distinguibili. Utilizzando separazioni preparative, spettrometria di massa ad alta risoluzione e risonanza magnetica nucleare, il team ha isolato e determinato le strutture di molteplici prodotti di degradazione formatisi per ciascun tipo di stress.
Uno sguardo alla sicurezza e al comportamento con modelli computazionali
Poiché testare ogni prodotto di degradazione su animali o persone è lento e costoso, i ricercatori si sono rivolti a strumenti in silico che stimano la tossicità e il comportamento farmacologico a partire dalla struttura chimica. Questi programmi hanno suggerito che tutti i prodotti di degradazione identificati rientrano in una fascia di tossicità moderata, ma i rischi previsti variano. Alcuni hanno mostrato segnali di possibili effetti su fegato, reni o sistema nervoso, mentre altri sembravano più benigni. Diversi sono stati segnalati per una potenziale attività cancerogena o genotossica, e la loro capacità di distribuirsi nell’organismo e attraversare la barriera emato-encefalica è risultata molto variabile. Sebbene queste previsioni non costituiscano prova di danno, indicano quali impurità meritano la più attenta valutazione sperimentale.
Cosa significa per i pazienti e i produttori di farmaci
Per le persone che assumono asciminib, lo studio non modifica l’uso clinico del farmaco, ma rafforza la rete di sicurezza intorno ad esso. Gli autori dimostrano che asciminib è abbastanza stabile nelle normali condizioni di conservazione, ma può formare un ristretto numero di prodotti di degradazione distintivi in condizioni più aggressive. Forniscono un metodo di laboratorio dettagliato per monitorare queste molecole e indizi iniziali basati su calcoli informatici su quali potrebbero essere più preoccupanti. Nel complesso, questo lavoro aiuta produttori e regolatori a monitorare la sicurezza a lungo termine di asciminib e offre un modello per valutare altri farmaci antitumorali con l’avanzare del tempo.
Citazione: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
Parole chiave: asciminib, degradazione del farmaco, impurità genotossiche, analisi HPLC, tossicità in silico