Clear Sky Science · sv
Strukturell och in silico-säkerhetsutvärdering av asciminibs nedbrytningsprodukter med en validerad stabilitetsindikerande HPLC-metod för bestämning av genotoxiska föroreningar
Varför säkerheten för ett cancerpiller förändras över tid
Många moderna cancerläkemedel tas under månader eller år, vilket innebär att tabletterna måste förbli säkra och effektiva under långa perioder. Men läkemedel bryts långsamt ner och bildar nya molekyler som aldrig ingick i den ursprungliga formulan. Denna studie undersöker hur leukemiläkemedlet asciminib sönderfaller under hårda förhållanden, hur man upptäcker de små nedbrytningsprodukterna och om datorverktyg tyder på att någon av dem kan vara skadlig.
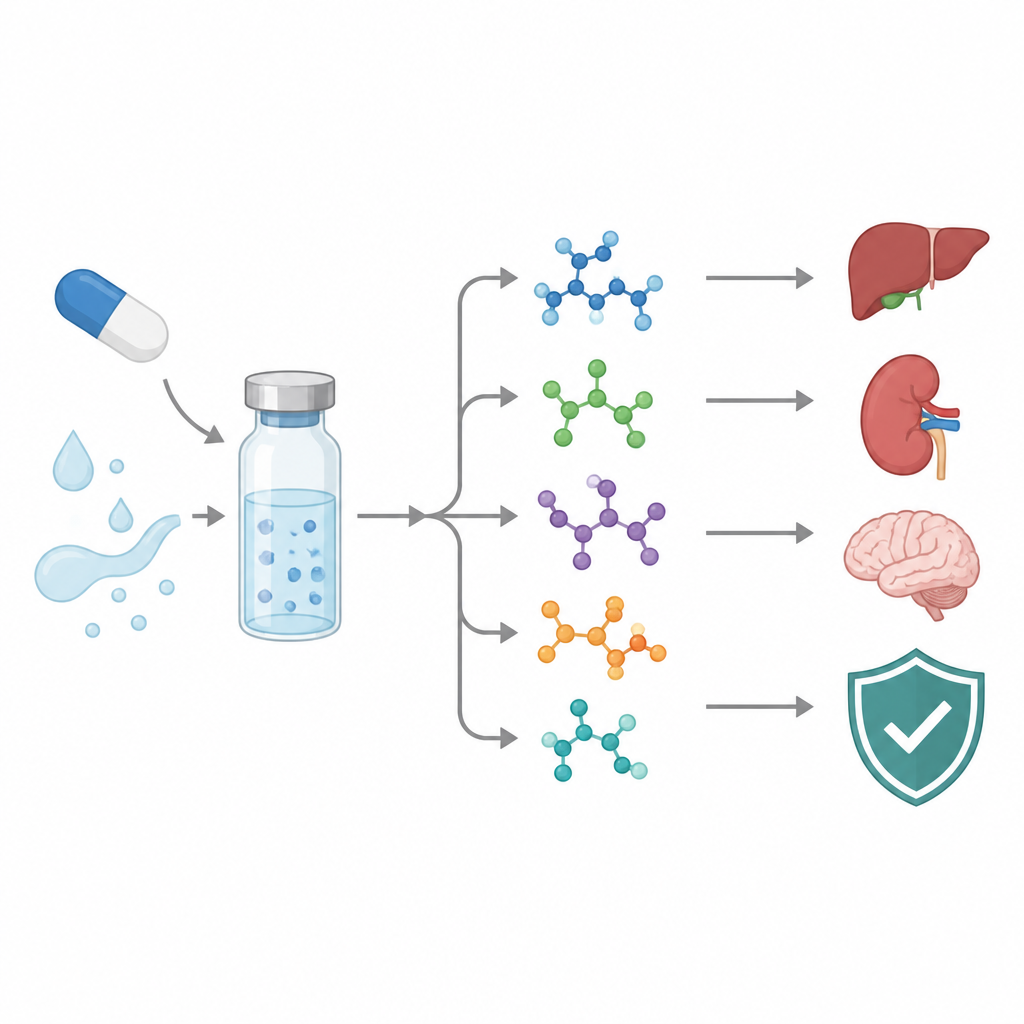
Följa ett cancerläkemedel när det bryts ner
Asciminib är en riktad tablett som används mot blodcancerformen kronisk myeloisk leukemi. Liksom alla läkemedel kan det reagera med syror, baser, ljus, värme eller syre under tillverkning, förvaring eller i kroppen. Dessa reaktioner skapar nedbrytningsprodukter, och några kan vara ”genotoxiska”, det vill säga skada DNA. Myndigheter kräver nu att företag söker efter sådana biprodukter, identifierar vad de är och håller deras nivåer under strikt kontroll. Forskarna satte därför upp projektet att kartlägga hur asciminib degraderar, identifiera de nya molekylerna som uppstår och utveckla ett praktiskt labbtest som separerar och mäter läkemedlet och dess föroreningar.
Bygga ett labbtest som ser de allra minsta spåren
Teamet designade och finslipade en vätskekromatografimetod, en grundläggande separationsmetod i läkemedelslaboratorier. De testade flera kolonner och lösningsmedelsblandningar innan de valde förhållanden som klart separerade asciminib från tre kända genotoxiska föroreningar och en rad okända nedbrytningsprodukter. Metoden kontrollerades för noggrannhet, känslighet och robusthet, enligt internationella riktlinjer. Den kunde upptäcka mycket låga föroreningsnivåer och visade konsekvent prestation även när förhållandena varierades något. Det gör den lämplig för rutinmässig kvalitetskontroll för att säkerställa att varje sats tabletter uppfyller strikta renhetsgränser.
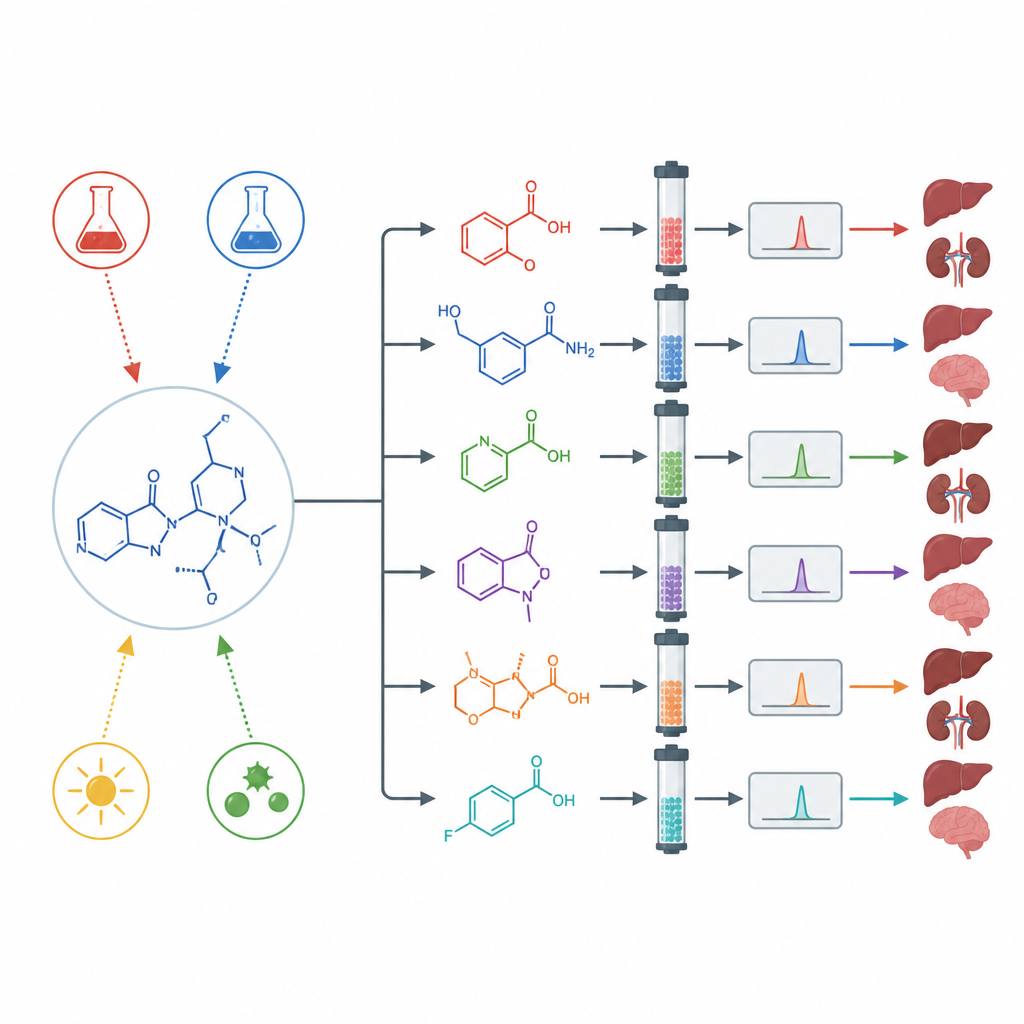
Stressa läkemedlet för att avslöja dolda biprodukter
För att se hur asciminib beter sig under extrema förhållanden genomförde forskarna så kallade ”forced degradation”-tester. De utsatte läkemedlet för stark syra, stark bas, oxiderande kemikalier, värme, vatten och starkt ljus inklusive ultraviolett. Under neutralt vatten, värme och normalt ljus förändrades läkemedlet knappt. Men under syra, bas, oxidanter och ultraviolett ljus bröts det ner tydligt och bildade flera distinkta nya molekyler. Med preparativ separation, högupplöst masspektrometri och kärnmagnetisk resonans isolerade teamet och bestämde strukturerna för flera nedbrytningsprodukter som bildades i varje typ av stress.
En titt på säkerhet och beteende med datorbaserade modeller
Eftersom det är långsamt och kostsamt att testa varje nedbrytningsprodukt i djur eller människor vände sig forskarna till in silico-verktyg som uppskattar toxicitet och läkemedelsliknande egenskaper från kemisk struktur. Dessa program föreslog att alla identifierade nedbrytningsprodukter hamnar i ett måttligt toxicitetsintervall, men deras förutsagda risker skiljer sig åt. Några visade signaler för möjliga lever-, njur- eller nervsystemseffekter, medan andra verkade mildare. Flera flaggades för potentiell cancerframkallande eller genpåverkande aktivitet, och deras förmåga att röra sig genom kroppen och passera in i hjärnan varierade kraftigt. Även om dessa prediktioner inte bevisar skada, pekar de ut vilka föroreningar som förtjänar närmast experimentell granskning.
Vad detta betyder för patienter och läkemedelstillverkare
För personer som tar asciminib förändrar studien inte hur läkemedlet används, men den stärker säkerhetsnätet kring det. Författarna visar att asciminib är ganska stabilt vid normal förvaring men kan bilda ett fåtal karaktäristiska nedbrytningsprodukter under hårdare förhållanden. De ger en detaljerad laboratoriemetod för att övervaka dessa molekyler och inledande datorbaserade ledtrådar om vilka som kan vara mer oroande. Tillsammans hjälper detta arbete tillverkare och myndigheter att följa asciminibs långsiktiga säkerhet och erbjuder en modell för att utvärdera andra cancerläkemedel när de åldras.
Citering: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
Nyckelord: asciminib, läkemedelsnedbrytning, genotoxiska föroreningar, HPLC-analys, in silico-toxikologi