Clear Sky Science · pl
Ocena strukturalna i in silico bezpieczeństwa produktów degradacji asciminibu wraz z walidowaną metodą HPLC wskazującą stabilność do oznaczania zanieczyszczeń genotoksycznych
Dlaczego bezpieczeństwo pigułki przeciwnowotworowej zmienia się w czasie
Wiele współczesnych leków przeciwnowotworowych przyjmuje się przez miesiące lub lata, co oznacza, że tabletki muszą pozostawać bezpieczne i skuteczne przez długi okres. Leki jednak stopniowo ulegają rozkładowi, tworząc nowe cząsteczki, które nie występowały w oryginalnym składzie. W tym badaniu analizowano, jak lek na białaczkę asciminib rozkłada się w warunkach stresowych, jak wykryć śladowe produkty degradacji oraz czy narzędzia komputerowe sugerują, że któreś z nich mogą być szkodliwe.
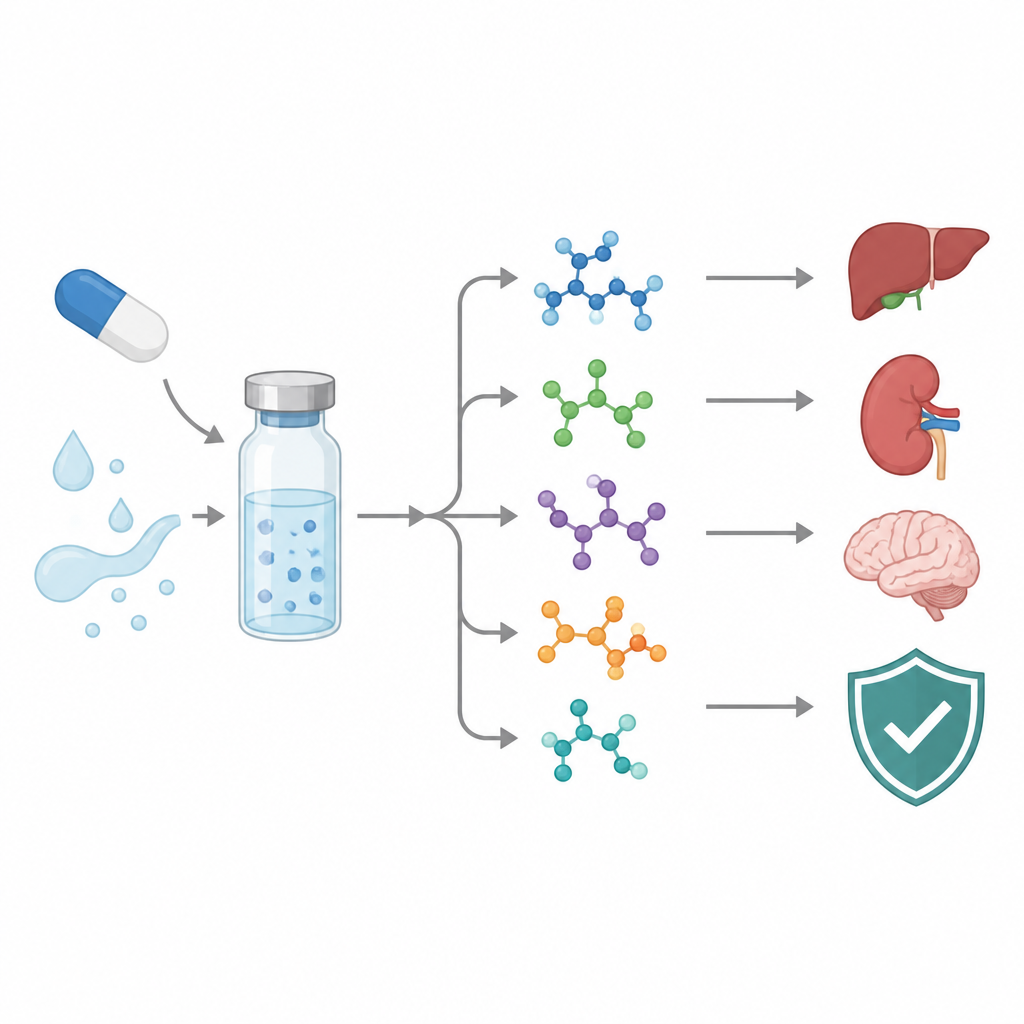
Śledzenie leku przeciwnowotworowego w czasie rozpadu
Asciminib to celowany lek stosowany w przewlekłej białaczce szpikowej. Jak wszystkie leki, może reagować z kwasami, zasadami, światłem, ciepłem lub tlenem podczas produkcji, przechowywania albo w organizmie. Reakcje te prowadzą do powstania produktów degradacji, z których kilka może być genotoksycznych, czyli potencjalnie uszkadzających DNA. Organy regulacyjne wymagają obecnie, by firmy wyszukiwały takie produkty uboczne, identyfikowały je i utrzymywały ich poziomy pod ścisłą kontrolą. Badacze postawili sobie za cel odwzorowanie sposobów degradacji asciminibu, identyfikację powstających nowych cząsteczek oraz opracowanie praktycznego testu laboratoryjnego, który rozdziela i mierzy lek oraz jego zanieczyszczenia.
Opracowanie testu laboratoryjnego wykrywającego najdrobniejsze ślady
Zespół zaprojektował i dopracował metodę chromatografii cieczowej, powszechnie stosowaną technikę rozdziału w laboratoriach farmaceutycznych. Przetestowali kilka kolumn i mieszanin rozpuszczalników, zanim wybrali warunki, które czysto rozdzielały asciminib od trzech znanych zanieczyszczeń genotoksycznych oraz szeregu nieznanych produktów degradacji. Metodę sprawdzono pod kątem dokładności, czułości i odporności, zgodnie z międzynarodowymi wytycznymi. Była zdolna wykrywać bardzo niskie poziomy zanieczyszczeń i wykazywała spójną wydajność nawet przy niewielkich zmianach warunków. To sprawia, że nadaje się do rutynowej kontroli jakości, aby zapewnić, że każda partia tabletek spełnia surowe limity czystości.
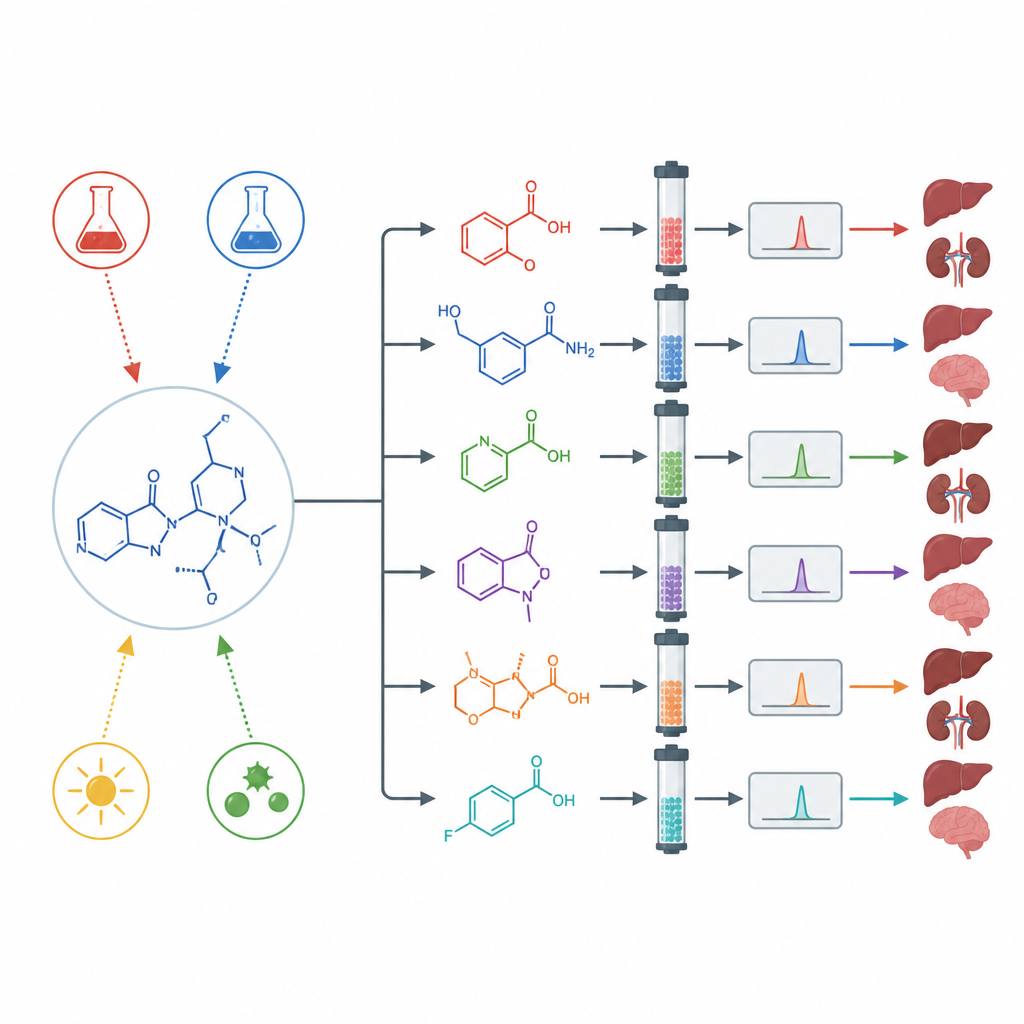
Obciążanie leku, by ujawnić ukryte produkty uboczne
Aby sprawdzić zachowanie asciminibu w skrajnych warunkach, naukowcy przeprowadzili testy „wymuszonej degradacji”. Poddali lek działaniu silnych kwasów, silnych zasad, utleniaczy, ciepła, wody oraz intensywnego światła, w tym ultrafioletu. W warunkach obojętnej wody, przy cieple i normalnym świetle lek prawie nie ulegał zmianie. Natomiast w środowisku kwaśnym, zasadowym, w obecności utleniaczy i promieniowania UV rozkładał się wyraźnie, tworząc kilka odrębnych nowych cząsteczek. Przy użyciu separacji preparatywnej, wysokorozdzielczej spektrometrii mas i jądrowego rezonansu magnetycznego zespół wyizolował i ustalił struktury wielu produktów degradacji powstających w każdym typie obciążenia.
Rzut oka na bezpieczeństwo i właściwości za pomocą modeli komputerowych
Ponieważ testowanie każdego produktu degradacji na zwierzętach lub ludziach jest czasochłonne i kosztowne, badacze sięgnęli po narzędzia in silico, które szacują toksyczność i właściwości podobne do leków na podstawie struktury chemicznej. Programy te sugerowały, że wszystkie zidentyfikowane produkty degradacji mieszczą się w przedziale umiarkowanej toksyczności, choć ich przewidywane ryzyko różniło się. Niektóre wykazywały sygnały możliwych skutków dla wątroby, nerek lub układu nerwowego, podczas gdy inne wyglądały na łagodniejsze. Kilka z nich zostało oznaczonych jako potencjalnie kancerogenne lub uszkadzające geny, a ich zdolność do przemieszczania się po organizmie i przenikania do mózgu była bardzo zróżnicowana. Chociaż te prognozy nie dowodzą szkodliwości, wskazują, które zanieczyszczenia zasługują na najbliższe badania eksperymentalne.
Co to oznacza dla pacjentów i producentów leków
Dla osób przyjmujących asciminib wyniki badania nie zmieniają sposobu stosowania leku, ale wzmacniają siatkę bezpieczeństwa wokół niego. Autorzy pokazują, że asciminib jest stosunkowo stabilny w normalnych warunkach przechowywania, ale w ostrzejszych warunkach może tworzyć kilka charakterystycznych produktów degradacji. Dostarczają szczegółową metodę laboratoryjną do monitorowania tych cząsteczek oraz wstępne, komputerowe wskazówki, które z nich mogą budzić większe obawy. Razem praca ta pomaga producentom i organom regulacyjnym śledzić długoterminowe bezpieczeństwo asciminibu i stanowi wzorzec do oceny innych leków przeciwnowotworowych w miarę ich starzenia się.
Cytowanie: Shaik, R.B., Padala, S.K.R., Gupta, M. et al. Structural and In silico safety evaluation of asciminib degradation products with a validated stability indicating HPLC method for genotoxic impurity determination. Sci Rep 16, 14965 (2026). https://doi.org/10.1038/s41598-026-44693-0
Słowa kluczowe: asciminib, degradacja leku, zanieczyszczenia genotoksyczne, analiza HPLC, toksyczność in silico