Clear Sky Science · zh
照射大鼠的中枢与外周镇痛:利血平诱导的疼痛模型
为何缓解长期疼痛至关重要
许多人每天都承受着常规止痛药只能部分缓解且常伴随令人不安副作用的疼痛。本研究探讨了一种不寻常的助力:极低剂量的伽马射线——与用于癌症治疗的高剂量同属一种能量。研究者在一种模拟广泛慢性疼痛特征的大鼠模型中,考察单次低剂量照射是否能安全减轻疼痛,以及在这种减痛发生时体内和大脑中可能发生的生物学变化。
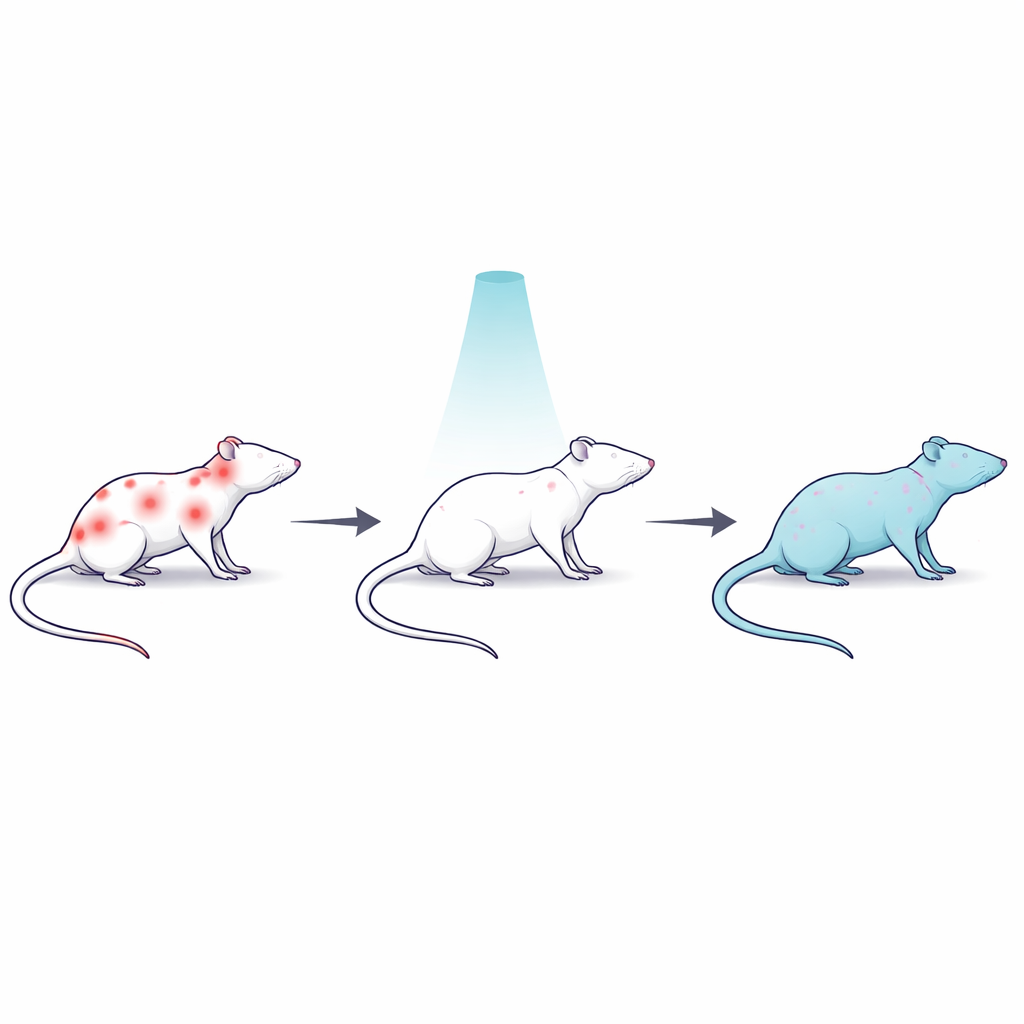
一种顽固全身疼痛的大鼠模型
为研究难治性疼痛,科研人员使用药物利血平,它会耗竭参与情绪与疼痛调控的关键脑内化学物质,并在大鼠中引起长期的肌肉与全身疼痛。30只雄性大鼠被分为若干组:健康对照组;未经处理的利血平组;接受单次全身低剂量伽马照射的利血平组;以及一组类似的照射组但同时给予纳洛酮(阻断脑内阿片受体的药物);还有一组利血平但接受常用抗炎止痛药双氯芬酸治疗。该设计使团队能将放射治疗与标准药物比较,并检验体内类似阿片系统是否参与任何观察到的镇痛效应。
评估疼痛并探查大脑
研究者通过两种方法测量疼痛。在尾巴抽动(tail‑flick)测试中,将大鼠尾部放入温水中,尾巴抽动所需的时间反映外周神经的痛觉敏感性。在Haffner尾夹(tail‑clip)测试中,在尾根附近轻夹一个小夹子,大鼠转身咬夹子的反应时间反映脊髓与大脑对疼痛的处理。完成这些测试后,科研人员收集血液与脑组织,以测量与疼痛及组织应激相关的标志物:血液中的P物质和肿瘤坏死因子‑α(均与疼痛和炎症相关),以及脑组织中的一氧化氮和丙二醛(氧化或“类似生锈”的应激信号)和多巴胺(一种参与情绪与疼痛调控的神经递质)。
放射令人意外的镇痛格局
利血平使大鼠在两种测试中均表现出更高的痛觉敏感性并扰乱其内在化学平衡:氧化应激标志物和炎症信号上升,而脑内多巴胺下降。单次低剂量伽马照射逆转了其中很多改变。两种测试中的疼痛反应时间延长,意味着大鼠在反应前能容忍更多不适。对于由尾部外周神经传导的疼痛,放射的效应与双氯芬酸相似。对于涉及脊髓与大脑的疼痛,放射同样降低了敏感性,但在先给予纳洛酮时这种益处大部分消失。这一模式提示,低剂量照射至少部分地激发了体内类似阿片的镇痛系统,同时也抑制了过度活跃的神经。
化学“风暴”减弱,更趋平衡
在化学层面,放射明显缓和了利血平引发的内在“风暴”。脑内的一氧化氮与丙二醛水平下降至接近正常,表明氧化应激减轻。先前被利血平抑制的脑内多巴胺含量在照射后回升。血液中升高的炎性信使肿瘤坏死因子‑α和与疼痛相关的神经肽P物质在低剂量照射后均下降。用纳洛酮阻断阿片受体并未逆转这些抗氧化和抗炎学上的改变,表明放射的化学平抑作用与其与阿片相关的信号效应在一定程度上是分离的。双氯芬酸也改善了许多这些指标,但与标准药物不同,低剂量放射仅需单次照射且不具有长期抗炎药已知的胃肠和心血管风险。
这对未来疼痛治疗的可能意义
通俗地说,该研究表明经过精确控制的低剂量伽马照射可使感觉疼痛的神经不那么过度兴奋,帮助恢复保护性的大脑化学物质,并抑制促进慢性疼痛的氧化与炎症信号。该工作仅在单一大鼠模型、使用一种照射剂量并在一个短时间点进行,因此尚无法直接推广到患者。然而,这支持了临床观察:低剂量放射疗法可缓解顽固的关节与肌腱疼痛,并指出了具体的生物学通路——抗氧化防御、炎症控制与与阿片相关的神经回路——未来基于放射或药物的靶向疗法可能安全利用这些通路来帮助饱受慢性疼痛的人群。
引用: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
关键词: 慢性疼痛, 低剂量放射, 氧化应激, 炎症, 阿片通路