Clear Sky Science · it
Analgesia centrale e periferica in ratti irradiati: modello di dolore indotto da reserpina
Perché attenuare il dolore prolungato è importante
Molte persone convivono con un dolore quotidiano che i comuni analgesici alleviano solo in parte e che spesso è accompagnato da effetti collaterali fastidiosi. Questo studio esplora un aiuto insolito: dosi molto basse di radiazione gamma, lo stesso tipo di energia usata a livelli molto più alti nel trattamento del cancro. Utilizzando un modello su ratto che riproduce alcuni aspetti del dolore cronico diffuso, i ricercatori hanno verificato se una singola dose bassa di radiazione potesse ridurre il dolore in modo sicuro e cosa potrebbe accadere nell’organismo e nel cervello quando ciò avviene.
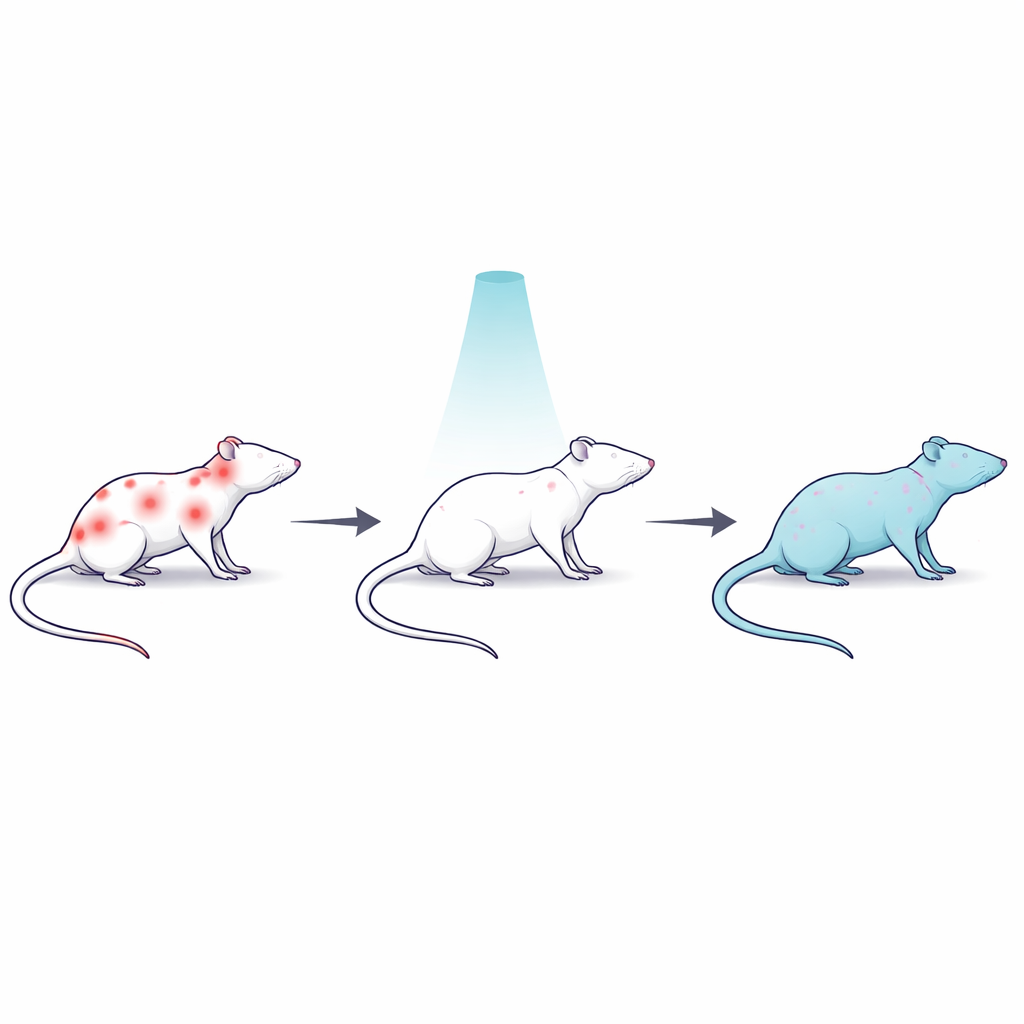
Un modello di dolore resistente e diffuso nel ratto
Per studiare il dolore difficile da trattare, gli scienziati hanno usato la reserpina, un farmaco che depleta sostanze cerebrali chiave coinvolte nell’umore e nel controllo del dolore e provoca nei ratti un dolore muscolare e generalizzato di lunga durata. Trentadue ratti maschi sono stati divisi in più gruppi: un gruppo controllo sano; un gruppo trattato con reserpina non sottoposto a terapia; un gruppo con reserpina che ha ricevuto una singola dose corporea totale di radiazione gamma a bassa dose; un gruppo irradiato simile che ha ricevuto anche naloxone, un farmaco che blocca i recettori oppioidi nel cervello; e un gruppo con reserpina trattato con il comune antinfiammatorio diclofenac. Questo disegno sperimentale ha permesso al team di confrontare la radiazione con un farmaco standard e di verificare se i sistemi oppioidi endogeni contribuiscano all’eventuale sollievo dal dolore.
Valutare il dolore e analizzare il cervello
I ricercatori hanno misurato il dolore in due modi. Nel test del riflesso della coda (tail‑flick), la coda del ratto viene immersa in acqua calda e il tempo impiegato per ritirarla riflette la sensibilità del dolore nelle fibre nervose periferiche. Nel test di Haffner (tail‑clip), una piccola clip è applicata delicatamente vicino alla base della coda e il tempo prima che il ratto reagisca girandosi per mordere riflette l’elaborazione del dolore a livello di midollo spinale e cervello. Dopo questi test, gli scienziati hanno raccolto sangue e tessuto cerebrale per misurare marker collegati al dolore e allo stress tissutale: sostanza P e fattore di necrosi tumorale‑alfa (entrambi associati a dolore e infiammazione) nel sangue, e ossido nitrico e malondialdeide (indicatori di stress ossidativo) oltre alla dopamina (un mediatore coinvolto nell’umore e nel controllo del dolore) nel cervello.
Il sorprendente effetto analgesico della radiazione
La reserpina ha reso i ratti molto più sensibili al dolore in entrambi i test e ha alterato la loro chimica interna: i marker di stress ossidativo e i segnali infiammatori sono aumentati, mentre la dopamina cerebrale è diminuita. Una singola bassa dose di radiazione gamma ha invertito molte di queste modificazioni. Le risposte al dolore in entrambi i test sono state ritardate, il che significa che i ratti hanno tollerato maggiore disagio prima di reagire. Per il dolore trasmesso dai nervi della coda, l’effetto della radiazione è risultato simile a quello del diclofenac. Per il dolore che coinvolge midollo spinale e cervello, la radiazione ha nuovamente ridotto la sensibilità, ma questo beneficio è scomparso in gran parte quando è stato somministrato prima il naloxone. Questo schema suggerisce che la radiazione a bassa dose attiva, almeno in parte, i sistemi oppioidi endogeni di attenuazione del dolore oltre a moderare l’iperattività delle vie nervose.
Meno “tempesta” chimica, più equilibrio
A livello chimico, la radiazione ha attenuato chiaramente la “tempesta” interna scatenata dalla reserpina. I livelli di ossido nitrico e di malondialdeide nel cervello sono diminuiti verso valori normali, indicando una riduzione dello stress ossidativo. Il contenuto cerebrale di dopamina, depresso dalla reserpina, è aumentato dopo l’irradiazione. Nel sangue, sia il messaggero infiammatorio fattore di necrosi tumorale‑alfa sia la neuropeptide legata al dolore sostanza P sono diminuiti dopo la bassa dose. Il blocco dei recettori oppioidi con naloxone non ha annullato questi cambiamenti antiossidanti e anti‑infiammatori, indicando che l’effetto calmante chimico della radiazione e i suoi effetti mediati da vie oppioidi sono almeno in parte separati. Anche il diclofenac ha migliorato molte di queste misure, ma a differenza dei farmaci standard, la radiazione a bassa dose lo ha fatto con una singola esposizione e senza i noti rischi digestivi e cardiovascolari legati all’uso prolungato di anti‑infiammatori.
Cosa potrebbe significare per la cura del dolore in futuro
In termini pratici, lo studio suggerisce che una dose controllata e bassa di radiazione gamma può rendere meno reattive le fibre nervose sensoriali, contribuire a ristabilire sostanze cerebrali protettive e attenuare sia i segnali ossidativi sia quelli infiammatori che alimentano il dolore cronico. Il lavoro è stato condotto in un singolo modello su ratto con una sola dose di radiazione e un unico punto temporale a breve termine, quindi non può essere trasferito direttamente ai pazienti. Tuttavia, supporta osservazioni cliniche secondo cui la radioterapia a bassa dose può alleviare dolori ostinati di articolazioni e tendini, e indica percorsi biologici concreti — difese antiossidanti, controllo dell’infiammazione e circuiti nervosi legati agli oppioidi — che terapie future mirate, basate sia sulla radiazione sia su farmaci, potrebbero sfruttare in sicurezza per aiutare le persone che vivono con dolore cronico.
Citazione: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
Parole chiave: dolore cronico, radiazione a bassa dose, stress ossidativo, infiammazione, vie degli oppioidi