Clear Sky Science · nl
Centraal en perifeer analgetisch effect bij bestraalde ratten: reserpine-geïnduceerd pijnmodel
Waarom verlichting van langdurige pijn belangrijk is
Veel mensen leven met dagelijkse pijn die standaard pijnstillers slechts deels verlichten en die vaak gepaard gaat met onaangename bijwerkingen. Deze studie onderzoekt een ongebruikelijke hulpbron: zeer lage doses gammastraling, hetzelfde type energie dat in veel hogere doses voor kankerbehandelingen wordt gebruikt. Met een rattenmodel dat enkele kenmerken van chronische wijdverspreide pijn nabootst, onderzochten de onderzoekers of een enkele lage stralingsdosis veilig pijn kan verminderen en wat er in lichaam en hersenen zou kunnen gebeuren wanneer dat het geval is.
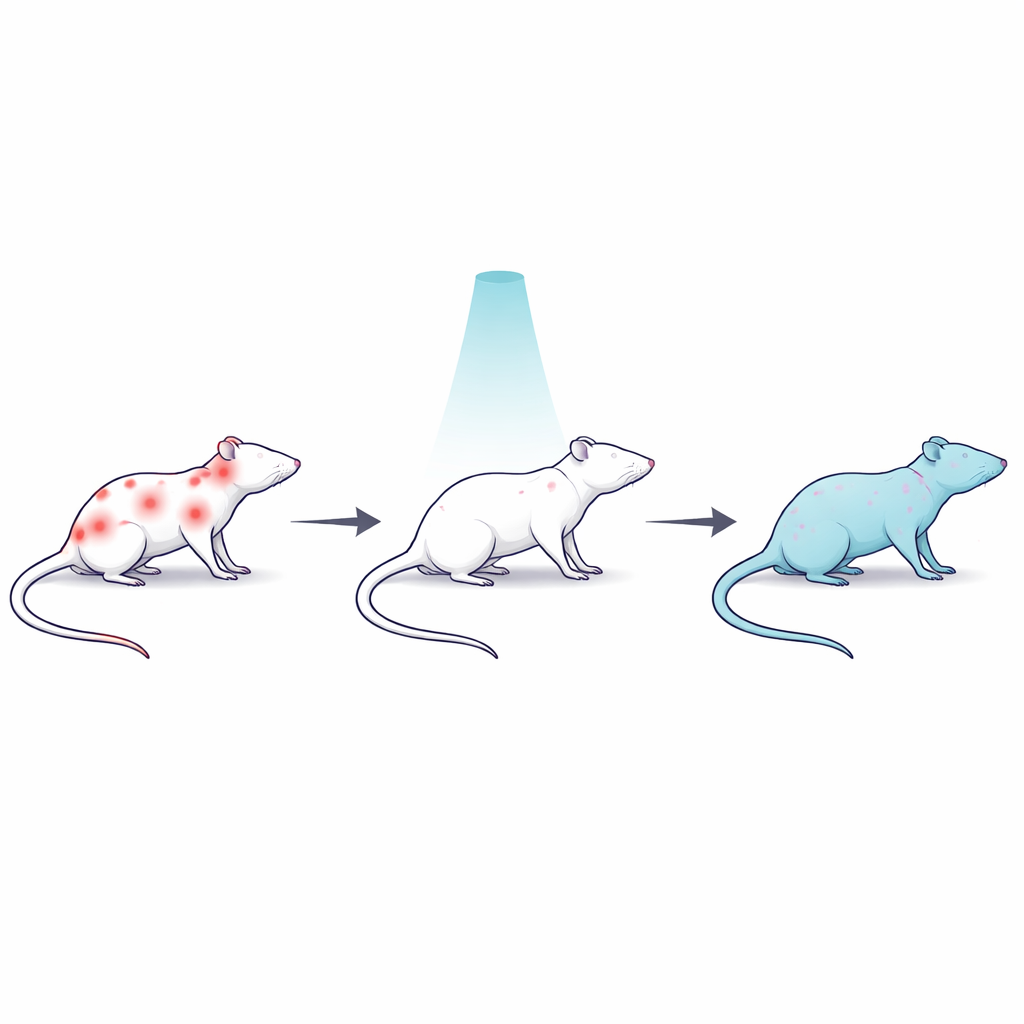
Een rattenmodel van hardnekkige, lichaamsbrede pijn
Om moeilijk behandelbare pijn te bestuderen, gebruikten de wetenschappers het middel reserpine, dat belangrijke hersenchemicaliën die betrokken zijn bij stemming en pijncontrole uitput en langdurige spier- en lichaamspijn bij ratten veroorzaakt. Dertig mannelijke ratten werden in meerdere groepen verdeeld: een gezonde controlegroep; een reserpine-groep met onbehandelde pijn; een reserpine-groep die een enkele hele-lichaam lage dosis gammastraling kreeg; een vergelijkbare bestraalde groep die ook naloxon kreeg, een middel dat opioïde receptoren in de hersenen blokkeert; en een reserpine-groep behandeld met de veelgebruikte ontstekingsremmende pijnstiller diclofenac. Dit ontwerp stelde het team in staat straling te vergelijken met een standaardmedicijn en te testen of het lichaamseigen opioïde systeem bijdroeg aan eventuele pijnverlichting.
Pijn testen en de hersenen onderzoeken
De onderzoekers maten pijn op twee manieren. Bij de staart‑flikkertest wordt de staart van de rat in warm water geplaatst en de tijd tot de staart wegflikkert weerspiegelt pijngevoeligheid in de zenuwen buiten de hersenen en het ruggenmerg. Bij Haffner’s staart‑klemtest wordt een kleine klem zachtjes bij de staartbasis aangebracht, en de tijd voordat de rat reageert door zich om te draaien en te bijten weerspiegelt pijnverwerking in het ruggenmerg en de hersenen. Na deze tests verzamelden de wetenschappers bloed en hersenweefsel om markers te meten die verband houden met pijn en weefselstress: substance P en tumor necrosis factor‑alpha (beide geassocieerd met pijn en ontsteking) in het bloed, en stikstofmonoxide en malondialdehyde (signaleren van oxidatieve, of “roestachtige,” stress) plus dopamine (een boodschapper betrokken bij stemming en pijncontrole) in de hersenen.
Het verrassende pijnstillende patroon van straling
Reserpine maakte de ratten veel gevoeliger voor pijn in beide tests en verstoorde hun interne chemie: markers van oxidatieve stress en ontstekingssignalen stegen, terwijl dopamine in de hersenen daalde. Een enkele lage dosis gammastraling keerde veel van deze veranderingen om. Pijnreacties in beide tests werden vertraagd, wat betekent dat de ratten meer ongemak tolereerden voordat ze reageerden. Voor pijn die door zenuwen in de staart wordt geleid, was het effect van straling vergelijkbaar met dat van diclofenac. Voor pijn die het ruggenmerg en de hersenen betrof, verminderde straling opnieuw de gevoeligheid, maar dit voordeel verdween grotendeels wanneer eerst naloxon werd toegediend. Dat patroon suggereert dat lage-dosis straling, naast het dempen van overactieve zenuwen, deels het lichaamseigen opioïde‑achtige pijnonderdrukkende systeem activeert.
Minder chemische “storm”, meer evenwicht
Op chemisch niveau verzachtte straling duidelijk de interne “storm” die door reserpine werd veroorzaakt. Niveaus van stikstofmonoxide en malondialdehyde in de hersenen daalden richting normaal, wat wijst op minder oxidatieve stress. Het dopaminegehalte in de hersenen, dat door reserpine was verlaagd, herstelde zich na bestraling. In het bloed daalden het verhoogde ontstekingssignaal tumor necrosis factor‑alpha en het aan pijn gerelateerde neuropeptide substance P na de lage dosis. Het blokkeren van opioïde receptoren met naloxon zette deze antioxidant- en ontstekingsremmende verschuivingen niet terug, wat aangeeft dat de chemische kalmering door straling en de opioïde-gerelateerde signaleringseffecten ten minste gedeeltelijk gescheiden zijn. Diclofenac verbeterde ook veel van deze maten, maar in tegenstelling tot standaardmiddelen deed lage-dosis straling dit met één enkele blootstelling en zonder de bekende maag-darm- en cardiovasculaire risico’s van langdurig gebruik van ontstekingsremmers.
Wat dit kan betekenen voor toekomstige pijnzorg
Simpel gezegd suggereert de studie dat een zorgvuldig gecontroleerde, lage dosis gammastraling pijnzintuiglijke zenuwen minder prikkelbaar kan maken, kan helpen beschermende hersenchemicaliën te herstellen en zowel oxidatieve als ontstekingssignalen stil kan leggen die chronische pijn in stand houden. Het onderzoek is uitgevoerd in één rattenmodel met één stralingsdosis en slechts één kort tijdsvenster, dus het kan nog niet direct op patiënten worden vertaald. Toch ondersteunt het klinische waarnemingen dat lage-dosis radiotherapie hardnekkige gewrichts- en peespijn kan verlichten, en het wijst op concrete biologische routes — antioxidantafweer, ontstekingsregulatie en opioïde-gerelateerde zenuwcircuits — die toekomstige gerichte therapieën, hetzij op basis van straling of medicijnen, veilig zouden kunnen benutten om mensen met chronische pijn te helpen.
Bronvermelding: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
Trefwoorden: chronische pijn, lage-dosis straling, oxiderende stress, ontsteking, opioïde routes