Clear Sky Science · pl
Analgezja centralna i obwodowa u naświetlanych szczurów: model bólu indukowany rezerpiną
Dlaczego łagodzenie bólu trwającego długo ma znaczenie
Wiele osób żyje z codziennym bólem, który typowe środki przeciwbólowe tylko częściowo łagodzą i który często wiąże się z niepożądanymi skutkami ubocznymi. Badanie to analizuje nietypowego pomocnika: bardzo niskie dawki promieniowania gamma, tej samej formy energii stosowanej w znacznie wyższych dawkach w leczeniu nowotworów. W modelu szczura odwzorowującym pewne cechy przewlekłego, rozlanego bólu zespół badawczy sprawdził, czy pojedyncza niska dawka promieniowania może bezpiecznie zmniejszyć ból i co może dziać się w organizmie i mózgu, gdy tak się dzieje.
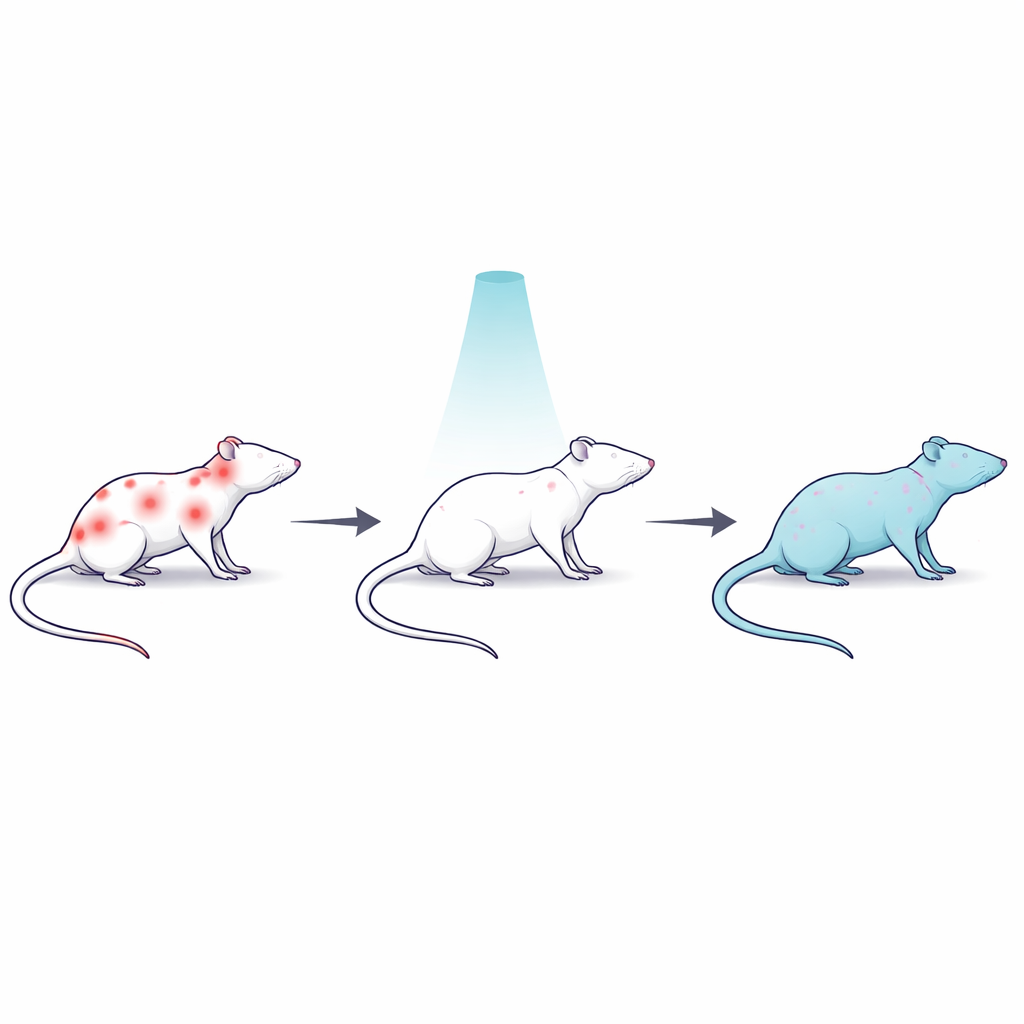
Model szczura z uporczywym, obejmującym całe ciało bólem
Aby badać trudny do leczenia ból, naukowcy użyli rezerpiny, leku wyczerpującego kluczowe neuroprzekaźniki mózgowe zaangażowane w nastrój i kontrolę bólu, co u szczurów wywołuje długotrwały ból mięśni i całego ciała. Trzydzieści samców szczurów podzielono na kilka grup: zdrową grupę kontrolną; grupę poddaną rezerpinie bez leczenia; grupę po rezerpinie, która otrzymała pojedynczą niską dawkę promieniowania gamma na całe ciało; podobną grupę naświetlaną, która dodatkowo otrzymała nalokson, lek blokujący receptory opioidowe w mózgu; oraz grupę po rezerpinie leczoną powszechnym lekiem przeciwzapalnym diklofenakiem. Taki układ pozwolił zespółowi porównać promieniowanie z standardowym lekiem i sprawdzić, czy własne systemy podobne do opioidów w organizmie przyczyniają się do ewentualnego złagodzenia bólu.
Badanie bólu i analiza mózgu
Naukowcy mierzyli ból na dwa sposoby. W teście odruchu ogona (tail‑flick) ogon szczura umieszczano w ciepłej wodzie, a czas do odskoczenia odzwierciedlał wrażliwość bólową nerwów obwodowych. W teście Haffnera z klipsem przy nasadzie ogona niewielki klips był delikatnie zakładany, a czas do reakcji, gdy szczur obracał się, by ugryźć, odzwierciedlał przetwarzanie bólu w rdzeniu kręgowym i mózgu. Po tych testach naukowcy pobrali krew i tkankę mózgową, by zmierzyć markery związane z bólem i stresem tkankowym: substancję P i czynnik martwicy nowotworów alfa (oba związane z bólem i zapaleniem) we krwi oraz tlenek azotu i malondialdehyd (oznaki stresu oksydacyjnego, „rdzewienia”) oraz dopaminę (neuroprzekaźnik zaangażowany w nastrój i kontrolę bólu) w mózgu.
Zaskakujący wzorzec przeciwbólowy po promieniowaniu
Rezerpina zwiększyła wrażliwość szczurów na ból w obu testach i zaburzyła ich wewnętrzną chemię: wzrosły markery stresu oksydacyjnego i sygnały zapalne, podczas gdy poziom dopaminy w mózgu spadł. Pojedyncza niska dawka promieniowania gamma odwróciła wiele z tych zmian. Reakcje bólowe w obu testach były opóźnione, co oznacza, że szczury dłużej tolerowały dyskomfort zanim zareagowały. W przypadku bólu przenoszonego przez nerwy ogona efekt promieniowania był podobny do działania diklofenaku. W przypadku bólu obejmującego rdzeń kręgowy i mózg promieniowanie również zmniejszyło wrażliwość, ale korzyść ta w dużej mierze znikała po podaniu naloksonu. Taki wzorzec sugeruje, że niskodawkowe promieniowanie uruchamia przynajmniej częściowo własne systemy przeciwbólowe przypominające opioidy organizmu, oprócz uspokajania nadmiernie aktywnych nerwów.
Mniej chemicznej „burzy”, więcej równowagi
Na poziomie chemicznym promieniowanie wyraźnie złagodziło wewnętrzną „burzę” wywołaną przez rezerpinę. Poziomy tlenku azotu i malondialdehydu w mózgu obniżyły się w kierunku normy, co wskazuje na zmniejszenie stresu oksydacyjnego. Zawartość dopaminy w mózgu, która była obniżona przez rezerpinę, odbiła po naświetleniu. We krwi podwyższony czynnik zapalny TNF‑alfa oraz związana z bólem neuropeptyd substancja P spadły po niskiej dawce. Zablokowanie receptorów opioidowych naloksonem nie cofnęło tych antyoksydacyjnych i przeciwzapalnych zmian, co wskazuje, że chemiczne uspokojenie wywołane promieniowaniem i jego efekty związane z sygnalizacją opioidową są przynajmniej częściowo odrębne. Diklofenak również poprawił wiele z tych wskaźników, ale w przeciwieństwie do standardowych leków niskodawkowe promieniowanie osiągnęło to po pojedynczej ekspozycji i bez znanych ryzyk żołądkowo‑czerwiowych oraz sercowo‑naczyniowych związanych z długotrwałym stosowaniem leków przeciwzapalnych.
Co to może oznaczać dla przyszłej opieki nad bólem
Mówiąc prosto, badanie sugeruje, że starannie kontrolowana, niska dawka promieniowania gamma może sprawić, że nerwy czuciowe bólu będą mniej reaktywne, pomóc przywrócić ochronne neurochemikalia mózgu oraz uciszyć zarówno sygnały oksydacyjne, jak i zapalne, które napędzają ból przewlekły. Praca została wykonana w jednym modelu szczura z jedną dawką promieniowania i tylko jednym krótkim punktem czasowym, więc nie można jej jeszcze bezpośrednio przełożyć na pacjentów. Mimo to wspiera obserwacje kliniczne, że niskodawkowa radioterapia może łagodzić uporczywy ból stawów i ścięgien, i wskazuje konkretne ścieżki biologiczne — mechanizmy antyoksydacyjne, kontrolę zapalenia i obwody nerwowe związane z opioidami — które przyszłe, celowane terapie, czy oparte na promieniowaniu, czy na lekach, mogłyby bezpiecznie wykorzystać, by pomóc osobom żyjącym z przewlekłym bólem.
Cytowanie: Saif-Elnasr, M. Central and peripheral analgesia in irradiated rats: reserpine-induced pain model. Sci Rep 16, 12193 (2026). https://doi.org/10.1038/s41598-026-44637-8
Słowa kluczowe: ból przewlekły, niskodawkowe promieniowanie, stres oksydacyjny, zapalanie, szlaki opioidowe